-
下列叙述中不正确的是
A. 质量是国际单位制(SI)的七个基本单位之一
B. 电流是国际单位制中安培(A)衡量的物理量
C. 物质的量是含有一定数目粒子集合体的物理量
D. 物质的量常用符号n表示,其单位是摩尔(mol)
难度: 简单查看答案及解析
-
某无色溶液放入铝片后有氢气产生,下列离子在该溶液中一定不能大量存在的是( )
A. SO42- B. Cu2+ C. K+ D. OH-
难度: 简单查看答案及解析
-
下列实验操作中都正确的选项是( )
①用剩的药品为避免浪费应放回原瓶
②蒸发氯化钠溶液时要用玻璃棒不断搅拌
③称取易潮解的药品必须放在玻璃器皿中称量
④用试纸检验气体性质时,手拿着试纸经水润湿后靠近气体观察试纸颜色变化
A.②③ B.②③④ C.②④ D.①②③④
难度: 中等查看答案及解析
-
能证明某溶液中含有氯化钠的是( )
A. 焰色反应是黄色
B. 溶液有咸味
C. 取少量溶液于试管中,滴加稀硝酸酸化的硝酸银溶液,出现白色沉淀
D. 焰色反应是黄色,同时又能与硝酸酸化的硝酸银溶液反应生成白色沉淀
难度: 简单查看答案及解析
-
下列关于硫的叙述中不正确的是( )
A.试管内壁附着的硫可用二硫化碳溶解除去
B.硫在自然界中只能以硫化物和硫酸盐的形态存在
C.化石燃料的大量燃烧是空气中二氧化硫含量升高的原因
D.分离黑火药中的硝酸钾、木炭、硫要用到二硫化碳、水及过滤操作
难度: 中等查看答案及解析
-
mg某金属M与足量盐酸完全反应,生成MCl2和nmol氢气,则该金属的相对原子质量为( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
今有0.1mol/LNa2SO4溶液300 mL,0.1mol/LMgSO4溶液200 mL和0.1mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子的物质的量浓度之比是
A.1∶1∶1 B.1∶1∶3 C.3∶2∶3 D.3∶2∶2
难度: 简单查看答案及解析
-
在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是
A.m=4;R3+是还原剂 B.m=y;R3+是氧化产物
C.m=2;R3+是氧化剂 D.m=y;R3+是还原产物
难度: 简单查看答案及解析
-
已知浓硫酸的密度为1.84 g·cm-3,质量分数为98%,则求硫酸物质的量浓度时,下面算式中正确的是( )
A.
=18.4 mol·L-1
B.
=18.4 mol·L-1
C.
=18.4 mol·L-1
D.
=18.4 mol·L-1
难度: 简单查看答案及解析
-
从20%的氢氧化钠溶液中取出5 g,所取出的溶液与原溶液的溶质质量分数相比( )
A.变小 B.变大 C.不变 D.无法判断
难度: 简单查看答案及解析
-
在做氨的催化氧化实验时,铂丝不能接触氨水,原因是( )
A.铂丝温度高,接触氨水会使氨气大量逸出
B.防止铂丝温度降低而不能起催化作用
C.红热铂丝会与氨水反应,使铂丝腐蚀
D.防止爆炸
难度: 简单查看答案及解析
-
铝用作焊接钢轨是利用
A.铝同氧气反应生成稳定的保护层 B.铝是热的良导体
C.铝合金强度大 D.铝是强还原剂,铝热反应放热
难度: 简单查看答案及解析
-
下列物质中不能电离出酸根离子的是( )
A. Ca(OH)2 B. KMnO4 C. KClO3 D. NaHSO4
难度: 中等查看答案及解析
-
标准状况下,将盛满二氧化氮的大试管倒扣在盛水的水槽中,充分吸收后,试管内溶液的物质的量浓度是
A. 0.045 mol·L-1 B. 0.036 mol·L-1
C. 0.033 mol·L-1 D. 0.018 mol·L-1
难度: 困难查看答案及解析
-
下列物质中,同时含有氯分子、氯离子和氯的含氧化合物的是( )
A.液氯 B.氯水 C.氯酸钾 D.次氯酸钙
难度: 简单查看答案及解析
-
2.3 g纯净的金属钠在干燥的空气中缓慢加热,被氧化后得到3.5 g固体,由此可判断出产物是( )
A.氧化钠 B.过氧化钠
C.氧化钠和过氧化钠的混合物 D.无法确定
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. CO2溶于水能导电,因此CO2是电解质
B. KHSO4只有在电流作用下才能电离成K+、H+和SO42-
C. 强电解质溶液的导电能力不一定都强;弱电解质溶液的导电能力不一定都弱
D. AgCl难溶于水,所以AgCl是弱电解质;醋酸铅易溶于水,所以醋酸铅是强电解质
难度: 中等查看答案及解析
-
将钠放入盛有空气的密闭容器中,生成Na2O还是Na2O2是由下列哪项因素所决定的( )
A.反应温度 B.空气的量 C.钠粒的大小 D.钠的状态(s、l)
难度: 简单查看答案及解析
-
下图为蒸馏实验装置图,图中标示的四种仪器名称不正确的是( )
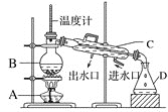
A. 酒精灯 B. 蒸馏烧瓶 C. 冷凝管 D. 烧瓶
难度: 简单查看答案及解析
-
关于硫酸铜的下列说法中不正确的是( )
A.无水硫酸铜是一种白色粉末
B.硫酸铜俗称蓝矾、胆矾
C.蓝矾的摩尔质量为250g·mol-1
D.实验室常用无水硫酸铜检验水的存在
难度: 简单查看答案及解析
-
下列关于氨的说法正确的是 ( )
A.氨气是无色无味的气体 B.氨气极易溶于水
C.可用向上排空气法收集 D.液氨和氨水是同一物质
难度: 简单查看答案及解析
-
将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
A.稀硝酸 B.稀盐酸 C.硝酸铜 D.氢氧化钠
难度: 中等查看答案及解析
-
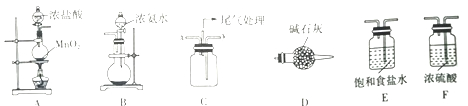
下列关于实验室用二氧化锰制取氯气的叙述不正确的是
A. 二氧化锰与浓盐酸共热 B. 缓慢加热反应
C. 用向下排空气法收集氯气 D. 多余氯气常用较浓的碱液吸收
难度: 中等查看答案及解析
-
质量比为2∶3的金属铝分别跟足量稀硫酸和氢氧化钠溶液反应,则产生氢气体积比是 ( )
A.1∶2 B.1∶3 C.2∶3 D.3∶2
难度: 简单查看答案及解析
-
电解质氯化钠溶液能导电是因为( )
A.氯化钠是一种化合物 B.氯化钠易溶于水
C.溶于水时产生自由移动的离子 D.通电时产生自由移动的离子
难度: 简单查看答案及解析
-
在Cl2+H2O=HCl+HClO中,水是( )
A.只作氧化剂 B.只作还原剂
C.既作氧化剂又作还原剂 D.既不是氧化剂又不是还原剂
难度: 简单查看答案及解析
-
金属钙的冶炼方法是电解法,这一事实说明了( )
A. 金属钙离子易得电子变成金属钙原子 B. 金属钙是不活泼的金属元素
C. 金属钙原子易失去电子变成钙离子 D. 金属钙离子的氧化性很强
难度: 中等查看答案及解析


 e.
e.