-
金属铜的提炼多从黄铜矿开始。黄铜矿在焙烧过程中主要反应之一的化学方程式为:
2CuFeS2 + O2 = Cu2S + 2FeS + SO2,下列说法不正确的是
A.O2只做氧化剂
B.CuFeS2既是氧化剂又是还原剂
C.SO2既是氧化产物又是还原产物
D.若有1 mol O2参加反应,则反应中共有4 mol电子转移
难度: 中等查看答案及解析
-
目前,我国上海、北京等各大城市已实行垃圾分类,下列垃圾可以置于第④个垃圾桶的是
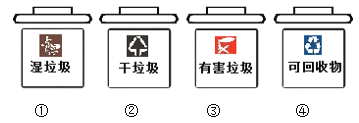
A.水果皮 B.残破瓷砖 C.牛奶包装纸盒 D.废电池
难度: 简单查看答案及解析
-
化学与生活、环境密切相关。下列说法正确的是
A.明矾在水中生成的
胶体有吸附性,因此常用明矾对水进行消毒
B.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
C.氨气很容易液化,液氨汽化吸收大量的热,所以液氨常用作制冷剂
D.为了消除碘缺乏病,在食用盐中加入一定量的碘单质
难度: 中等查看答案及解析
-
下列化学用语对事实的表述不正确的是
A.硬脂酸与乙醇的酯化反应:
B.常温时,
氨水的
,NH3•H2O ⇌
+
C.次氯酸的结构式为:
D.电解精炼铜的阴极反应:
难度: 中等查看答案及解析
-
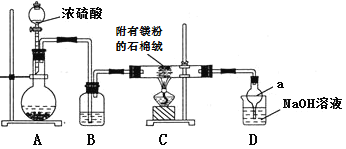
下列实验合理的是
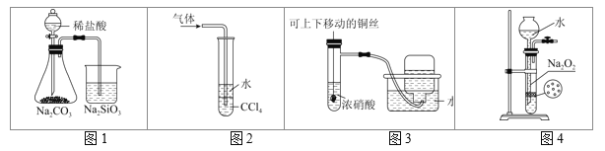
A.用图1所示装置证明非金属性强弱:
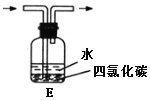
B.用图2所示装置吸收氨气,并防止倒吸
C.用图3所示装置制备并收集少量
气体
D.用图4所示装置制备少量氧气
难度: 中等查看答案及解析
-
下列物质的分类合理的是
A.强电解质:BaSO4、乙醇、CO2、Fe
B.碱:烧碱、纯碱、苛性钾、氢氧化钡
C.混合物:盐酸、漂白粉、水煤气、氢氧化铁胶体
D.碱性氧化物:
、CaO、MgO、
难度: 中等查看答案及解析
-
下列各组离子一定能大量共存的是
A.在含大量
的溶液中:
、
、
、
B.在无色透明溶液中:
、
、
、
C.在强碱性溶液中:
、
、
、
D.常温下,c(H+)/c(OH-)=1×1010的溶液中:K+、Na+、
、NO3-
难度: 中等查看答案及解析
-
某些化学问题可用相似的示意图来表示。下列说法不正确的是
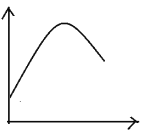
选项
横坐标
纵坐标
研究对象
A
反应时间
溶液温度
足量镁条放在
溶液中
B
反应温度
反应速率
酶催化反应
C
盐酸体积
沉淀质量
盐酸滴加到同浓度
溶液中
D
反应过程
能量
和
反应
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
阿伏加德罗常数的值为
。下列说法正确的是
A. 1L0.1mol·
NH4Cl溶液中,
的数量为0.1
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2
难度: 困难查看答案及解析
-
中国女药学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔医学奖,有关青蒿素的结构如图所示,下列关于靑蒿素的推断,不合理的是( )
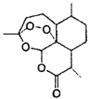
A.青蒿素的分子式是
B.青蒿素所有碳原子均在同一平面上
C.青蒿素在碱性条件下不能稳定存在
D.青蒿素可以发生氧化反应
难度: 中等查看答案及解析
-
下列说法正确的是
A.核外电子排布相同的微粒化学性质相同
B.将FeCl3溶液加热蒸干,可以制备无水FeCl3
C.浓硝酸保存在棕色玻璃试剂瓶中
D.甲烷中混有乙烯,用高锰酸钾溶液除杂,可以得到纯净的甲烷
难度: 中等查看答案及解析
-
NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法正确的是
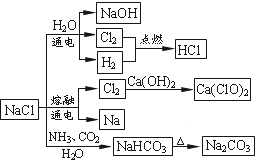
A.石灰乳与
的反应中,
既是氧化剂又是还原剂
B.电解饱和食盐水的阳极产物是H2
C.图示转化反应都是氧化还原反应
D.
与过量的铁反应生成
难度: 困难查看答案及解析
-
下列指定反应的离子方程式正确的是
A.钠与水反应:
B.向
溶液中通入足量氯气:
C.向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O
D.向碳酸氢铵溶液中加入足量石灰水:
难度: 中等查看答案及解析
-
在给定条件下,下列选项所示的物质间转化均能实现的是
A.S
SO3
H2SO4
B.NH3
NO
HNO3
C.NaHCO3(s)
Na2CO3(s)
NaOH(aq)
D.Al(s)
NaAlO2(aq)
Al(OH)3(s)
难度: 中等查看答案及解析
-
高炉炼铁过程中发生的主要反应为:1/3Fe2O3(s)+CO(g)
2/3Fe(s)+CO2(g) △H<0,欲提高上述反应CO的平衡转化率,可采取的措施是
A.移出部分
B.提高反应温度
C.加入合适的催化剂 D.减小容器的容积
难度: 中等查看答案及解析
-
一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是
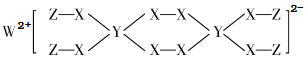
A.工业上通过电解熔融的WX来制得W
B.W、X对应的简单离子半径顺序为:W>X
C.Y的最高价氧化物对应水化物为弱酸
D.该漂白剂中各元素均满足8电子稳定结构
难度: 困难查看答案及解析
-
下列图示与对应叙述相符的是
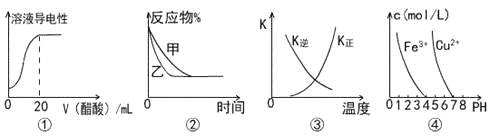
A.图①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液导电性随加入酸体积的变化
B.图②表示压强对可逆反应A(g)+2B(g)
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图③中曲线表示反应3A(g) + B(g)
2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
D.据图④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
难度: 中等查看答案及解析
-
某化工厂制备净水剂硫酸铁铵晶体
的一种方案如下:
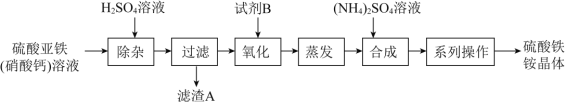
下列说法不正确的是
A.滤渣A的主要成分是
B.“合成”反应要控制温,温度过高,产率会降低
C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等
D.相同条件下,
净水能力比
强
难度: 中等查看答案及解析
-
一定温度时,向
恒容密闭容器中充入
和
,发生反应:
经过一段时间后达到平衡,反应过程中测定的部分数据见下表:
0
2
4
6
8
0
下列说法正确的是
A.反应在前2s的平均速率
B.保持其他条件不变,体积压缩到
,平衡常数将增大
C.相同温度下,起始时向容器中充入
,达到平衡时,
的转化率等于
D.保持温度不变,向该容器中再充入
、
,反应达到新平衡时
增大
难度: 困难查看答案及解析
-
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为2K2S2+KI3
K2S4+3KI;装置(Ⅱ)为电解池的示意图,当闭合开关K时,X附近溶液先变红。则下列说法正确的是
( )
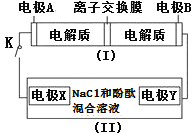
A.闭合K时,K+从左到右通过离子交换膜
B.闭合K时,电极X是阳极
C.闭合K时,电极A的反应式为3I--2e-=I3-
D.闭合K时,当有0.1molK+通过离子交换膜,X电极上产生气体2.24L
难度: 中等查看答案及解析
-
时,
的
,
,室温下向10mL
溶液中逐滴加入
溶液,如图是溶液中含碳元素微粒物质的量分数随pH降低而变化的图象
因有逸出未画出
。下列说法错误的是
A.
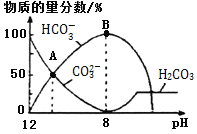
A点所示溶液的
B.B点所示溶液:
C.A点
点发生反应的离子方程式为
D.Na2CO3溶液中,c(Na+)+c(H+)=2C(CO32-)+c(
)+c(OH-)
难度: 困难查看答案及解析
-
将Mg和Cu的合金1.52 g投入稀HNO3中反应,固体全部溶解时,收集的还原产物为NO,体积为0.448L(标准状况下),向反应后的溶液中加入适量NaOH溶液,使金属离子恰好完全沉淀,则形成沉淀的质量为
A.2.15 g B.2.54 g C.4.17 g D.5.26 g
难度: 困难查看答案及解析
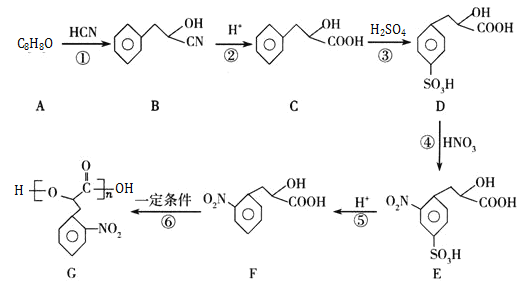
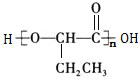 的合成路线______。
的合成路线______。