-
下列说法错误的是
A.酒越陈越香与酯化反应有关 B.细铁粉可作食品抗氧化剂
C.双氧水可作消毒剂 D.熟石灰可作食品干燥剂
难度: 简单查看答案及解析
-
可把苯酚、硫氰化钾、乙醛、氢氧化钠、硝酸银等五种溶液鉴别出来的一种试剂是
A.溴水 B.酚酞溶液 C.银氨溶液 D.FeCl3溶液
难度: 中等查看答案及解析
-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
难度: 简单查看答案及解析
-
下列有关化学反应速率的说法中,不正确的是
A.实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快
B.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大
C.可用单位时间内氢离子物质的量浓度的变化来表示NaOH和H2SO4反应的速率
D.实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快
难度: 中等查看答案及解析
-
能够跟1mol
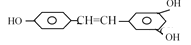 起反应的Br2或H2的最大用量分别是
起反应的Br2或H2的最大用量分别是A.1mol,1mol B.3.5mol,7mol
C.1mol,7mol D.6mol,7mol
难度: 中等查看答案及解析
-
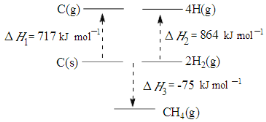
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l);ΔH1
2 H2(g)+ O2(g)= 2H2O(g);ΔH2
C(s)+ O2(g)=CO2(g);ΔH3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的ΔH为
A.12ΔH3+5ΔH2-2ΔH1 B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1 D.ΔH1-5ΔH2-12ΔH3
难度: 中等查看答案及解析
-
油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热△H为
A.3.8×104kJ·mol-1 B.-3.8×104kJ·mol-1
C.3.4×104kJ·mol-1 D.-3.4×104kJ·mol-1
难度: 简单查看答案及解析
-
把0.6 mol X气体和0.4 mol Y气体混合于2 L容器中,使它们发生如下反应:3X(g)+Y(g)
nZ(g)+2W(g),在5 min时已经生成0.2 mol W,若测知以Z的浓度变化表示平均反应速率为0.01 mol·L-1·min-1,则上述反应中Z气体的化学计量数n的值是( )
A.1 B.2 C.3 D.4
难度: 中等查看答案及解析
-
已知热化学方程式2H2(g)+O2(g)=2H2O(g) ΔH,下列有关ΔH的说法正确的是
A.与化学方程式的书写形式无关
B.与H-H键、O=O键、H-O键的键能有关
C.与是否使用催化剂有关
D.与物质的状态无关
难度: 中等查看答案及解析
-
已知反应CO(g)+H2O(g)
CO2(g)+H2(g) △H<0,在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是( )
A.升高温度,n(CO)减少 B.减小压强,n(CO2)增加
C.更换高效催化剂,CO的转化率增大 D.充入一定量的氮气,n(H2)不变
难度: 中等查看答案及解析
-
下列各组化合物中不互为同分异构体的是( )
A.
 B.
B. 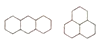
C.
 D.
D. 
难度: 简单查看答案及解析