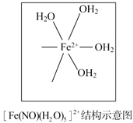
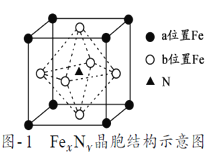
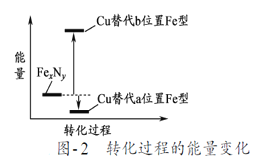
-
下列表示式错误的是( )
A. Na+的轨道表示式:

B. Na+的结构示意图:
C. Ge的电子排布式:[Ar]3d104s24p2
D. Cu+的价电子排布式:3d10
难度: 中等查看答案及解析
-
同周期的三种元素X、Y、Z,已知其最高价氧化物对应水化物的酸性强弱为HXO4>H2YO4>H3ZO4,则下列判断错误的是( )
A. 原子半径:Z>Y>X B. 气态氢化物的稳定性HX>H2Y>ZH3
C. 电负性:X>Y>Z D. 第一电离能:X>Y>Z
难度: 中等查看答案及解析
-
下列为各组指定的元素原子的价电子排布式,能形成AB2型离子化合物的是( )
A. 2s22p2和2s22p4 B. 3s23p4和2s22p4
C. 3s2和2s22p5 D. 3s1和3s23p4
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 含有极性键的分子一定是极性分子
B. H2O和CH4中心原子的杂化类型相同,键角前者大于后者
C. 最外层电子数为8的微粒都是稀有气体原子
D. 若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化,在变化各阶段被破坏的粒子间的主要相互作用依次是氢键、氢键和分子间作用力、极性键
难度: 中等查看答案及解析
-
在单质的晶体中,一定不存在( )
A. 离子键 B. 分子间作用力
C. 共价键 D. 金属离子与自由电子间的作用
难度: 简单查看答案及解析
-
下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )
A. 氯化钠与蔗糖熔化 B. 碘和干冰升华
C. 镁和硫熔化 D. 金刚石与氧化钠熔化
难度: 中等查看答案及解析
-
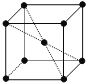
F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑,下列推测正确的是( )
A. XeF2分子中各原子均达到八电子结构
B. 某种氟化氙的晶体结构单元如图,可推知其化学式为XeF6
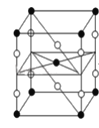
C. XeF4按已知方程式水解,每生成4molXe,转移16mol电子
D. XeF2加入水中,在水分子作用下将重新生成Xe和F2
难度: 困难查看答案及解析
-
下列说法不正确的是( )
A. 60克SiO2晶体中,含有4 NA个硅氧键
B. 12克金刚石中,含有2 NA个碳碳键
C. 12克石墨中,含有1.5 NA个碳碳键
D. 31克白磷中,含有6 NA个磷磷键
难度: 困难查看答案及解析
-
a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。下列叙述错误的是( )
A. d元素的基态原子的核外电子的运动状态有17种
B. 它们均存在两种或两种以上的氧化物
C. b与c或d形成的化合物都是良好的有机溶剂
D. b、c、d与氢形成的化合物中化学键均为极性共价键
难度: 中等查看答案及解析
-
金属钠晶体为体心立方晶胞,实验测得钠的密度为ρ(g·cm-3)。已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性小球且处于体对角线上的三个球相切。则钠原子的半径r(cm)为( )
A.
B.
C.
D.
难度: 困难查看答案及解析
-
下列叙述正确的是( )
A. 在光照条件下,将乙烷与氯气混合最多可得8种有机产物
B. 乙烷、丙烷和丁烷都没有同分异构体
C. 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色
D. 苯酚有毒,沾到皮肤上,可用酒精洗涤
难度: 中等查看答案及解析
-
下列关于有机化合物的说法正确的是( )
A. 除去乙醇中的少量水,方法是加入新制生石灰,经过滤后即得乙醇
B. 裂化汽油可用于萃取溴水中的溴
C. 三联苯的一氯代物有4种
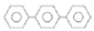
D. 室温下,在水中的溶解度:苯酚>丙三醇>1—氯丁烷
难度: 中等查看答案及解析
-
下列说法全部正确的是( )
①环丙烷和乙烯的最简式相同②相同质量的乙炔和苯充分燃烧耗氧量相同
③苯乙烯和丁烯互为同系物④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2 L的己烷所含的分子数为0.5NA(NA为阿伏加德罗常数的值)
⑥
分子中所有原子一定都在同一平面上
A. ①②③ B. ②④⑤⑥
C. ①②④ D. ①②④⑥
难度: 中等查看答案及解析
-
将体积为10 mL两种气态烃与过量的氧气混合后充分燃烧,将生成物先通过浓H2SO4体积减小15 mL,再通过碱石灰气体体积又减小20 mL(气体体积均为同温同压下)。则混合烃的组成可能为( )
A. C2H4和C2H2 B. C2H6和C2H4
C. CH4和C3H4 D. C4H10和C2H4
难度: 困难查看答案及解析
-
下列有机物的同分异构体数目判断错误的是( )
选项
有机物
同分异构体数目
A
分子式为C5H12
3
B
分子式为C4H8,不能使溴的四氯化碳溶液退色
2
C
分子式为C4H10O,能与Na反应生成氢气
4
D
分子式为C3H8的二氯代物
3
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
4-溴环己烯主要用于有机合成,它可发生如图所示的转化,下列叙述错误的是( )

A. 反应①为氧化反应,产物含有溴原子和羧基两种官能团
B. 反应②为取代反应,产物含有羟基和碳碳双键两种官能团
C. 反应③为消去反应,产物含碳碳双键和溴原子两种官能团
D. 反应④为加成反应,产物只含溴原子一种官能团
难度: 中等查看答案及解析