-
2019 年世界环境日将聚焦“空气污染”主题,我市在环境保护上取得显著成就。下列做法符合这一主题是
A.直接焚烧废弃塑料 B.餐饮油烟直接排放空气中
C.大量燃放烟花爆竹 D.使用清洁能源的公共汽车
难度: 简单查看答案及解析
-
以下实验,仅发生物理变化的是
A.
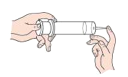 压缩空气 B.
压缩空气 B.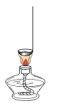 加热砂糖
加热砂糖C.
 铁的锈蚀 D.
铁的锈蚀 D.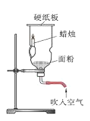 粉尘爆炸
粉尘爆炸难度: 中等查看答案及解析
-
战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即指牡蛎壳之类的贝壳),并把这种灰称为“蜃”。在东汉蔡伦改进造纸术中,用“蜃”溶于水制得的碱液将树皮脱胶。“蜃”的主要成分是
A.氯化钠 B.氢氧化钙 C.碳酸钙 D.氧化钙
难度: 中等查看答案及解析
-
下列物质的性质和用途,对应关系正确的是
A
B
C
D
物质
碳酸氢铵
酒精
氧气
盐酸
性质
受热易分解
可燃性
助燃性
与金属氧化物反应
用途
作氮肥
消毒剂
焊接和切割金属
实验室制取少量氢气
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
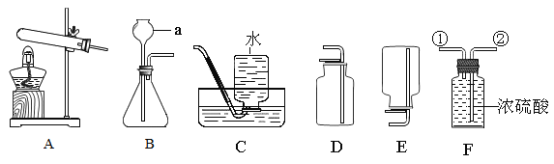
下列实验操作正确的是
A.
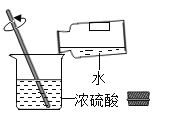 稀释浓硫酸 B.
稀释浓硫酸 B.检查装置气密性
C.
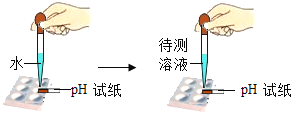 测定溶液 pH D.
测定溶液 pH D.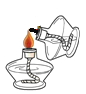 引燃酒精灯
引燃酒精灯难度: 简单查看答案及解析
-
古代的“打火机”——“火折子”是用草纸卷成密集的纸卷,用火点燃,再将其吹灭放入竹筒中,需要的时候取出轻轻吹一下即可生火。以下关于“火折子”制作及使用的说法错误的是
A.制作“纸卷”的草纸是可燃物
B.准备放入竹筒中的“火折子”要留些火星
C.纸卷放入竹筒后,盖子不能将竹筒完全密封
D.“火折子”吹了会燃烧是因为降低“纸卷”的着火点
难度: 中等查看答案及解析
-
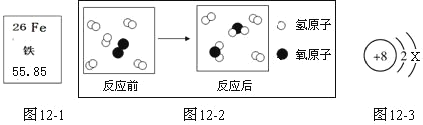
氮化碳(C3N4,其中 C 为+4 价)硬度超过金刚石,成为首屈一指的超硬新材料。下列有关 C3N4 的说法正确的是
A.氮化碳属于非金属氧化物
B.氮化碳中氮元素化合价是-3
C.氮化碳中 C、N 元素质量比为 3∶4
D.氮化碳由 3 个碳原子和 4 个氮原子构成
难度: 中等查看答案及解析
-
下列化学观念错误的是
A.转化观:二氧化碳和一氧化碳在一定条件下可相互转化
B.微粒观:二氧化碳是由碳原子和氧分子构成的
C.结构观:水和过氧化氢化学性质不同是因为它们分子的构成不同。
D.分类观:氧气、氮气、氢气均属于非金属单质
难度: 中等查看答案及解析
-
下列鉴别物质的方案不能达到实验目的是
选项
需鉴别的物质
主要实验操作
A
硬水和蒸馏水
滴加肥皂水观察现象
B
棉纱线和羊毛线
点燃并闻气味
C
稀盐酸和稀硫酸
滴加石蕊试液观察现象
D
固体 NaOH、NH4NO3、NaCl
加水溶解测温度
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
向碳酸钠溶液中滴加盐酸,利用 pH 传感器测得溶液 pH 与消耗盐酸体积的变化关系如图所示。已知该反应过程分为两个阶段:
①Na2CO3 +HCl = NaHCO3+ NaCl;
②NaHCO3 +HCl = NaCl + H2O + CO2↑,AB 段主要进行①反应,CD 段主要进行②反应。下列说法不合理的是
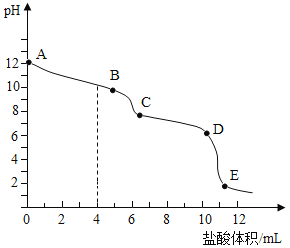
A.加入盐酸体积为 4mL 时有大量气泡产生
B.Na2CO3 溶液比 NaHCO3 溶液的碱性更强
C.D 点处反应基本结束
D.E 点溶液的溶质有氯化钠和氯化氢
难度: 困难查看答案及解析