-
下列关于有机物因果关系的叙述中,完全正确的一组是( )
选项
原因
结论
A
乙烯和苯都能使溴水退色
苯分子和乙烯分子含有相同的碳碳双键
B
乙酸分子中含有羧基
可与NaHCO3溶液反应生成CO2
C
纤维素和淀粉的分子式均为(C6H10O5)n
它们属于同分异构体
D
乙酸乙酯和乙烯在一定条件下都能与水反应
两个反应属于同一类型反应
A. A B. B C. C D. D
难度: 中等查看答案及解析
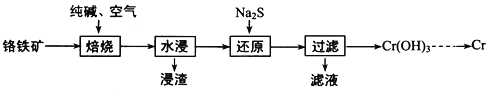
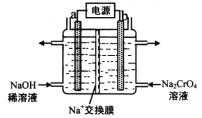
-
雌黄(As2S3)在我国古代常用作书写涂改修正胶。浓硝酸氧化雌黄可制得硫黄,并生成砷酸和一种红棕色气体,利用此反应原理设计为某原电池。下列有关叙述正确的是
A. 砷酸的分子式为H2AsO4
B. 红棕色气体在该原电池的负极区生成并逸出
C. 该反应的氧化剂和还原剂物质的量之比为12:1
D. 该反应中每析出4.8g硫黄,则转移0.5mol电子
难度: 中等查看答案及解析
-
根据下列实验操作和现象所得出的结论正确的是( )
选项
实验操作和现象
结论
A
向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀
X具有强氧化性
B
将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生
非金属性:Cl>Si
C
常温下,分别测定浓度均为0.1 mol·L-1 NaF和NaClO溶液的pH,后者的pH大
酸性:HF<HClO
D
卤代烃Y与NaOH水溶液共热后,加入足量稀硝酸,再滴入AgNO3溶液,产生白色沉淀
Y中含有氯原子
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关文献的理解错误的是( )
A. “所在山洋,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”过程包括了溶解、蒸发、结晶等操作。
B. 《物理小识》记载“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不没,”“气”凝即得“矾油”。青矾厂气是NO和NO2。
C. 《开宝本草》中记载了中药材铁华粉的制作方法:“取钢煅作时如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”中药材铁华粉是醋酸亚铁。
D. 唐代《真元妙道要略》中有云“以硫磺、雄黄合销石并蜜烧之,焰起烧手、面及屋舍者”,描述了黑火药制作过程。
难度: 简单查看答案及解析
-
[安徽省蚌埠市2019届高三第一次质量监测]下列有关化学用语表示正确的是
A.水分子的比例模型
B.过氧化氢的电子式为:
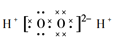
C.石油的分馏和煤的气化、液化均为物理变化
D.甲基环丁烷二氯代物的同分异构体的数目是10种(不考虑立体异构)
难度: 中等查看答案及解析
-
已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L−1磷酸钠溶液含有的
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
难度: 中等查看答案及解析
-
用“银-Ferrozine”法测室内甲醛含量的原理为:
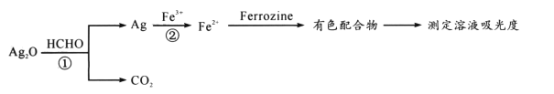
已知:吸光度与溶液中有色物质的浓度成正比。下列说法正确的是
A.反应①中参与反应的HCHO为30g时转移电子2mol
B.可用双氧水检验反应②后的溶液中是否存在Fe3+
C.生成44.8 LCO2时反应②中参加反应的Ag一定为8mol
D.理论上测得溶液吸光度越高,HCHO含量也越高
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18g氨基(-ND2)中含有的电子数为10NA
B. 向NH4Al(SO4)2稀溶液中逐滴加入过量Ba(OH)2溶液,发生反应的离子方程式为:NH4++Al3++2SO42-+2Ba2++5OH-=
2BaSO4↓+AlO2-+2H2O+NH3·H2O
C. 麦芽糖溶液中:SO42-、MnO4-、K+、H+可以大量共存
D. 标准状况下,2.24LCl2通入足量NaOH溶液反应转移的电子数为0.2NA
难度: 中等查看答案及解析
-
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下,下列说法错误的是
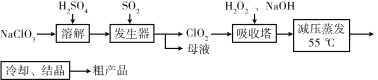
A. NaClO3在发生器中作氧化剂
B. 吸收塔中1mol H2O2得到2mol电子
C. 吸收塔中温度不宜过高,会导致H2O2的分解
D. 从“母液”中可回收的主要物质是Na2SO4
难度: 中等查看答案及解析
-
BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法不正确的是
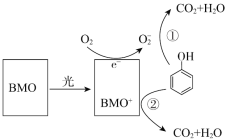
A.该过程的总反应:C6H6O+7O2
6CO2+3H2O
B.该过程中BMO表现较强氧化性
C.降解产物的分子中只含有极性共价键
D.①和②中被降解的苯酚的物质的量之比为3:1
难度: 中等查看答案及解析
-
主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Y、Z的族序数之和为12;X与Y的电子层数相同;向过量的ZWY溶液中滴入少量硫酸铜溶液,观察到既有黑色沉淀生成又有臭鸡蛋气味的气体放出。下列说法正确的是
A. 原子半径由大到小的顺序为:r(Z)>r(Y)>r(X)>r(W)
B. 氧化物的水化物的酸性:H2XO3<H2YO3
C. ZWY是离子化合物,其水溶液中只存在电离平衡
D. 单质熔点:X<Y
难度: 困难查看答案及解析
-
工业制氢气的一个重要反应是:CO(g)+H2O(g)=CO2(g)+H2(g)。
已知在25℃时:①C(s)+
O2(g)
CO(g) ∆H4=-111kJ/mol
②H2(g)+
O2(g)=H2(g) ∆H2=-242kJ/mol
③C(s)+O2(g)=CO2(g) ∆H2=-394kJ/mol
下列说法不正确的是( )
A.25℃时,
B.增大压强,反应①的平衡向逆反应方向移,平衡常数K减小
C.反应①达到平衡时,每生成
的同时生成0.5molO2
D.反应②断开2molH2和1molO2中的化学键所吸收的能量比形成4molO-H键所放出的能量少484kJ
难度: 中等查看答案及解析
-
2019年诺贝尔化学奖花落锂离子电池,美英日三名科学家获奖,他们创造了一个可充电的世界。像高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。
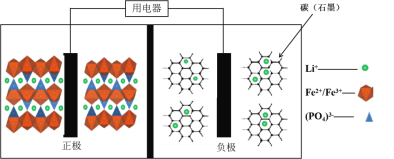
原理如下:(1−x)LiFePO4+xFePO4+LixCn
LiFePO4+nC。下列说法不正确的是( )
A.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn
D.充电时,Li+向左移动
难度: 困难查看答案及解析
-
某温度下,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
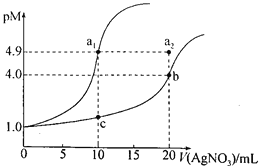
A.该温度下,Ksp(Ag2CrO4)=4×10-12
B.al、b、c三点所示溶液中c(Ag+):al>b>c
C.若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点
D.用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂
难度: 困难查看答案及解析
-
下列物质在给定条件下的同分异构体数目正确的是( )
A.C4H10属于烷烃的同分异构体有3种
B.分子组成是C5H10O2属于羧酸的同分异构体有5种
C.分子组成是C4H8O属于醛的同分异构体有3种
D.
的一溴代物有5种
难度: 困难查看答案及解析
-
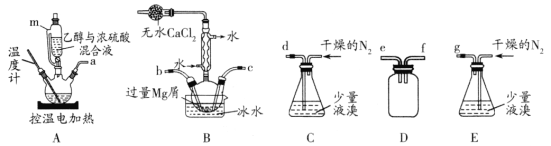
工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯(柠檬烯
)。提取柠檬烯的实验操作步骤如下:
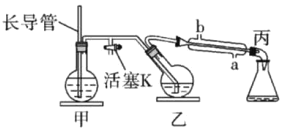
①将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30mL水;
②松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是
A.当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B.蒸馏结束后,先把乙中的导气管从溶液中移出,再停止加热
C.为完成实验目的,应将甲中的长导管换成温度计
D.要得到纯精油,还需要用到以下分离提纯方法:分液、蒸馏
难度: 中等查看答案及解析
-
下列关于有机物1-氧杂-2,4-环戊二烯(
)的说法正确的是
A. 与
互为同系物 B. 二氯代物有3种
C. 所有原子都处于同一平面内 D. 1mol该有机物完全燃烧消耗5molO2
难度: 困难查看答案及解析
-
下列各选项有机物同分异构体的数目,与分子式为ClC4H7O2,且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)( )
A.分子式为C5H10的烯烃 B.分子式为C4H8O2的酯
C.
的一溴代物 D.立方烷(
)的二氯代物
难度: 中等查看答案及解析
-
在
分子中,处于同一平面上的碳原子数最多可能有
A.6个 B.8个 C.10个 D.12个
难度: 简单查看答案及解析
-
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
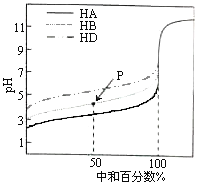
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
难度: 中等查看答案及解析
-
交联聚合物P的结构片段如图所示。下列说法不正确的是(图中
表示链延长)
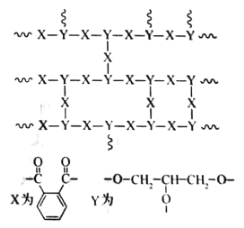
A. 聚合物P中有酯基,能水解
B. 聚合物P的合成反应为缩聚反应
C. 聚合物P的原料之一丙三醇可由油脂水解获得
D. 邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构
难度: 简单查看答案及解析
-
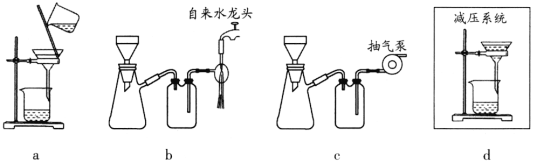
实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
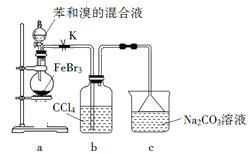
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
难度: 中等查看答案及解析
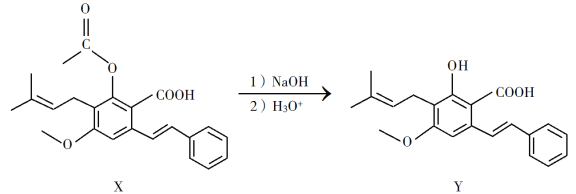

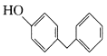 )是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。
)是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。