-
硫酸钾、硫酸铝和硫酸组成的混合溶液c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8 mol·L-1,则c(K+)为( )
A.0.15 mol·L-1 B.0.2 mol·L-1 C.0.3 mol·L-1 D.0.4 mol·L-1
难度: 简单查看答案及解析
-
常用仪器的使用及注意事项正确的是
A.给试管中的固体加热,应先预热,后局部加热
B.量筒、容量瓶、锥形瓶都是能加热的玻璃仪器
C.灼烧固体时,坩埚放在铁圈或三脚架上直接加热
D.在蒸馏过程中,若发现忘加沸石,应立即补加
难度: 简单查看答案及解析
-
下列说法不正确的是
A.蒸馏时温度计水银球可以高于蒸馏烧瓶支管口
B.计量仪器的读数:精确度①托盘天平:0.1 g;②量筒:0.1 mL
C.过滤所需的主要仪器有铁架台(附铁圈)、烧杯、漏斗、玻璃棒
D.蒸发所需的主要仪器有铁架台(附铁圈)、酒精灯、蒸发皿、玻璃棒
难度: 简单查看答案及解析
-
关于物质的类别,下列说法正确的是
A.食盐水、糖水和冰水都是饮料,属于混合物
B.O2不能导电,故O2是非电解质
C.SO2属于氧化物、 HCl属于强酸
D.NaHSO4能电离出氢离子,故NaHSO4属于酸
难度: 简单查看答案及解析
-
下列说法正确的是
A.胶体粒子不能透过滤纸
B.按照分散质和分散剂的状态,分散系可分为9种
C.向豆浆中加入盐卤或石膏做豆腐 与胶体性质无关
D.溶液是电中性的,胶体是带电的
难度: 简单查看答案及解析
-
下列说法正确的是
A.阿伏加德罗常数(NA)与6.02×1023是完全相同的
B.摩尔是化学上常用的一个物理量
C.当1 mol气体的体积是22.4 L时,一定是标准状况
D.氖气的摩尔质量(单位g·mol-1)在数值上等于它的相对原子质量
难度: 简单查看答案及解析
-
关于某混合物的说法正确的是( )
A. 物质的组成元素一定是两种或两种以上 B. 构成物质一定是化合物
C. 构成物质一定是单质 D. 构成物质可能只有一种元素
难度: 中等查看答案及解析
-
按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氧化物 ③含氧酸 ④一元酸 ⑤电解质 ⑥混合物 ⑦无机化合物
A.①③④⑤⑦ B.①②③④⑤⑦
C.①②③④⑥ D.①④⑥⑦
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
B.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,生成H2的体积为112mL
C.常温常压下,3.2 g O2所含的原子数为0.2NA
D.标准状况下,2.24 LH2O含有的H2O分子数为0.1NA
难度: 简单查看答案及解析
-
下列说法正确的是
A.1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl
B.用100 mL水吸收0.1 mol HCl气体所得溶液的物质的量浓度恰好是1 mol·L-1
C.将62 g Na2O溶于水中,配成1 L溶液,所得溶质的物质的量浓度为2 mol·L-1
D.1 L水中溶解5.85 g NaCl所形成的溶液的物质的量浓度是0.1 mol·L-1
难度: 简单查看答案及解析
-
能正确表示下列反应的离子方程式的是
A.澄清石灰水检验CO2:CO2+2OH-+Ca2+===CaCO3↓+H2O
B.用醋酸NaOH溶液反应:H++OH-===H2O
C.向NaHCO3溶液中滴加盐酸:CO32-+2H+===H2O+CO2↑
D.锌片插入硝酸银溶液中:Zn+Ag+===Zn2++Ag
难度: 简单查看答案及解析
-
下列各组离子中的离子,能在溶液中大量共存的是
A.Na+、Mg2+、Cl-、OH-
B.H+、Ca2+、CO32-、NO3-
C.Cu2+、K+、SO42-、NO3-
D.Na+、HCO3- 、OH-、Ca2+
难度: 简单查看答案及解析
-
下列说法不正确的是
A.元素在自然界中的存在形式有原子、分子或离子。
B.在化学变化中,分子可以再分,离子和原子不可以再分。
C.同一种原子可能形成不同的离子。
D.原子与该原子形成的离子相对原子质量几乎相等。
难度: 简单查看答案及解析
-
在体积相同的两个密闭容器中分别充满O2、O3气体,当两个容器内温度和气体密度相等时,说法正确的是 ( )
A.两种气体的压强相等 B.O2比O3质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
难度: 简单查看答案及解析
-
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
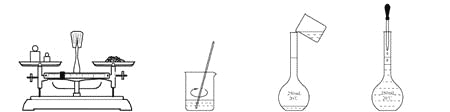
A. 称量 B. 溶解 C. 转移 D. 定容
难度: 中等查看答案及解析