-
I.写出下列典型物质的电离方程式
(1)H2SO4_________________________________________
(2)Fe(OH)3________________________________________
(3)NaHSO4_________________________________________
(4)NaHCO3________________________________________
(5)Al2O3(熔融)____________________________________
II.写出下列典型反应的离子方程式:
(1)在稀H2SO4中加入CH3COONa溶液___________________________________
(2)氧化镁溶于稀硫酸______________________________________________
(3)CuSO4溶液与Ba(OH)2溶液混合_______________________________________
(4)NaHCO3溶液与稀盐酸混合________________________________________
(5)NaHSO4溶液与NaOH溶液混合_____________________________________
高一化学填空题简单题查看答案及解析
-
I.写出下列物质溶于水的电离方程式:
(1)HCl: ,(2)Ba(OH)2: ,
(3)NaHCO3: ,(4)NaHSO4: 。
Ⅱ.试用质子数、中子数、电子数、质量数和同位素填空:
(1)
C与
N具有相同的 (2)
C与
C具有相同的
(3)
C与
N具有相同的 (4)
N与
N互为
Ⅲ.用“相等”或“不相等”填空:
0.3 mol的氧气和0.2 mol的臭氧(O3),它们的质量 ,它们所含的分子数 ,原子数 。
高一化学填空题中等难度题查看答案及解析
-
(12分)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:
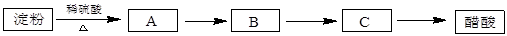
B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
(1)写出化学方程式,并注明反应类型:
I、淀粉水【解析】
________,________反应。II、B与醋酸反应:________,________反应。
Ⅲ、B→C:________,________反应。
(2) 可用于检验淀粉水解是否产生A的试剂是 ________ 。]
检验所酿的陈醋中是否含有淀粉的方法是________。
高一化学填空题简单题查看答案及解析
-
写出下列物质在水溶液中的电离方程式:H2SO4________AlCl3________.
高一化学填空题中等难度题查看答案及解析
-
I.已知常温下,H2SO3的电离常数Ka1=1.54×10-2,Ka2=1.02×10-7;H2CO3的电离常数Ka1=4.30×10-7,Ka2=5.60×10-11。
(1)下列微粒可以大量共存的是___________(填选项字母)。
a. CO32-、HSO3- b. HCO3-、HSO3-
c. SO32-、 HCO3- d. H2SO3、HCO3-
(2)已知NaHSO3溶液显酸性,NaHSO3的稀溶液中各离子浓度从大到小的排列顺序是________________________________。
(3)浓度均为0.1 mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为_____________________。
(4)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_________________________________。
Ⅱ. Na2S2O5(焦亚硫酸钠)是常见的食品抗氧化剂之一。
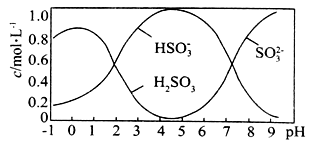
(5)将0. 5 mol Na2S2O5溶于水配成1 L溶液,该溶液的pH==4.5。溶液中部分微粒浓度随溶液酸碱性的变化情况如图所示。当溶液pH小于1后,溶液中H2SO3的浓度变小,其原因可能是___________________________________________________________。
(6)已知:Ksp (BaSO4)=1.0×10-10,Ksp (BaSO3)=5.0×10-7。将部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c (SO42-)≤1.0×10-5 mol•L-1],此时溶液中c (SO32-)≤_____________mol•L-1
高一化学简答题困难题查看答案及解析
-
I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
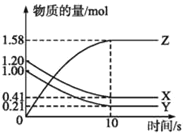
(1)写出该反应的化学方程式___________________
(2)下列叙述中不能说明上述反应达到平衡状态的是___________.
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(3)为使该反应的反应速率减小,可采取的措施是_____.
A 恒压时充入Ne B 适当升高温度
C 缩小容器的体积 D 选择高效催化剂.
II.一定温度下将3mol的A及3molB混合于2L的密闭
容器中,发生如下反应:3A(g)+B(g)
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60﹪,C的平均反应速率是0.18mol/(L.min)。
求:(1)平衡时B的浓度=______mol/L。
(2)D的平均反应速率υ(D)=______mol/( L.min)。
(3)x=______。
高一化学计算题中等难度题查看答案及解析
-
写出下列物质的电离方程式:
H2SO4________,
K2CO3________Ba(OH)2________。
高一化学选择题中等难度题查看答案及解析
-
写出下列物质的电离方程式:
H2SO4________;
Ba(OH)2________;
Fe2(SO4)3________.
高一化学填空题简单题查看答案及解析
-
写出下列物质的电离方程式:
H2SO4______Ca(OH)2______
K3PO4______Fe2(SO4)3______.高一化学解答题中等难度题查看答案及解析
-
写出下列物质在水溶液中的电离方程式:
H2SO4______Ba(OH)2______AlCl3______Fe2(SO4)3______.高一化学解答题中等难度题查看答案及解析