-
无机化学命名委员会在1989年作出决定:把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列。按这个规定,下列说法正确的是( )
A. 第3列元素种类最多,第14列的化合物种类最多
B. 每一列只有金属元素
C. 从上到下第1列元素的单质熔点逐渐降低,而第17列元素的单质熔点逐渐升高
D. 只有第2列元素的原子最外层有2个电子
难度: 中等查看答案及解析
-
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H218O与D216O的相对分子质量相同
难度: 中等查看答案及解析
-
最近医学界通过用放射性14C标记的C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病病毒(AIDS)。则有关14C的下列说法中正确的是
A.14C与12C、13C互为同位素 B.14C与C60互为同素异形体
C.14C原子与14N原子中所含中子数相同 D.14C原子与12C原子化学性质不同
难度: 中等查看答案及解析
-
下列表示物质结构的化学用语正确的是( )
A.H、D、T表示同一种核素
B. MgCl2的形成过程
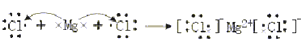
C.Cl-离子的结构示意图:
D.NH4Cl的电子式:
难度: 中等查看答案及解析
-
含有下列键型的物质,可能为单质的是
A.只有离子键的物质 B.既有离子键,又有非极性键的物质
C.既有极性键,又有离子键的物质 D.只有非极性键的物质
难度: 简单查看答案及解析
-
下列物质中,既含有非极性共价键又含有离子键的物质是
A.CO2 B.H2O C.Na2O2 D.Cl2
难度: 简单查看答案及解析
-
关于元素周期表,下列叙述中正确的是 ( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B. 在主族元素中可以寻找制备催化剂及耐高温和耐腐蚀材料的元素
C. 在过渡元素区域可以寻找制备新型农药材料的元素
D. 非金属性最强的元素在元素周期表的最右上角
难度: 简单查看答案及解析
-
部分卤族元素的某种性质A随核电荷数的变化趋势如图所示,则A可能表示
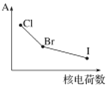
A.原子半径 B.氢化物的稳定性
C.原子的电子层数 D.单质的密度
难度: 简单查看答案及解析
-
下列事实不能作为实验判断依据的是
A.钠和镁分别与冷水反应,判断金属性强弱
B.铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中,不能置换出铜,判断钠与铁的金属性强弱
C.酸性:H2CO3<H2SO4,判断硫与碳的非金属性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱
难度: 中等查看答案及解析
-
X元素最高价氧化物对应的水化物为HXO3,它的气态氢化物为( )
A. HX B. H2X C. XH3 D. XH4
难度: 简单查看答案及解析
-
已知X、Y、Z、W原子序数都不超过18,它们的离子aX (n+1)+、bY n+、cZ (n+1)-、dW n-具有相同的电子层结构,则下列说法正确的是
A.原子序数:a>b>c>d B.离子半径:X (n+1)+>Y n+>Z (n+1)->W n-
C.单质还原性:X <Y D.单质氧化性:Z>W
难度: 中等查看答案及解析
-
硒(Se)是第4周期ⅥA族元素,下列叙述不正确的是( )
A.硒的氢化物为H2Se B.硒可以形成SeO2和SeO3
C.硒是一种金属性很强的元素 D.硒的最高价氧化物对应水化物的是H2SeO4
难度: 简单查看答案及解析
-
CN-为拟卤素离子,(CN)2性质和卤素类似。下列叙述错误的是( )
A. (CN)2可以和H2反应 B. (CN)2不能和碱反应
C. CN-具有还原性 D. (CN)2的性质活泼
难度: 简单查看答案及解析
-
关于化学键的下列叙述中,正确的是( )
①化学键只存在于分子之间
②化学键是相邻原子或离子之间强烈的相互作用
③化学键是一种静电作用
④化学键是相邻分之之间强烈的相互吸引
⑤离子化合物可能含共价键
⑥共价化合物可能含离子键
⑦离子化合物只含离子键 ⑧共价化合物不含离子键
A.②③④⑦ B.②④⑤⑥ C.②③⑤⑧ D.①③⑤⑧
难度: 中等查看答案及解析
-
如图是元素周期表中短周期的一部分,若A原子最外层的电子数比次外层少3,则下列说法正确的是( )
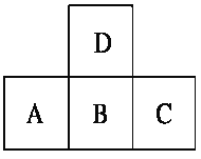
A.原子半径的大小顺序是C > B > A > D
B.B、D之间只能形成一种化合物
C.只有A的单质存在同素异形体
D.A、B、C的最高价氧化物对应水化物的酸性强弱的关系是C > B > A
难度: 中等查看答案及解析