-
水是最常见的物质,以下与水有关的说法正确的是
A.地球上水资源丰富,人类不缺淡水 B.水由2个氢原子和1个氧原子构成
C.蒸馏水是软水 D.自来水中只含有水分子,不含其它粒子
难度: 简单查看答案及解析
-
“分类”是学习化学的重要思想。下列说法正确的是
A.氯酸钾属于酸
B.硝酸钾属于复合肥料
C.氨气和过氧化氢属于氧化物
D.生理盐水和铁粉都是混合物
难度: 简单查看答案及解析
-
“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是( )
A.
 土壤加水搅拌 B.
土壤加水搅拌 B. 过滤
过滤C.
检验酸碱性 D.
 测定pH
测定pH难度: 简单查看答案及解析
-
下列说法正确的是
A.合金中一定不含有非金属元素
B.空气是由氮气、氧气两种气体组成的混合物
C.金刚石和石墨是由碳元素组成的不同的单质
D.物体的热胀冷缩是因为微粒的大小发生了改变
难度: 简单查看答案及解析
-
下列有关物质的性质与用途叙述正确是
A.酒精具有可燃性,可用作溶剂
B.碳具有可燃性,因此可用于冶炼金属
C.生石灰遇水能放出热量,所以常用作干燥剂
D.食醋具有酸性,因此可用于减轻松花蛋中所含碱性物质的涩味
难度: 简单查看答案及解析
-
A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是
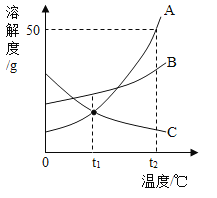
A.三种物质的溶解度:A>B>C
B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:2
C.将t2℃时,A、B两种物质的饱和溶液分别降温至t1℃,所得溶液的溶质质量分数的大小关系是B>A
D.将C的饱和溶液变为不饱和溶液,可采用升温的方法
难度: 中等查看答案及解析
-
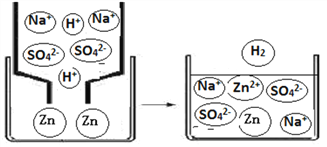
向 MgSO4和CuSO4的混合溶液中加入一定质量的铁粉,充分反应后过滤,得滤液和滤渣。向滤渣中加入稀盐酸,有气泡产生。根据上述实验得出的下列推断不正确的是
A.滤液的颜色为浅绿色 B.滤液中含Fe2+和Mg2+ C.滤渣含有铁和铜 D.滤渣的质量小于加入铁粉的质量
难度: 中等查看答案及解析
-
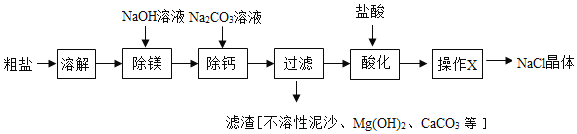
下列物质提纯所用的实验不正确的是
选项
物质(括号内为杂质)
实验方法
A
CuO(Cu)
在氧气流中充分加热
B
Fe(Al2O3)
加入足量稀硫酸,充分反应后结晶
C
H2(HCl)
通过装有NaOH 溶液的洗气瓶
D
KNO3 溶液(K2SO4)
加入适量的 Ba(NO3)2 溶液,过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列实验能达到实验目的是( )
A.
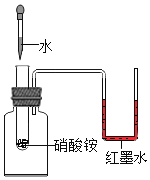 验证硝酸铵溶解吸热
验证硝酸铵溶解吸热B.
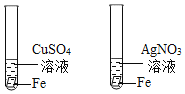 验证Fe、Cu、Ag的活动性依次减弱
验证Fe、Cu、Ag的活动性依次减弱C.
 制取并收集纯净的CO2
制取并收集纯净的CO2D.
 验证铁钉的锈蚀与氧气有关
验证铁钉的锈蚀与氧气有关难度: 中等查看答案及解析
-
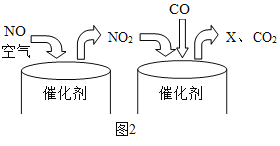
在光照条件下,AgNO3 可分解为 Ag、O2 和某种氮的氧化物 X。取一定质量的 AgNO3 固体充分光照,测得反应后生成Ag、O2、X 的质量分别为 21.6 g、m g、9.2 g。下列说法正确的是
A.AgNO3 的质量为 30.8 g
B.m = 3.6
C.X 的化学式为 NO
D.该反应方程式中 Ag 与O2 的化学计量数之比为 2∶1
难度: 困难查看答案及解析