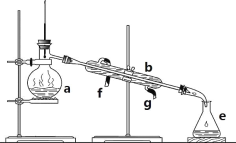
-
配制一定物质的量浓度的溶液,如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度与所要求的相比
A. 偏大 B. 偏小 C. 不变 D. 无法确定
难度: 简单查看答案及解析
-
已知① 2Fe3+ +2I- =2Fe2+ +I2 ② 2Fe2+ +Cl2 =2Fe3+ +2Cl-,则有关离子的还原性由强到弱的顺序是: ( )
A. Cl->Fe2+>I- B. Fe2+>I->Cl- C. Fe2+>Cl->I- D. I->Fe2+>Cl-
难度: 简单查看答案及解析
-
已知5KCl + KClO3 +3H2SO4==3Cl2 ↑+ 3K2SO4 + 3H2O ,下列说法不正确的是
A. H2SO4 既不是氧化剂又不是还原剂
B. 1mol KClO3 参加反应时有5mol电子转移
C. KClO3是氧化剂
D. 被氧化与被还原的氯元素的质量比为1:5
难度: 简单查看答案及解析
-
下列溶液中,Na+浓度最大的是( )
A. 1mol·L-1Na2SO4溶液100mL B. 0.9mol·L-1Na3PO4溶液10mL
C. 2.5mol·L-1NaOH溶液50mL D. 1 mol·L-1NaHCO3溶液100mL
难度: 简单查看答案及解析
-
仪器名称为“容量瓶”的是( )
A.
 B.
B.C.
D.
难度: 简单查看答案及解析
-
用NA 代表阿伏加德罗常数的值,下列说法正确的是( )
A. 阿伏伽德罗常数是6.02×1023
B. 标准状况下,11.2LCCl4所含分子数为0.5NA
C. 1.8g的NH4+中含有的电子数为NA
D. 0.1mol·L-1的MgCl2溶液中,所含Cl-的数目为0.2NA
难度: 简单查看答案及解析
-
对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。下面所列物质,贴错了包装标签的是( )
A.酒精
 B.浓硫酸
B.浓硫酸
C.汽油
 D.氯酸钾
D.氯酸钾
难度: 简单查看答案及解析
-
现有两份溶液:①将106 g Na2CO3固体溶于1 L水配成溶液,②将1 mol Na2CO3·10H2O溶于水配成1 L溶液。下列量一定相等的是( )
A. 物质的量浓度 B. 溶质的物质的量
C. 溶液的体积 D. 质量分数
难度: 简单查看答案及解析
-
关于物质分类正确的组合是( )
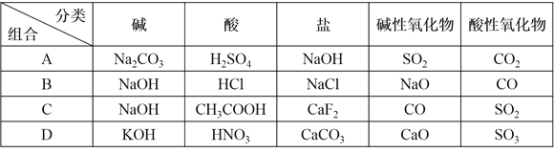
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后的正确现象是
A.溶液分层,上层紫红色 B.溶液分层,下层紫红色
C.整个溶液变为棕黄色 D.整个溶液变紫红色
难度: 简单查看答案及解析
-
下列物质中,其物质的量为0.2mol的是
A.2.2g CO2 B.4.8gMg C.4.48L O2 D.49g H2SO4
难度: 简单查看答案及解析
-
下列分散系中,能产生“丁达尔效应”的是
A.食盐水 B.豆浆 C.石灰乳 D.硫酸铜溶液
难度: 简单查看答案及解析
-
下列中和反应对应的离子方程式能以“H++OH-═H2O”表示的是
A.醋酸和氢氧化钠溶液反应 B.氢氧化镁和盐酸反应
C.澄清石灰水和硝酸反应 D.氢氧化钡和稀硫酸反应
难度: 简单查看答案及解析
-
下列叙述中正确的是( )
A. 金属元素从化合态变为游离态时,该元素一定被还原
B. 氧化还原反应的实质是电子的得失
C. 氧化还原反应中一种元素化合价升高一定有另一种元素化合价降低
D. 有单质参加或有单质生成的反应一定是氧化还原反应
难度: 简单查看答案及解析
-
下列仪器可以加热的是( )
①蒸馏烧瓶;②容量瓶;③蒸发皿;④试管;⑤表面皿;⑥分液漏斗;⑦量筒;⑧锥形瓶
A. ①③④⑧ B. ②④⑥⑧ C. ③④⑤ D. ②③④⑦
难度: 简单查看答案及解析
-
某同学欲配制含有大量下列各离子的溶液,其中能实现的是( )
A.K+ H+
OH- B.Na+ Ca2+
C.Na+ H+ Cl-
D.Na+ Cu2+ Cl-
难度: 简单查看答案及解析
-
下列变化需加入还原剂才能完成的是
A.MnO2→MnO42- B.HCO3-→CO2 C.HNO3→NO D.Br-→Br2
难度: 简单查看答案及解析
-
下列状态的物质,既能导电又属于电解质的是
A.MgCl2晶体 B.NaCl溶液 C.液态氯化氢 D.熔融的KOH
难度: 简单查看答案及解析
-
下列反应中,氯元素全部被氧化的是
A.2Fe+3Cl2═2FeCl3 B.2NaCl
2Na+Cl2↑
C.NaOH+HCl═NaCl+H2O D.2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
难度: 简单查看答案及解析
-
氧化还原反应:
,
,向
、
混合溶液中通入适量
,溶液中某些离子的物质的量变化如图所示。下列说法不正确的( )
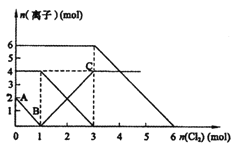
A.通过上述反应,比较还原性强弱
B.原混合液中
C.原混合液中
D.通入
时,溶液中发生的离子反应方程式为
难度: 困难查看答案及解析