-
《流浪地球》的热播让普通人了解到“人造空气”帮助人类实现了太空漫步的梦想,它含有 70% 的氮气(体积分数)、20%以上的氧气、还有 CO2 等。下列说法错误的是( )
A.“人造空气”比空气中的氮气含量高
B.在“人造空气”中,燃着的蜡烛不会迅速熄灭
C.利用灼热的铜粉,可粗略测定“人造空气”中氧气的含量
D.在太空中呼吸“人造空气”时,氧气消失但氧原子并未消失
难度: 简单查看答案及解析
-
中华古代文化蕴含着丰富的化学知识。下面理解合理的是( )
A.“露从今夜白,月是故乡明”描述中只有化学变化
B.“暖暖远人村,依依墟里烟”描述中只有物理变化
C.“野火烧不尽,春风吹又生”描述中包含了化学变化
D.“金(即钢)柔锡柔,合两柔则刚”说明合金的熔点比组成它的纯金属高
难度: 简单查看答案及解析
-
“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述正确的是( )
A.缺乏维生素A,会引起贫血 B.小苏打可作为治疗胃酸过多症的药剂
C.室内起火,应迅速打开所有门窗通风 D.氢氧化钠沾到皮肤上,要立即涂上硼酸溶液
难度: 简单查看答案及解析
-
中国科学院发布了113号、115号、117号及118号四种元素的中文名称,其中一种元素在元素周期表中的信息如图所示,下列有关该元素的说法正确的是( )
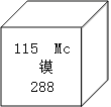
A.该元素属于非金属元素 B.核内有115个质子
C.镆原子质子数与中子数之和为403 D.该原子的质量为288
难度: 简单查看答案及解析
-
下列实验操作正确的是
A.
 闻药品的气味 B.
闻药品的气味 B.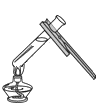 给液体加热
给液体加热C.
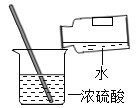 稀释浓硫酸 D.
稀释浓硫酸 D.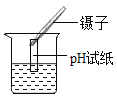 测溶液pH
测溶液pH难度: 简单查看答案及解析
-
我国是世界上第一个在海域成功试采可燃冰的国家,可燃冰的结构如图所示,甲烷分子(CH4)被包进水分子构成的“笼子”内,下列有关说法正确的是
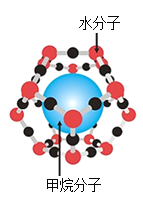
A.用可燃冰作燃料会大大减弱温室效应
B.“笼子”内的甲烷分子不再运动
C.可燃冰中甲烷分子和水分子何存在间隔
D.可燃冰提供了水可能变成油的例证
难度: 简单查看答案及解析
-
图示分析是学习化学的一种重要方法,下列图示分析正确的是
A.
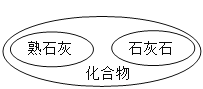 物质的分类
物质的分类B.
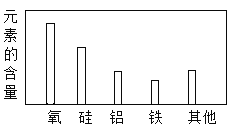 地壳中元素的含量
地壳中元素的含量C.
生活中常见物质的pH
D.
燃烧的条件
难度: 简单查看答案及解析
-
对比实验是实验探究的一种重要方法,下列实验方案的设计中,没有利用对比实验方法的是
A.
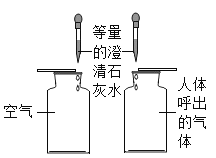 比较空气与人体呼出的气体中CO2的含量
比较空气与人体呼出的气体中CO2的含量B.
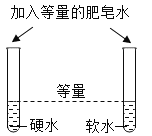 区分硬水和软水
区分硬水和软水C.
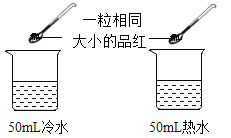 探究温度对分子运动快慢的影响
探究温度对分子运动快慢的影响D.
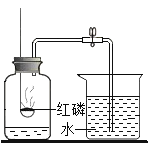 测量空气中氧气的含量
测量空气中氧气的含量难度: 简单查看答案及解析
-
科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如图,下列说法正确的是( )
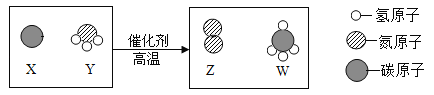
A.Y是由四种元素组成的化合物
B.该反应中X、Z两种物质的质量比为3:14
C.该反应中生成的Z和W两物质的分子个数比为1:1
D.参加反应的Y中氮元素的质量一定等于生成Z的质量
难度: 中等查看答案及解析
-
如图为Na2Cr2O7、Na2SO4两种物质的溶解度曲线,下列说法正确的是( )
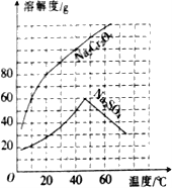
A.60℃时两种物质的溶解度:Na2Cr2O7大于Na2SO4
B.20℃时,Na2Cr2O7饱和溶液中溶质的质量分数为80%
C.两种物质的溶解度都随温度的升高而增大
D.50℃时,将210gNa2Cr2O7饱和溶液降温到10℃,析出150g Na2Cr2O7
难度: 简单查看答案及解析