-
钛被称为航空金属,国产C919大飞机的钛合金用量达到9.3%。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为
A. 4 B. 22 C. 26 D. 48
难度: 简单查看答案及解析
-
下列做法中,不符合“低碳”理念的是
A. 公交出行 B. 道路绿化 C. 节约用电 D. 浪费纸张
难度: 简单查看答案及解析
-
下列物质的性质中,属于化学性质的是
A. 铝具有导电性 B. 氢氧化钠能与硫酸铜反应
C. 氮气难溶于水 D. 常温下氧气是无色无味气体
难度: 简单查看答案及解析
-
每年5月31日为世界无烟日。吸烟有害健康,烟气中的一种有毒气体是
A.O2 B.N2 C.CO D.CO2
难度: 简单查看答案及解析
-
下列图标表示“禁止烟火”的是
A.
 B.
B. C.
C. D.
D.
难度: 简单查看答案及解析
-
下列物质中,含有氢分子的是
A.H2SO4 B.H2O C.H2 D.H2O2
难度: 简单查看答案及解析
-
硅酸钠(Na2SiO3)是制作防火板材的原料之一。其中,硅元素(Si)的化合价为
A.-4 B.-2 C.+2 D.+4
难度: 简单查看答案及解析
-
下列措施中,不能起到节约化石能源作用的是
A.采用风力发电 B.使用乙醇汽油
C.使用太阳能电池为路灯供电 D.使用脱硫煤燃烧发电
难度: 简单查看答案及解析
-
下列安全措施不正确的是
A.燃放烟花爆竹时,远离人群和可燃物
B.正在使用的家用电器着火,立即用水浇灭
C.燃着的酒精灯不慎碰倒,立即用湿布盖灭
D.天然气泄漏,立即关闭阀门并开窗通风
难度: 简单查看答案及解析
-
下列性质中,与“二氧化碳可用于灭火”无关的是
A. 不能燃烧 B. 能溶于水
C. 密度比空气大 D. 不支持燃烧
难度: 简单查看答案及解析
-
下列物质的化学式书写不正确的是
A.氧化铝AlO B.碳酸钙CaCO3
C.氢氧化镁Mg(OH)2 D.氧气O2
难度: 简单查看答案及解析
-
下列化学方程式书写正确的是
A.C+CO2
2CO B.4P + 5O2↑=2P2O5
C.2CO + O2
CO2 D.4Fe + 3O2
2Fe2O3
难度: 简单查看答案及解析
-
下列关于 CaCO3
CaO+ CO2↑的说法正确的是
A.反应中CaCO3和CO2的质量比为1:1 B.反应中原子种类发生了改变
C.反应中元素种类没有发生改变 D.CaCO3中的氧元素全部转化到CO2中
难度: 中等查看答案及解析
-
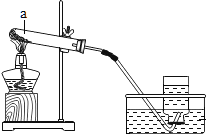
下列实验基本操作中,正确的是
A.
检查装置气密性 B.
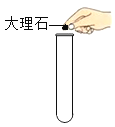 加入块状固体 C.
加入块状固体 C.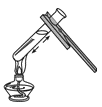 加热液体 D.
加热液体 D.滴加液体
难度: 简单查看答案及解析
-
实验室制氯气的反应为:MnO2 + 4HCl(浓)
MnCl2 + Cl2↑ + 2X,则X的化学式是
A.O2 B.H2 C.H2O D.H2O2
难度: 简单查看答案及解析
-
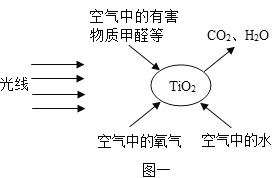
根据图示,下列说法中,不正确的是

A. MnO2可作为该反应的催化剂
B. 用该反应可以制备氧气
C. 物质不同,其元素组成一定不同
D. 该反应属于分解反应
难度: 中等查看答案及解析
-
如图所示,下列关于物质构成以及变化的说法中,正确的是
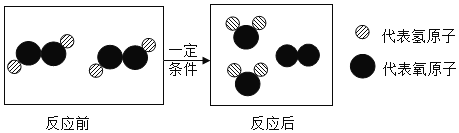
A.反应物中含有氧分子
B.反应前后,分子的种类一定发生改变
C.当34份质量的H2O2参加反应时,生成32份质量的O2
D.反应物分子中,氢原子与氧原子质量之比为2:16
难度: 简单查看答案及解析
-
膨松剂是一种食品添加剂,它受热分解产生的气体,能使面胚在焙烤过程中变得松软、多孔。碳酸氢钠(NaHCO3)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一。它既可以作为碱性膨松剂单独使用,也可以与酒石酸氢钾、淀粉按一定比例混合制成复合膨松剂。复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是

A. 任何受热分解能产生气体的物质都可以做食品膨松剂
B. 碳酸氢钠受热分解的化学方程式为:NaHCO3
CO2↑+ H2O + Na2CO3
C. 碳酸氢钠做膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D. 复合膨松剂应在干燥的环境中保存
难度: 简单查看答案及解析
-
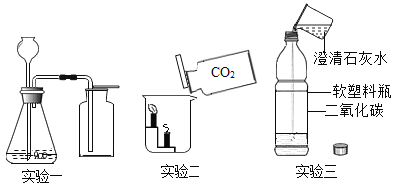
下图所示的四个实验中,得出的结论不正确的是( )
编号
A
B
C
D
实验设计

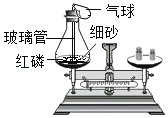
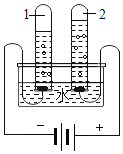

实验结论
二氧化碳能溶于水
化学反应前后物质的总质量不变
水是由氢气和氧气组成
MnO2能加快H2O2反应速率
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
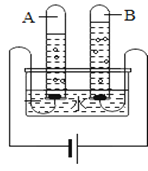
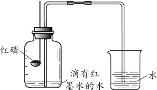
用下图所示4个实验探究二氧化碳能否与水反应(实验中所用的纸花均用石蕊染成紫色 并干燥),下列说法正确的是

A. 最终只有实验④中的紫色石蕊小花会变红
B. 实验④就能说明二氧化碳与水发生了反应
C. 在实验④中,若对比小花放入集气瓶前后的现象,可以不必做实验③
D. 由实验①④推断,实验④中有酸性物质
难度: 简单查看答案及解析








 _____Cu+____CO2↑。
_____Cu+____CO2↑。