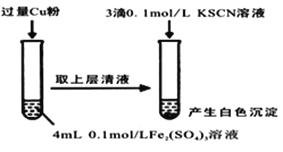
-
化学与人类生产、生活、社会可持续发展等密切相关。下列说法正确的是( )
A.活性炭具有除异味和杀菌消毒作用
B.碳化硅是一种新型的有机高分子材料
C.“光化学烟雾”、“硝酸型酸雨”的形成与氮氧化物有关
D.为更好地为植物提供N、P、K三种营养元素,可将草木灰与NH4H2PO4混合使用
难度: 中等查看答案及解析
-
下列化学用语对事实的表述正确的是 ( )
A.CH4或CCl4分子的比例模型:

B.硫化钠的电子式:
C.H2S的电离方程式:H2S
2H++S2-
D.由Na和Cl形成离子键的过程:

难度: 中等查看答案及解析
-
中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是( )
A.熬胆矾(CuSO4·5H2O)铁釜,久之亦化为铜 B.千淘万漉虽辛苦,吹尽狂沙始到金
C.凡石灰(CaCO3)经火焚炼为用 D.丹砂(HgS)烧之成水银,积变又成丹砂
难度: 中等查看答案及解析
-
下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
难度: 中等查看答案及解析
-
下列有关热化学方程式的叙述正确的是( )
A.已知甲烷的燃烧热为890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ/mol
B.已知C(s,金刚石)=C(s,石墨)ΔH=−1.9 kJ·mol−1,则石墨比金刚石稳定
C.已知中和热为ΔH=-57.3 kJ/mol,则NaOH与醋酸反应的中和热可以表示为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH=−57.3 kJ·mol−1
D.已知S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2
难度: 中等查看答案及解析
-
已知NA是阿伏加德罗常数的值,下列说法错误的是 ( )
A.常温常压下,17g甲基(-14CH3)所含的中子数为8NA
B.电解精炼铜,当外电路通过NA个电子时;阳极质量减少32g
C.1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D.17g H2O2中含有非极性键的数目为0.5NA
难度: 中等查看答案及解析
-
常温下,下列各组离子一定能在指定溶液中大量共存的是
A.
溶液中:
、
、
、
B.
的溶液中:
、
、
、
C.与Al反应能放出
的溶液中:
、
、
、
D.水电离的
的溶液中:
、
、
、
难度: 中等查看答案及解析
-
某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
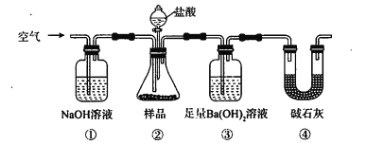
下列说法不正确的是
A.必须在②③间添加吸收HCl的装置
B.④的作用是防止空气中的气体影响实验的精确度
C.通入空气的作用是保证②中产生的气体完全转移到③中
D.称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
难度: 中等查看答案及解析
-
下列离子方程式能用来解释相应实验现象的是 ( )
A.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶【解析】
B.向沸水中滴加饱和氯化铁溶液得到红褐色液体:
C.二氧化硫使酸性高锰酸钾溶液褪色:
D.用铜做电极电解NaCl溶液: 2Cl﹣+2H2O
H2↑+Cl2↑+2OH﹣
难度: 中等查看答案及解析
-
W、X、Y、Z均为短周期主族元素,原子序数依次增大,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18。下列说法正确的是()
A.原子半径:W>X B.氧化物的水化物的酸性:Y<Z
C.阴离子的还原性:W>Z D.X与Y不能存在于同一离子化合物中
难度: 中等查看答案及解析
-
室温下,关于pH=11的NH3·H2O溶液,下列分析正确的是
A. c(NH3·H2O)=10-3mol/L
B. 由水电离出的c(H+)=10-11 mol/L
C. 加入少量 NH4Cl固体,NH3·H2O的电离平衡逆向移动,KW值减小
D. 加入等体积 pH=3的盐酸,所得溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
难度: 中等查看答案及解析
-
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。

下列说法中不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质
难度: 中等查看答案及解析
-
一种肼(N2H4)燃料电池的结构如图所示,下列说法正确的是 ( )
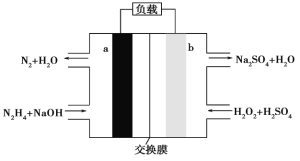
A.a为正极,电极反应式为:N2H4-4e-+4OH-=N2↑+4H2O
B.外电路中每通过1mol 电子,则有NA个Na+穿过交换膜向正极移动
C.b极的电极反应式为H2O2+2e-=2OH-
D.用该电池作电源电解饱和食盐水,当得到0.1mol Cl2时,至少要消耗0.1mol N2H4
难度: 中等查看答案及解析
-
下列图中的实验方案,能达到实验目的的是 ( )
A.验证FeCl3对H2O2分解反应有催化作用
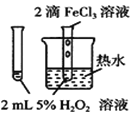
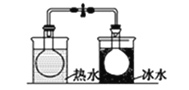
B.探究温度对平衡2NO2
N2O4的影响
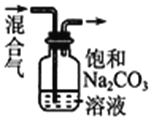
C.除去CO2气体中混有的SO2
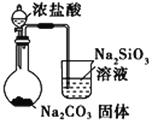
D.比较HCl、H2CO3和H2SiO3的酸性强弱
难度: 中等查看答案及解析
-
乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g)
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。下列分析不正确的是( )
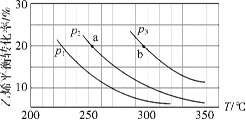
A.乙烯气相直接水合反应的∆H<0
B.图中压强的大小关系为:p1>p2>p3
C.图中a点对应的平衡常数K =
D.达到平衡状态a、b所需要的时间:a>b
难度: 中等查看答案及解析
-
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。下列推断正确的是 ( )
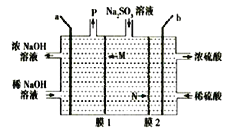
A.a极应与电源的负极相连
B.膜1为阴离子交换膜,膜2为阳离子交换膜
C.a极的电极反应式为2H2O一4e一=4H++O2↑
D.若收集22.4L的P(标准状况下),则转移4mol电子
难度: 中等查看答案及解析