-
苯环结构中不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使酸性KMnO4溶液褪色;②苯中碳碳键的键长均相等;③苯能在一定条件下跟H2发生加成反应生成环己烷;④经实验测得邻二甲苯仅一种结构;⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色。
A. ②③④⑤ B. ①③④⑤ C. ①②④⑤ D. ①②③④
难度: 简单查看答案及解析
-
化学与生活密切相关。下列说法错误的是( )
A. 用灼烧的方法可以区分蚕丝和人造纤维
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 医用消毒酒精中乙醇的浓度为95%
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
难度: 简单查看答案及解析
-
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是( )
A. 元素原子的最外层电子数等于元素的最高化合价
B. 多电子原子中,在离核较近的区域内运动的电子能量较高
C. 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
D. Si、P、S得电子能力和最高价氧化物对应水化物的酸性均依次增强
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是( )
A. 中子数为10的氧原子:
B. Mg的结构示意图:
C. 硫化钠的电子式:
D. 明矾的化学式:Al2(SO4)3
难度: 简单查看答案及解析
-
下列关于有机化合物的说法正确的是( )
A. 乙烯和聚乙烯互为同系物 B. 苯、乙醇和乙酸都能发生取代反应
C. C4H9Cl有3种同分异构体 D. 糖类和蛋白质都属于高分子化合物
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 氯化铵受热固体消失和干冰升华只需克服分子间作用力
B. NaF、H2SO4中所含化学键类型相同
C. HCl气体溶于水和NaOH熔化破坏的化学键类型相同
D. I2、Br2、Cl2、F2的熔沸点逐渐降低
难度: 中等查看答案及解析
-
下列有关化工生产的叙述错误的是( )
①电解熔融的氯化钠制取金属钠 ②将钠加入氯化镁饱和溶液中制取镁 ③用电解法冶炼铝时,原料是氯化铝 ④炼铁时高炉中所发生的反应都是放热反应,故无需加热
A. ②③ B. ①③ C. ①②③ D. ②③④
难度: 中等查看答案及解析
-
下列变化完全符合右图图示的是( )
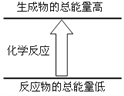
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④生石灰溶于水 ⑤二氧化碳与灼热的碳反应 ⑥碘的升华
⑦Ba(OH)2·8H2O与NH4Cl反应
A. ①②⑥ B. ②⑤⑦ C. ①②⑤⑥⑦ D. ②④⑤⑦
难度: 中等查看答案及解析
-
塑料、合成橡胶和合成纤维这三大合成材料,都主要是以石油、煤和天然气为原料生产的,下列有关说法错误的是( )
A. 天然气作为化工原料主要用于合成氨和生产甲醇
B. 煤可以直接液化,煤与氢气作用生成液体燃料
C. 煤是以单质碳为主的复杂混合物,干馏时单质碳与混合的物质发生化学变化
D. 通过石油的催化重整等工艺可获取芳香烃
难度: 中等查看答案及解析
-
在密闭容器中于一定条件下进行下列反应:2SO2+O2
2SO3,当达到平衡时通入18O2,再次平衡时,18O存在于( )
A. SO2、O2 B. SO2、SO3 C. SO2、O2、SO3 D. O2、SO3
难度: 简单查看答案及解析
-
下列事实不能用原电池原理解释的是( )
A. 家用电热水器不锈钢内胆镶嵌有镁棒 B. 用铝质铆钉接铁板,铁不易被腐蚀
C. 镀锌的铁制品比镀锡的铁制品耐用 D. 铁被钝化处理后不易腐蚀
难度: 中等查看答案及解析
-
在反应C(s)+CO2(g)
2CO(g)中,可使反应速率明显加快的措施是( )
①升高温度或增大压强 ②增加碳的量 ③恒容下通入CO2 ④恒压下充入N2 ⑤恒容下充入N2
A. ①③ B. ②④ C. ①④ D. ③⑤
难度: 简单查看答案及解析
-
如图所示的原电池装置中,X,Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
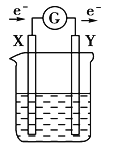
A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C. 若两电极都是金属,则它们的活动性强弱为X>Y
D. X极上发生的是还原反应,Y极上发生的是氧化反应
难度: 中等查看答案及解析
-
一定温度下,在容积恒定的密闭容器中,进行如下可逆反应:A(s)+B(g)
2C(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )
①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④B物质的量浓度
A. ①②④ B. ②③ C. ②③④ D. 全部
难度: 中等查看答案及解析
-
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:
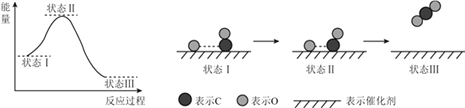
下列说法正确的是( )
A. CO和O生成CO2是吸热反应 B. 在该过程中,CO断键形成C和O
C. CO和O生成了具有极性共价键的CO2 D. 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
难度: 简单查看答案及解析
-
a、b、c、d 为原子序数依次增大的短周期主族元素,a 原子核外电子总数与 b 原子次外层的电子数相同;c 所在周期数与族数相同;d 与 a 同族,下列叙述正确的是
A. 原子半径:d>c>b>a B. 4 种元素中 b 的金属性最强
C. c 的氧化物的水化物是强碱 D. d 单质的氧化性比 a 单质的氧化性强
难度: 中等查看答案及解析
-
已知分解1mol H2O2放出热量98kJ。在含有少量I
的溶液中,H2O2分解的机理为: H2O2+I-
H2O+IO- 慢 ; H2O2+IO-
H2O+O2+I- 快
下列有关该反应的说法正确的是( )
A. 反应速率与I
浓度有关 B. IO
也是该反应的催化剂
C. H2O2分解生成1mol O2释放的热量为98kJ D. ν(H2O2)=ν(H2O)=ν(O2)
难度: 中等查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是( )
选项
实验操作和现象
实验结论
A
向某食盐溶液中滴加淀粉溶液,溶液颜色没有变为蓝色
不是加碘食盐
B
向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解
部分Na2SO3被氧化
C
向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液;未出现银镜
蔗糖未水解
D
向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色
溶液中含Br2
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(ν)如下表。下列判断不正确的是
c/mol·L-1
v/mmol·L-1·min-1
T/K
0.600
0.500
0.400
0.300
318.2
3.60
3.00
2.40
1.80
328.2
9.00
7.50
a
4.50
b
2.16
1.80
1.44
1.08
A. a=6.00 B. 同时改变反应温度和蔗糖的浓度,ν可能不变
C. b<318.2 D. 不同温度时,蔗糖浓度减少一半所需的时间相同
难度: 困难查看答案及解析
-
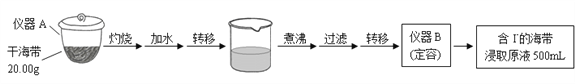
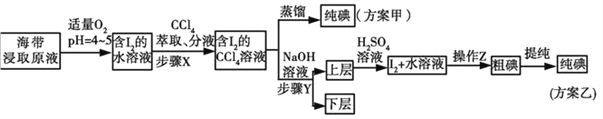
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是( )
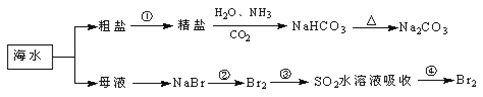
A. 除去粗盐中杂质(Mg2+、SO42﹣、Ca2+),加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→过滤后加盐酸
B. 用澄清的石灰水不可鉴别NaHCO3和Na2CO3
C. 在第②、④步骤中,溴元素均被氧化
D. 从第②步到第④步的目的是为了富集
难度: 中等查看答案及解析
-
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是
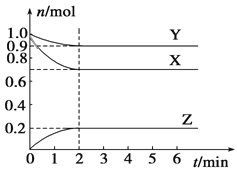
A. 该反应的化学方程式为3X+Y
2Z
B. 2 min时,反应达最大限度,但化学反应仍在进行
C. 2 min末时,Z的反应速率为0.05 mol·L-1·min-1
D. 反应达到平衡时,压强是开始时的0.9倍
难度: 困难查看答案及解析
-
CH4分子中的4个H被苯基取代后的分子结构如图所示,则关于该有机物下列说法正确的是

A. 该有机物分子式为C25H24
B. 最多可能有5个碳原子在同一直线上
C. 该分子中最多可能有13个碳原子在同一平面上
D. 该有机物能使酸性高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
在一定条件下,在容积为2 L的密闭容器中加入一定量的A,发生如下的反应并建立平衡:A(g)
2B(g), 2B(g)
C(g)+2D(g)。测得平衡时各物质的浓度是:c(A)=0.3 mol·L-1,c(B)=0.2mol·L-1,c(C)=0.05mol·L-1,则最初加入的A物质的量是( )
A. 0.45mol B. 0.5mol C. 0.9mol D. 1.2mol
难度: 中等查看答案及解析
-
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒 。下列说法正确的是( )

A. 正极反应为AgCl+e-=Ag+Cl-
B. 电池工作时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用KCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子
难度: 困难查看答案及解析
-
某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入标准状况下112 ml Cl2,恰好将Fe2+完全氧化。x值为( )
A. 0.80 B. 0.85 C. 0.90 D. 0.93
难度: 中等查看答案及解析