-
某学习小组按如下实验流程探究海带中碘的制取。
步骤(一)
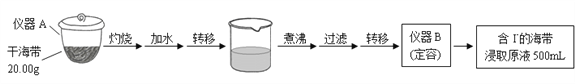
步骤(二)
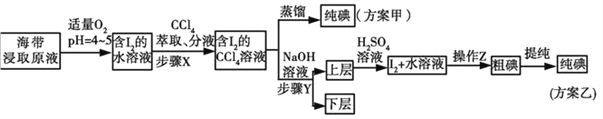
已知:①3I2+6NaOH=5NaI+NaIO3+3H2O;②常温下,碘单质微溶于水,易溶于CCl4。
请回答:
(1)步骤(一)中的仪器名称:仪器A______________, 仪器 B_______________。
(2)①分液漏斗使用前须检漏,检漏方法为__________________________。
②步骤X中,萃取后分液漏斗内观察到的现象是_______________________。
③下列有关步骤Y的说法,正确的是_______________。
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
④步骤(二)中操作Z的名称是_____________。
(3)方案甲中采用蒸馏不合理,理由是_____________________________________。
-
某课题组采用活性炭回收海带化工提碘废水中残留的低浓度碘(主要以I-形式存在,杂质不参与反应),实验过程如下:
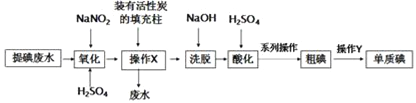
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;
I2+2S2O32-=2I-+S4O62-。
请回答:
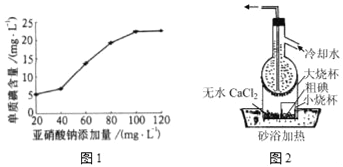
(1)结合图1可知,NaNO2最适宜的添加量为_____mg•L-1。
(2)操作X的目的是_____。
(3)系列操作中涉及抽滤操作,下列有关抽滤的说法中不正确的是_____。
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.当溶液具有强酸性、强氧化性时,可用玻璃砂漏斗代替布氏漏斗
C.抽滤不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(4)进行操作Y时所用装置如图2所示(省去了夹持装置),则操作Y的名称为_____;该装置中有两处不合理,请指出其中的一处_____。
(5)称取0.5080g粗碘试样于250mL碘量瓶中,加入足量的KI溶液,加盖摇匀至碘完全溶解.迅速用0.1200mol•L-1Na2S2O3标准溶液滴定至浅黄色,再加入淀粉指示剂,继续滴定至蓝色褪去即为终点,共消耗Na2S2O3标准溶液24.00mL。则粗碘试样中碘单质的纯度为_____。
-
某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定

取0.0100 mol·L-1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液于锥形瓶中,加2~3滴指示剂,达到终点时,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A的名称为 ;若滴定管洗净后未用标准溶液润洗,其它操作正确,测出碘的含量可能 (填“偏高”、“偏低”或“无影响”)。
(2)计算得海带中碘的百分含量为 %。
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水溶液中的溶解度很小。
(3)步骤X中,萃取后分液漏斗内观察到的现象是 。
(4)下列有关步骤Y的说法,正确的是 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH溶液可由乙醇代替
(5)实验(二)中操作Z的名称是 。
(6)方案甲中采用蒸馏不合理,理由是 。
-
某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
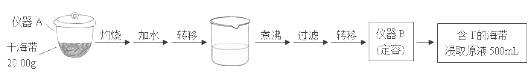
取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
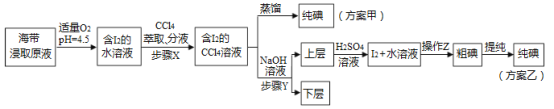
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)①实验(一) 中的仪器名称:仪器A_________, 仪器 B_________。
②该次滴定终点时用去AgNO3溶液的体积为_____mL,计算得海带中碘的百分含量为_______%。
(2)①步骤X中,萃取后分液漏斗内观察到的现象是_______________。
②下列有关步骤Y的说法,正确的是___________________。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二) 中操作Z的名称是______________________。
(3)方案甲中采用蒸馏不合理,理由是_____________________。
-
海带中含有丰富的碘。某研究性学习小组按下图所示实验流程提取海带中的碘。

回答下列问题:
(1)步骤①灼烧海带时,除三脚架外,还需要用到下列仪器中的________(填字母标号)。
A.烧杯 B.坩埚 C.蒸发皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是________。
(3)步骤④反应的离子方程式为____________________________。
(4)步骤⑤中,可以用苯来提取碘的理由是__________________,碘水溶液加入苯后,振荡、静止可观察到的实验现象为________。
(5)请设计实验检验提取碘后的水溶液中是否还有单质碘__________________。
-
某学习小组按如下实验过程(固定、加热及盛接仪器略)证明了海带中存在碘元素:

下列说法不正确的是
A.步骤①需要将干海带放入坩埚中灼烧
B.步骤②反应的离子方程式为:2I-+2H++H2O2=I2+2H2O
C.步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素
D.若步骤③加入的试剂是CCl4,振荡、静置后,液体分层,上层紫色,下层无色
-
海带中含有碘元素,某校研究性学习小组设计了如下实验步骤来提取碘:
①通足量氯气②将海带烧成灰,向灰中加水搅拌③加CC14振荡④过滤⑤用分液漏斗分液。合理的操作顺序为 ( )
A. ①→③→⑤→②→④ B. ②→①→③→④→⑤
C. ②→④→①→③→⑤ D. ③→①→②→⑤→④
-
某学习小组按如下实验流程制备乙酸乙酯,并测定乙酸乙酯的酸值(乙酸的含量)。

实验(一)乙酸乙酯的制取
已知:乙酸乙酯在盐溶液中溶解度较小
实验(二)乙酸乙酯酸值的测定
某同学通过查阅资料可知:
A.中和1g酯中含有的酸所需氢氧化钾的质量(mg)即为酸值,单位用mg/g表示;
B.常温下乙酸乙酯在稀碱溶液中反应速率较慢;
该学习小组设计如下实验步骤测定乙酸乙酯的酸值。
步骤1:取10mL乙醇,加入2-3滴酚酞试液,用0.10mol/LKOH标准液滴加至出现微粉红色,备用。
步骤2:用托盘天平称取10.0g样品,加入步骤1中配制的溶液,待试样完全溶解后,用0.10mol/LKOH标准液滴定,直至出现微粉红色,并保持5s不褪色即为终点。
步骤3:重复测定,计算乙酸乙酯的酸值 回答下列问题:
(1)实验(一)中浓硫酸的作用是 ;
(2)蒸馏2最适合的装置 。(加热装置和夹持仪器已省略)

(3)洗涤-分液环节操作②的目的是 。
(4)实验(二)步骤1加入乙醇的目的 ;
(5)下列操作会导致酸值测定结果偏高的是 。
A.装氢氧化钾标准液的滴定管水洗后直接滴定
B.溶液出现微粉红色,并持续30秒不褪色
C.锥形瓶用蒸馏水洗净后未干燥即盛放待测液
D.振荡过猛,锥形瓶中有溶液溅出
(6)数据记录如下表,计算酸值 mg/g。
| 次数 | 滴定前读数/mL | 滴定后读数/mL |
| 第1次 | 0.00 | 1.98 |
| 第2次 | 1.98 | 4.00 |
| 第3次 | 4.00 | 5.80 |
| 第4次 | 5.80 | 7.80 |
-
MgSO4·7H2O是一种重要的化工原料,某研究性学习小组设计了利用菱镁矿石(主要成分是MgCO3,并含有MnCO3、SiO2)制取MgSO4·7H2O的实验流程如下:
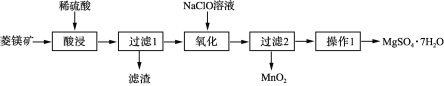
已知:Mn2++ClOˉ+H2O=MnO2↓+Clˉ+2H+
(1)过滤1的滤渣主要成分是______。
(2)酸浸时MgCO3发生反应的离子反应方程式为:_________________________。
(3)操作1经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤才可得到产品,检验产品是否洗涤干净的方法是_______________。
-
某校研究性学习小组设计了如下实验步骤来提取碘:
①加H2O2②将海带烧成灰,向灰中加水搅拌③加CC14振荡④过滤⑤用分液漏斗分液。合理的操作顺序为
A.②→④→①→③→⑤ B.②→①→③→④→⑤
C.③→①→②→⑤→④ D.①→③→⑤→②→④












