-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
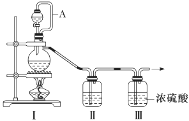
为制备纯净干燥的气体,补充下表中缺少的药品。
装置Ⅰ
装置Ⅱ
烧瓶中
分液漏斗中
制备纯净的Cl2
MnO2
①________
②________
制备纯净的NO
Cu
③________
④________
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
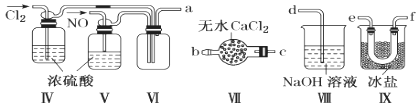
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________。
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________。
高二化学实验题困难题查看答案及解析
-
溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢被氧化。实验室制备
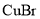 的步骤如下:
的步骤如下: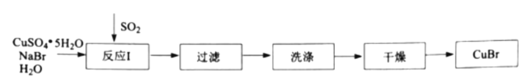
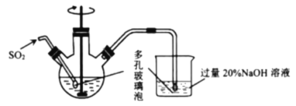
(1)反应Ⅰ在如图所示实验装置的三颈烧瓶中进行,实验所用蒸馏水需经煮沸,目的是除去水中的_________(写化学式)。
(2)反应Ⅰ中:三颈烧瓶中反应生成
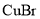 的离子方程式为________;烧杯中发生反应的化学方程式为________。
的离子方程式为________;烧杯中发生反应的化学方程式为________。(3)过滤步骤中,需要在避光的条件下进行,原因是________。
(4)洗涤步骤中,依次用溶有少量
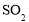 的水、溶有少量
的水、溶有少量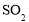 的乙醇、纯乙醚洗涤。洗涤剂需“溶有
的乙醇、纯乙醚洗涤。洗涤剂需“溶有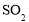 ”的原因是________。
”的原因是________。(5)欲利用上述装置烧杯中的吸收液制取较纯净的无水
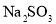 晶体。
晶体。(水溶液中
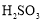 、
、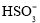 、
、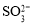 随
随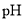 的分布,
的分布,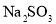 的溶解度曲线如题图所示)。
的溶解度曲线如题图所示)。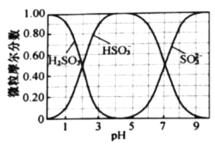
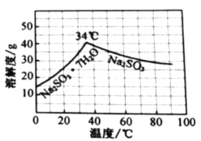
请补充完整实验方案[须用到
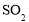 (贮存在钢瓶中)、
(贮存在钢瓶中)、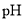 计]:
计]:①________;
②加入少量维生素C溶液(抗氧剂),加热浓缩溶液至有大量晶体析出;
③________;
④用无水乙醇洗涤2-3次;
⑤放真空干燥箱中干燥。
高二化学实验题困难题查看答案及解析
-
钴的某些化合物与铁的化合物性质相似,某研究性学习小组为探究钴的化合物的性质,进行了以下实验:
Ⅰ.探究草酸钴的热分解产物
(1)为探究草酸钴的热分解产物,按气体流动方向,各装置的连接顺序为:A→E→________________。
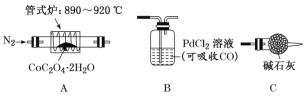
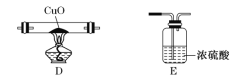
(2)能证明分解产物中有CO的实验现象是_____________________________________________________。
(3)取5.49gCoC2O4·2H2O于硬质玻璃管中加热至恒重,冷却、称量,剩余固体的质量为2.25g,球形干燥管增重1.32g。则球形干燥管吸收的气体的结构式为:__________________;A中发生反应的化学方程式为:_____________________________________________________。
Ⅱ.探究Co(OH)2的还原性及Co(OH)3的氧化性
取A装置所得固体溶解于稀H2SO4中得到粉红色溶液,备用。
已知试剂颜色:CoSO4溶液(粉红色),Co(OH)2(粉红色),Co(OH)3(棕褐色)。
实验记录如表:
实验操作及现象
实验分析
实验1
取少许粉红色溶液于试管中,滴加0.1mol·L-1NaOH溶液,生成粉红色沉淀,并将该沉淀分成两份
实验2
取一份实验1中所得的粉红色沉淀,加入3%的H2O2溶液,粉红色沉淀立即变为棕褐色
反应的化学方程式为___________________________
实验3
向实验2得到的棕褐色沉淀中滴加浓盐酸,固体逐渐溶解,并有黄绿色气体产生
反应的离子方程式为____________________________
实验4
取另一份实验1中所得的粉红色沉淀,滴加浓盐酸,粉红色沉淀溶解,未见气体生成
酸性条件下,Cl2、Co(OH)2、Co(OH)3的氧化能力由大到小的顺序是______________________________
高二化学实验题困难题查看答案及解析
-
铋酸钠(NaBiO3)是分析化学中的重要试剂,某化学兴趣小组设计下图实验装置制取铋酸钠并进行纯度检测。
(制取)氯气和氢氧化铋反应制取NaBiO3。
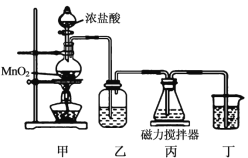
已知:① Bi(OH)3难溶于水,白色。
②装置丙中盛有Bi(OH)3与NaOH溶液混合物。
③NaBiO3不溶于冷水,浅黄色,遇沸水或酸则迅速分解。
(1)装置乙中盛装的试剂是__,装置丁的作用是__。
(2)装置丙中发生反应的离子方程式是_____。
(3)当观察到___现象时,可以初步判断丙中反应已完成。
(4)反应结束后,为了从装置丙中获得更多产品,需要的操作依次:在冰水中冷却结晶、___、干燥。
(5)有人设计如图的装置制取NaBiO3(加热和夹持仪器已略去)。
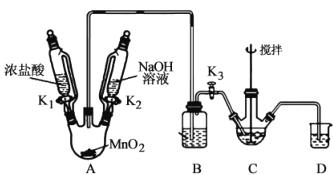
该装置比上一装置具有更高的安全性。
①盛浓盐酸的滴液漏斗中右侧玻璃管的作用是____。
②拆除装置前必须先除去A中残留Cl2以免污染空气。通过控制开关,除去Cl2的操作是___。
(检测纯度)
(6)取上述NaBiO3产品wg,用足量硫酸和MnSO4稀溶液使其还原为Bi3+,再用c mol•L-1的H2C2O4标准溶液滴定生成的MnO
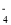 (已知:H2C2O4+ MnO
(已知:H2C2O4+ MnO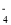 —CO2+Mn2++HO2,未配平),滴定终点时溶液的颜色变化为 __,假设终点时消耗VmL标准溶液。计算该产品的纯度为___(用含w、c、V的代数式表示)。
—CO2+Mn2++HO2,未配平),滴定终点时溶液的颜色变化为 __,假设终点时消耗VmL标准溶液。计算该产品的纯度为___(用含w、c、V的代数式表示)。高二化学实验题困难题查看答案及解析
-
辛烯醛是一种重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。
(制备实验)
已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848g•cm-3,不溶于水。
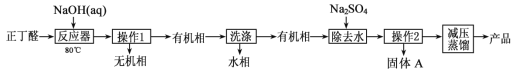
② CH3CH2CH2CHO
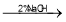
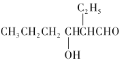
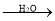
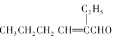
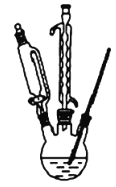
(1)在如图三颈瓶中加入12.6mL2%NaOH溶液,在充分搅拌下,从滴液漏斗慢慢滴入10mL正丁醛。采用适宜加热方式是 _____;使用冷凝管的目的是 ____ 。
(2)判断有机相已洗涤至中性的操作方法: ___ 。
(3)操作2的名称是____;固体A的摩尔质量为322g•mol-1,固体A的化学式为__ 。
(4)利用“减压蒸馏”操作获取产品。温度计示数一定_______177℃(填“高于”、“等于”或“低于”)。
(性质实验)
资料显示:醛类在常温下能与溴水、酸性高锰酸钾溶液反应。
(5)为了证明辛烯醛含有碳碳双键,设计能达到实验目的的方案 ___。
高二化学实验题困难题查看答案及解析
-
POCl3 遇水强烈水解:POCl3+ 3H2O = H3PO4 +3HCl,是一种重要的化工原料。某兴趣小组准备在实验室中进行 POCl3 制备实验。
(1)小组同学在如下装置中分别加入三氯化磷、氯气、二氧化硫来制备 POC13, 产物中还有一种遇水强烈水解的物质 SOCl 2, 写出制备反应的化学方程式_______。
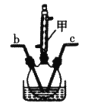
(2)仪器甲的名称是________。
(3)B中反应温度控制在60 ~ 65℃ , 不能过高或过低的原因是__________。
(4)小组同学查阅资料后,用以下方法测定POC13含量:准确称取4.00gPOCl3产品,配成20.00mL溶液,置于锥形瓶中;加入20.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;加入指示剂,用0.2000mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去20.00mLKSCN溶液。[已知:Ksp(AgC1)=3.2×l0-10,Ksp(AgSCN)=2×10-12]
①滴定选用的指示剂是_________(填字母代号);滴定终点的现象为___________。
A.FeCl2 B. NH4 Fe(SO4)2 C. 淀粉 D. 甲基橙
②用硝基苯覆盖沉淀的目的是____________。
③产品中 POC13的百分含量_______________(保留小数点后两位)。
高二化学实验题困难题查看答案及解析
-
己二酸在化工生产中有重要作用。某兴趣小组用50%的硝酸作氧化剂,钒酸铵作催化剂,氧化环己醇制备己二酸,其反应原理为
 ,实验装置如图所示。
,实验装置如图所示。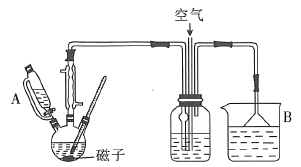
实验步骤:在装有回流冷凝管、温度计的
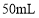 三颈烧瓶中,加入50%
三颈烧瓶中,加入50%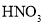 溶液(含
溶液(含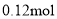
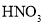 )及少量钒酸铵(
)及少量钒酸铵(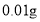 ),缓慢滴加5~6滴环己醇,有红棕色气体二氧化氮产生,将剩余的环己醇滴加完毕,总量为
),缓慢滴加5~6滴环己醇,有红棕色气体二氧化氮产生,将剩余的环己醇滴加完毕,总量为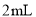 (约
(约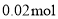 )。在温度为80~90℃时,反应至无红棕色气体逸出。将反应液倒入
)。在温度为80~90℃时,反应至无红棕色气体逸出。将反应液倒入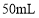 的烧杯中,冷却后,析出己二酸。减压过滤,用
的烧杯中,冷却后,析出己二酸。减压过滤,用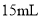 冷水洗涤,干燥后得到粗产品
冷水洗涤,干燥后得到粗产品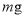 。
。回答以下问题:
(1)仪器A的名称为________,仪器B中所盛装的试剂为________。
(2)实验过程中,最适宜的加热方法为________;该加热方法的优点是________。
(3)本实验中称量钒酸铵的仪器应选用________(填“托盘天平”或“电子天平”)。
(4)减压过滤后的晶体用冷水洗涤,简述洗涤的操作过程:________。
(5)为测定粗产品中己二酸的含量,将得到的粗产品配成溶液,并用
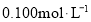 的
的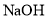 标准溶液进行滴定,下列操作可能使实际消耗
标准溶液进行滴定,下列操作可能使实际消耗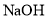 标准溶液的体积偏大的是________(填标号)。
标准溶液的体积偏大的是________(填标号)。A.使用甲基橙作指示剂
B.滴定前俯视读数,滴定后仰视读数
C.实验用的碱式滴定管、锥形瓶水洗后均未润洗
(6)若纯化后称重得到
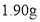 精制己二酸,则己二酸的产率为________(保留三位有效数字)。
精制己二酸,则己二酸的产率为________(保留三位有效数字)。高二化学实验题困难题查看答案及解析
-
含苯酚的工业废水的方案如下图所示:
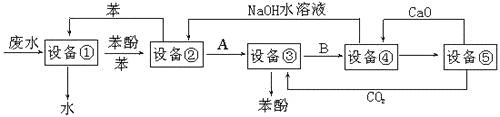
回答下列问题:
(1)设备①进行的是________操作(填写操作名称),实验室这一步操作所用的仪器是_______。
(2)由设备②进入设备③的物质A是_____________。
(3)在设备③中发生反应的化学方程式为_____________________________。
(4)在设备④中,物质B的水溶液和CaO反应,产物是CaCO3、_________和水,再通过过滤得产物。
(5)上图中,能循环使用的物质是C6H6、CaO、NaOH水溶液、___________。
(6)写出同时满足下列条件的苯酚的一种同分异构体的结构简式是_________。
①核磁共振氢谱只有一个峰
②分子中无碳碳双键
高二化学实验题困难题查看答案及解析
-
二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些支持装置省略了)所示。已知SO2Cl2的熔点为-54.1℃,沸点为69. 1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。

(1)仪器E的名称是_______,由B的使用可知SO2与氯气之间的反应居于______(填“放”或“吸”)热反应,B处反应管冷却水应从___________(填“a”或“b”)接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是__________。
(2)试剂X、Y的组合最好是_________。
a.98%硫酸和铜 b.稀硝酸和亚硫酸钠固体 c.60%硫酸和亚硫酸钾固体
(3)戊是贮气装置,则E中的试剂是_________;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是___________________________.
(4)取1.00g蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.50g,则所得馏分中二氯化砜的质量百分含量为__________%(结果保留小数点后1位)。
(5)二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是______。
高二化学实验题困难题查看答案及解析
-
将ClO2通入NaOH和H2O2的混合溶液中,可制得一种高效漂白剂亚氯酸钠(NaClO2),实验装置如图所示:
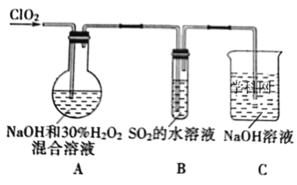
请回答:
(1)写出A装置中发生反应的离子方程式_____________。
(2)请设计实验方案探究通入ClO2一段时间后,B装置溶液中存在的含有硫元素的微粒_________。
高二化学实验题困难题查看答案及解析