-
新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是( )
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面方案等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
难度: 简单查看答案及解析
-
某校学生用化学知识解决生活中的问题,下列家庭小实验中不合理的是 ( )
A.用高度白酒进行皮肤消毒
B.用米汤(含淀粉)检验加碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3溶液)洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
难度: 中等查看答案及解析
-
某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
A.C14H18O5 B.C14H16O4 C.C16H22O5 D.C16H20O5
难度: 简单查看答案及解析
-
下列化合物中既含有离子键又含有共价键的是 ( )
A.HNO3 B.CaCl2 C.NH4Cl D.H2SO4
难度: 中等查看答案及解析
-
苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.脱落酸 B.乙烯 C.生长素 D.甲烷
难度: 简单查看答案及解析
-
已知一定温度时:2SO2(g)+O2(g) ⇌2SO3(g),当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
A.Q=197 kJ B.Q<197×2 kJ C.Q<197 kJ D.Q>197 kJ
难度: 简单查看答案及解析
-
下列表示物质结构的化学用语或模型图正确的是( )
A.
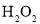 的电子式:
的电子式: 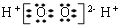
B.
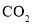 的比例模型:
的比例模型: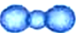
C.丙烷分子的比例模型示意图:
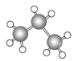
D.甲烷碱性燃料电池的负极反应式是:CH4+10OH--8e- =
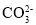 +7H2O
+7H2O难度: 中等查看答案及解析
-
某有机物的结构简式如图所示,有关该有机物的叙述正确的是
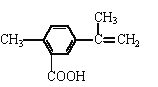
A.分子中含有3 种官能团
B.在一定条件下,能发生取代、氧化、酯化和加聚反应
C.该物质分子中最多可以有10 个碳原子在同一平面上
D.1 mol 该物质最多可与5 mol H2 发生加成反应
难度: 中等查看答案及解析
-
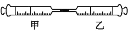
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯反应温度为115~125℃,反应装置如下图。下列对该实验的描述错误的是( )
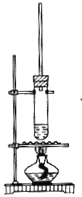
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
难度: 中等查看答案及解析
-
淀粉水解后,用新制的氢氧化铜悬浊液检验其水解产物,取适量淀粉后进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的氢氧化铜悬浊液;④加入足量的氢氧化钠溶液。以上各步操作的先后顺序是( )
A.①②③④① B.②①④③① C.②③①④① D.③④①②①
难度: 中等查看答案及解析
-
常压下羰基化法精炼镍的原理:Ni(s)+4CO(g)
 Ni(CO)4(g)。230 ℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4 的沸点为 42.2 ℃,固体杂质不参与反应。
Ni(CO)4(g)。230 ℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4 的沸点为 42.2 ℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至 230 ℃制得高纯镍。下列判断正确的是
A.增加 c(CO),平衡向正向移动,反应的平衡常数增大
B.该反应达到平衡时,
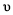 生成[Ni(CO)4])=4
生成[Ni(CO)4])=4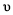 生成(CO)
生成(CO)C.第一阶段,在 30 ℃和 50 ℃两者之间选择反应温度,选50 ℃
D.第二阶段,Ni(CO)4分解率较低
难度: 中等查看答案及解析
-
我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图,下列说法不正确的是( )
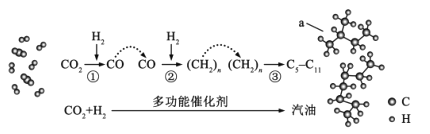
A.汽油主要是C5—C11的烃类混合物
B.反应①的产物中含有水
C.反应②中只有碳碳键形成
D.图中a的名称是2-甲基丁烷
难度: 简单查看答案及解析
-
某新型甲醚( CH3OCH3)燃料电池工作原理如图所示。下列说法正确的是( )
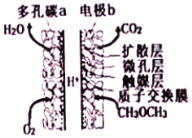
A.H+由b电极向a电极迁移,b极周围的pH变大
B.多孔碳a能增大气固接触面积,该电极为电池负极
C.甲醚直接燃烧的能量效率比燃料电池高
D.电极b上发生的反应为
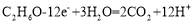
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C.1 mol Fe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24 L CCl4含有的共价键数为0.4NA
难度: 中等查看答案及解析
-
研究表明N2O与CO在Fe+的作用下会发生反应:①N2O+Fe+→FeO++N2、②FeO++CO→Fe++CO2,其能量变化示意图如图所示。下列说法错误的是( )
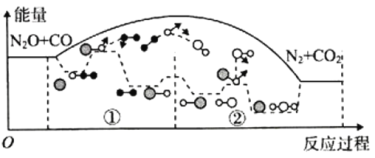
A.总反应△H<0
B.反应①过程中,N2O中的化学键发生了断裂
C.Fe+使反应的活化能减小
D.该催化剂可有效提高反应物的平衡转化率
难度: 中等查看答案及解析
-
根据海水综合利用的工业流程图,判断下列说法正确的是( )
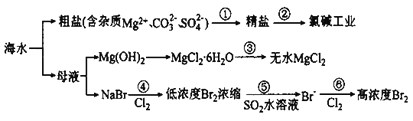
A.过程①的提纯时加试剂Na2CO3必须在BaCl2之前
B.在过程③中将MgCl2·6H2O制得无水MgCl2是物理变化
C.在过程④、⑥反应中每氧化0.2mol Br-一定需消耗2.24L Cl2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐浊问题
难度: 中等查看答案及解析
-
对于反应中的能量变化,下列表述中正确的是( )
A.放热反应中,反应物的总能量大于生成物的总能量 B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应 D.氧化还原反应均为吸热反应
难度: 简单查看答案及解析
-
a、b、c、d为短周期元素。a的单质既能与强酸反应又能与强碱反应,a的简单离子与
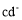 含有相同的电子数,b原子与c原子的最外层电子数相同。下列说法正确的是( )
含有相同的电子数,b原子与c原子的最外层电子数相同。下列说法正确的是( )A.简单氢化物的热稳定性:b>c
B.原子半径:b>a>c>d
C.工业上可以电解熔融的a的氧化物来制得a的单质
D.
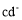 中各元素原子的最外层均满足8电子稳定结构
中各元素原子的最外层均满足8电子稳定结构难度: 中等查看答案及解析
-
有机物A的结构简式为
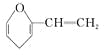 , A的同分异构体中带苯环的化合物(烯醇结构除外)共有
, A的同分异构体中带苯环的化合物(烯醇结构除外)共有A.3种 B.4种 C.5种 D.6种
难度: 中等查看答案及解析
-
汽车尾气净化的主要原理为
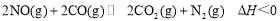 ,以下表格的“图像”中,若纵坐标代表不同物理量,其他条件一定, 甲和乙代表某一条件的改变,针对该反应的相关说法可能正确的是( )
,以下表格的“图像”中,若纵坐标代表不同物理量,其他条件一定, 甲和乙代表某一条件的改变,针对该反应的相关说法可能正确的是( )选项
纵坐标
甲
乙
图像
A
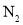 的体积分数
的体积分数未使用催化剂
使用催化剂
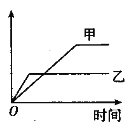
B
NO(g)的物质的量
400℃
500℃
C
平衡常数
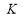
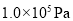
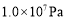
D
NO的转化率
CO(g)与NO(g)的物质的量之比为2∶1
CO(g)与NO (g)的物质的量之比为1 ∶2
A.A B.B C.C D.D
难度: 中等查看答案及解析
 CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1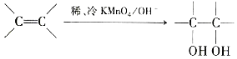 ,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式:__________。
,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式:__________。