-
表示两个氢分子的是
A. 2H B. 2H2 C. H D. H2
难度: 中等查看答案及解析
-
化学反应常常伴随发光、变色、产生沉淀等现象,下列反应现象描述错误的是
A.镁带在空气中燃烧,发出耀眼白光 B.硫在氧气中燃烧,发出蓝紫色火焰
C.铁丝在氧气中燃烧,生成四氧化三铁 D.红磷在空气中燃烧,产生大量白烟
难度: 简单查看答案及解析
-
属于化学变化的是
A.香水气味充满整个房间 B.自行车长期使用后,车身金属部分氧化
C.干冰用于人工降雨 D.从冰箱拿出的干燥玻璃杯,过一会表面有很多水珠
难度: 简单查看答案及解析
-
属于混合物的是
A.碳酸钙 B.干冰 C.冰水 D.木炭
难度: 简单查看答案及解析
-
属于化合反应的是
A.CH4+2O2
 CO2+2H2O B.2H2O
CO2+2H2O B.2H2O 2H2↑+O2↑
2H2↑+O2↑C.2Na+Cl2
 2NaCl D.C+2CuO
2NaCl D.C+2CuO  CO2↑+2Cu
CO2↑+2Cu难度: 简单查看答案及解析
-
84消毒液中有效成分为次氯酸钠NaClO,其中氯元素的化合价为
A.0 B.-1 C.+1 D.+2
难度: 简单查看答案及解析
-
与石墨互称同素异形体的是
A.活性炭 B.木炭 C.一氧化碳 D.金刚石
难度: 简单查看答案及解析
-
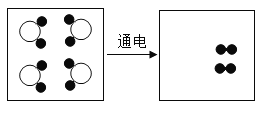
“
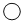 ”、“
”、“ ”、“
”、“ ”表示不同元素的原子,下图表示氧化物的微观示意图为
”表示不同元素的原子,下图表示氧化物的微观示意图为A.
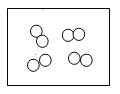 B.
B.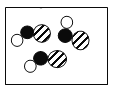 C.
C.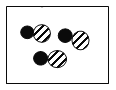 D.
D.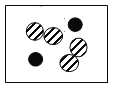
难度: 简单查看答案及解析
-
有关溶液说法正确的是
A.溶液由溶质和溶剂两种物质组成 B.溶液是均一稳定的化合物
C.溶液中一定含有水 D.水是常见的溶剂
难度: 简单查看答案及解析
-
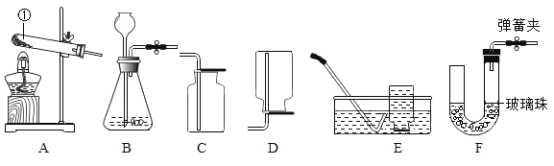
下列实验操作正确的是
A.
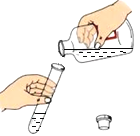 倾倒液体药品 B.
倾倒液体药品 B.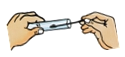 取用固体药品 C.
取用固体药品 C.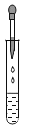 滴加少量液体 D.
滴加少量液体 D.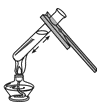 加热液体
加热液体难度: 简单查看答案及解析
-
实验测得某些溶液的pH如下,其中呈碱性的是
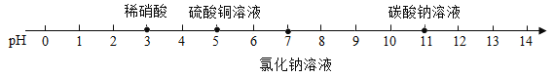
A.稀硝酸 B.硫酸铜溶液 C.氯化钠溶液 D.碳酸钠溶液
难度: 简单查看答案及解析
-
不属于氧气用途的是
A.供给呼吸
B.富氧炼钢
C.支持燃烧
D.钢铁生锈
难度: 简单查看答案及解析
-
下列化学方程式正确的且文字描述的事实相符的是
A.H2O+CO2=H2CO3 制作碳酸饮料
B.CuSO4+H2O=CuSO4∙H2O 检验水的存在
C.C+O2
 CO2 实验室制二氧化碳
CO2 实验室制二氧化碳D.CuO+CO
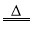 Cu+CO2 湿法炼铜
Cu+CO2 湿法炼铜难度: 中等查看答案及解析
-
用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( )
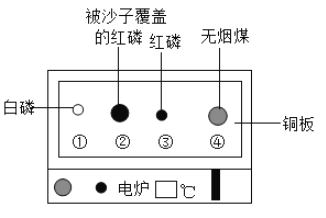
A. ①燃烧,说明白磷是可燃物
B. 对比①③,可说明红磷的着火点比白磷的高
C. 对比②③,可验证燃烧需可燃物与氧气接触
D. ④未燃烧,说明无烟煤不是可燃物
难度: 中等查看答案及解析
-
用集气瓶可完成多种实验.对下列实验示意图的分析正确的是
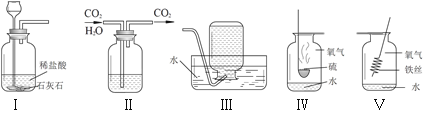
A.连接Ⅰ、Ⅲ装置,可以制取二氧化碳
B.Ⅱ中的液体一定可以做干燥剂
C.Ⅳ、Ⅴ中水的作用相同
D.将Ⅰ中药品改为双氧水和二氧化锰,依次连接Ⅰ、Ⅱ、Ⅲ装置,可以得到干燥的氧气
难度: 中等查看答案及解析
-
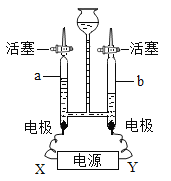
常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
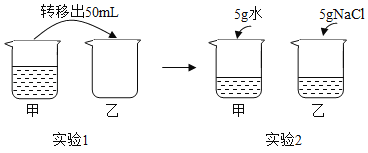
A. 实验1后,甲、乙中溶液的溶质质量分数相等
B. 实验2后,乙中比甲中氯化钠的溶解度大
C. 实验2后,甲中溶液为氯化钠的不饱和溶液
D. 实验2后,甲、乙中溶液所含溶质质量相等
难度: 中等查看答案及解析
-
实验设计能实现其对应的实验目的是
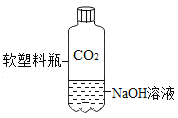
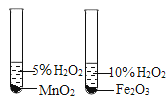
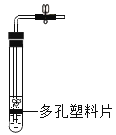
A. 测定空气中O2 的含量
B. 证明 CO2 与NaOH溶液反应
C. 比较 MnO2 和Fe2O3 的催化效果
D. 此装置具有“启普发生器”的功能
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
有关物质的量说法正确的是
A.物质的量就是物质所含微粒的数量,单位是 mol
B.物质的量就是 1mol 物质的质量
C.物质的量越大,表示该物质的分子越大
D.物质的量是国际单位制中的一个物理量,用符号“n”表示
难度: 中等查看答案及解析
-
t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH >7。关于溶液变浑浊的原因,同学们有两种观点:①Ca(OH)2 的溶解度随温度升高而减小;②Ca(OH)2 与空气中 CO2 反应。他们设计以下方案进行探究,其中没有意义的是
A.将装有浊液的烧杯,用冰水冷却,恢复到 t℃,观察浑浊是否消失
B.取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C.取适量浊液,过滤,往滤液中加入酚酞,观察是否变红色
D.其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
难度: 中等查看答案及解析
 H2O+CO↑。2. 浓硫酸具有吸水性。3. 氢氧化钠溶液可以吸收二氧化碳、二氧化硫等氧化物。某兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜并检验反应的产物,请回答:
H2O+CO↑。2. 浓硫酸具有吸水性。3. 氢氧化钠溶液可以吸收二氧化碳、二氧化硫等氧化物。某兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜并检验反应的产物,请回答: