-
下列变化属于化学变化的是( )
A.榨取果汁 B.燃放烟花 C.切割玻璃 D.汽油挥发
难度: 简单查看答案及解析
-
日常生活中加碘食盐、高钙牛奶中的“碘”和“钙”指的是( )
A.单质 B.分子 C.原子 D.元素
难度: 简单查看答案及解析
-
下列物质中,属于纯净物的是( )
A.蒸馏水 B.空气 C.海水 D.生铁
难度: 简单查看答案及解析
-
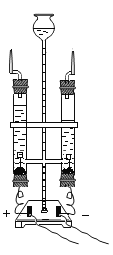
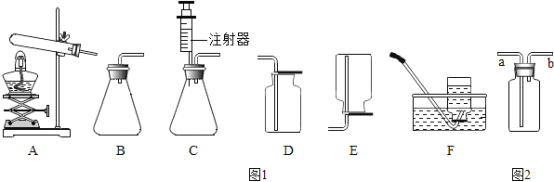
下图所示实验操作不正确的是( )
A.
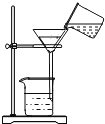 过滤 B.
过滤 B.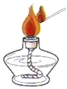 点燃酒精灯
点燃酒精灯C.
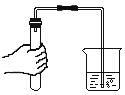 检查气密性 D.
检查气密性 D.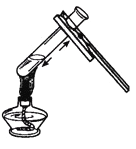 加热液体
加热液体难度: 简单查看答案及解析
-
保护环境利在千秋,功在当代。为了保护环境,你认为下列措施切实可行的是 ( )
①大量砍伐森林,作为燃料代替燃煤 ②合理使用化肥、农药 ③使用风力、水力发电代替火力发电 ④控制烟花爆竹的燃放 ⑤控制生活污水和工业废水的排放
A.只有②③④⑤ B.只有①③④⑤
C.只有①③⑤ D.①②③④⑤
难度: 简单查看答案及解析
-
钒被誉为“合金中的维生素”,钒元素的部分信息如下图。下列有关钒的说法正确的是
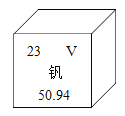
A.属于非金属元素 B.原子序数为23
C.原子核外电子数为28 D.相对原子质量为50.94g
难度: 中等查看答案及解析
-
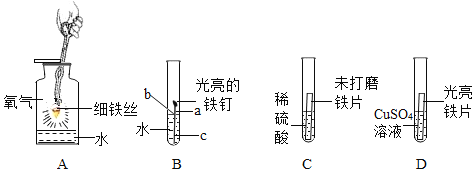
下列可用于验证Fe、Cu、Ag三种金属的活动性顺序的一组药品是 。
A.Fe、Cu、H2SO4溶液
B.Cu、Ag、FeSO4溶液
C.Fe、Ag、CuSO4溶液
D.Ag、FeSO4溶液、CuSO4溶液
难度: 中等查看答案及解析
-
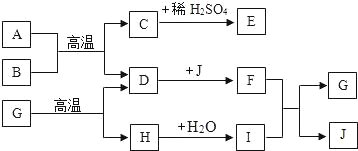
在
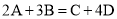 的反应中,已知
的反应中,已知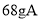 与
与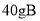 恰好完全反应,生成
恰好完全反应,生成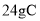 ,若A物质的相对分子质量为136,则D物质的相对分子质量为
,若A物质的相对分子质量为136,则D物质的相对分子质量为A.42 B.168 C.35.5 D.84
难度: 中等查看答案及解析
-
将零散的化学知识进行梳理、归纳,会使你的头脑变得更聪明。下列归纳中,全部正确的是( )
A.化学巨匠及杰出贡献
B.化学元素与人体健康
张青莲﹣﹣测量相对原子质量
侯德榜﹣﹣发明联合制碱法
门徒列夫﹣﹣发现元素周期律
缺铁元素﹣﹣发育迟缓智力低下
缺钙元素﹣﹣会发生骨质疏松或患佝偻病
缺碘元素﹣﹣会引起甲状腺肿大
C.生产生活中安全常识
D.日常生活中经验常识
煤气中毒﹣﹣由甲烷引起
煤气爆炸﹣﹣由一氧化碳引起
假盐中毒﹣﹣由亚硝酸钠引起
食品干燥剂﹣﹣常用浓硫酸
硬水与软水﹣﹣常用肥皂水检验
煤充分燃烧﹣﹣煤制成蜂窝状
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
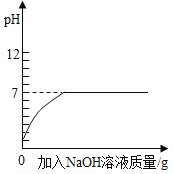
下列实验对应的图象正确的是( )
A.将等质量的镁和铝分别与足量的盐酸反应
B.向pH=2的盐酸中滴加过量的氢氧化钠溶液
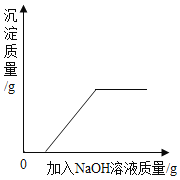
C.向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液
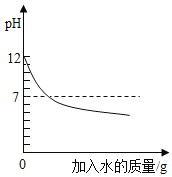
D.向pH=12的氢氧化钠溶液中加水稀释
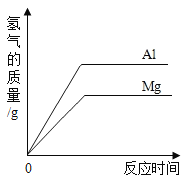
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列说法中一定正确的是( )
A.有机物都含碳元素,含碳元素的物质都是有机物
B.酸和碱生成盐和水,有盐和水生成的反应一定是中和反应
C.两种化合物生成两种化合物的反应不一定是复分解反应
D.碱溶液显碱性,显碱性的溶液﹣定是碱溶液
难度: 简单查看答案及解析