-
常温下,下列各组物质中,X既能与Y反应又能与Z反应的是
X
Y
Z
①
CO2
Ca(OH) 2溶液
H2O
②
H2
O2
CuO
③
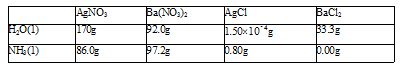
Ba(NO3) 2溶液
稀硫酸
Na2CO3溶液
④
Fe2O3
CO
稀盐酸
A.①② B.①③ C.①③④ D.①②③④
难度: 中等查看答案及解析
-
根据生活经验和所学知识判断,下列课外实验不能成功的是
A. 用pH试纸检验酸牛奶是否变质
B. 用肥皂水鉴别硬水和软水
C. 用食醋除去暖水瓶中的水垢
D. 用紫甘蓝和酒精溶液制酸碱指示剂
难度: 中等查看答案及解析
-
婴儿“尿不湿”最关键的材料是聚丙烯酸钠,其吸水性是棉花、纸张 的数十倍。它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸的说法中,正确的是
A. 它是有机高分子化合物
B. 其中氧元素与氢元素的质量比为9:1
C. 其中碳元素的质量分数为50%
D. 一个丙烯酸分子由3个碳原子、4个氢原子和1个氧分子构成
难度: 中等查看答案及解析
-
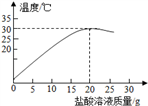
A、B、C三种物质的溶解度曲线如图5所示。下列分析正确的是

A. t1℃时,A、C两种物质的饱和溶液中溶质的质量相等
B. t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3
C. 将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A
D. 将C的饱和溶液变为不饱和溶液,可采用升温的方法
难度: 困难查看答案及解析
-
通过下列实验操作和现象能得出相应结论的是 ( )
实验操作
现象
结论
A
向收集满 CO2的软塑料瓶中加入约1/3 体积滴有石蕊试液的水,旋紧瓶盖,振荡
塑料瓶变瘪,
溶液变红
CO2能与石蕊反应
B
往久置于空气中的氢氧化钠溶液滴加稀硫酸
有气泡
氢氧化钠溶液已变质
C
在某无色溶液中滴加氯化钡溶液
有白色沉淀
无色溶液中一定含有
SO42-离子
D
把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸屮
镁条与盐酸
产生气体更快
镁的金厲活动性比锌强
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列说法正确的是 ( )
A.
 铁钉很快生锈 B.
铁钉很快生锈 B.  能用来检测空气中O2的含量
能用来检测空气中O2的含量C.
 白磷能燃烧 D.
白磷能燃烧 D.  乙厂只排出Na2SO4
乙厂只排出Na2SO4难度: 中等查看答案及解析
-
将10g碳酸钙固体高温煅烧足够时间,冷却后投入足量稀盐酸中完全反应。有关结论错误的是( )
A. 共生成11.1克氯化钙 B. 燃烧越充分则消耗的盐酸量越少
C. 共生成4.4克二氧化碳 D. 燃烧后固体中氧元素的质量分数减小
难度: 中等查看答案及解析
-
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是

A. 该反应为化合反应
B. 丙可能为该反应的催化剂
C. 该反应中,乙、丁的质量变化之比为7:5
D. 该反应中,甲、乙的质量变化之比为1:4
难度: 简单查看答案及解析
-
如图所示,加热烧瓶中的水使之沸腾.水蒸气从铜管喷出,把火柴靠近管口P处,火柴被加热,迅速移开火柴,火柴开始燃烧.下列说法正确的是 ( )
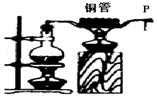
A. 水沸腾,水分子质量和体积增大
B. P处水蒸气的作用是提高火柴的着火点,使其燃烧
C. 火柴移离水蒸气,与氧气充分接触,从而燃烧
D. 水变为水蒸气质量不变符合质量守恒定律
难度: 中等查看答案及解析
-
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。对该实验的分析正确的是 ( )

A. 实验结束时应先熄灭D处酒精灯
B. C中增加的质量与B中固体减少的质量相等
C. 反应开始后通入2.8g一氧化碳可生成6.4g铜
D. 省略A装置仍可证明一氧化碳不能和石灰水反应,因为为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳,未见装置C变浑浊
难度: 中等查看答案及解析