-
下列有关物质的组成或分类说法正确的是( )
A. 金刚石、C60都是碳的化合物 B. 水、过氧化氢都含有相同组成元素
C. 碳酸氢铵、硫酸钾都是氮肥 D. 钙、氧都是人体必需的微量元素
难度: 中等查看答案及解析
-
2017年5月18日南海可燃冰试采成功,这是中国科学家勇攀世界科技高峰的又一标志性成就。1体积可燃冰可储载100~200倍体积的甲烷气体。甲烷(CH4)属于( )
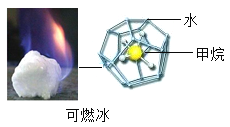
A.混合物 B.单质 C.氧化物 D.有机物
难度: 简单查看答案及解析
-
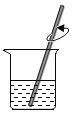
某学生要配制一定溶质质量分数的NaOH溶液,实验操作如图所示,其中正确的是( )
A.取用NaOH固体
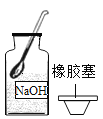
B.称量NaOH固体
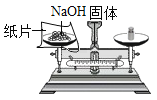
C.量取一定体积的水
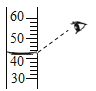
D.溶解NaOH固体
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.乙醇、橡胶都属于合成高分子材料
B.蛋白质、糖类均属于基本营养素
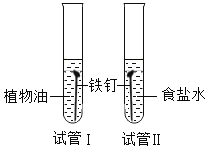
C.如图试管Ⅰ中铁钉比试管Ⅱ中更容易锈蚀
D.物质由气态变成液态,分子间的间隔变大
难度: 中等查看答案及解析
-
下列有关物质的性质与用途具有对应关系的是
A.石墨很软,因此可用作电池电极
B.H2具有还原性,因此可用于充氢气球
C.Al(OH)3能与盐酸反应,因此可用于治疗胃酸过多
D.N2不易溶于水,因此可用于焊接金属时的保护气
难度: 简单查看答案及解析
-
甲、乙、丙三种固体的溶解度曲线如图所示,下列说法正确的是
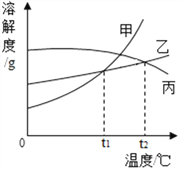
A.三种物质的溶解度:甲>乙>丙
B.t1℃时,溶质的质量分数:甲=乙
C.t2℃时,乙、丙的饱和溶液降温均有溶质析出
D.甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯
难度: 中等查看答案及解析
-
人类的日常生活和工农业生产离不开水,下列说法正确的是( )
A.无法用水鉴别硝酸铵、氢氧化钠两种固体
B.用水浇灭着火的纸箱,其原理是移除了可燃物
C.天然水经过自然沉降、过滤、吸附,即得纯水
D.使用加有洗涤剂的水可去除衣服上的油污
难度: 中等查看答案及解析
-
下列除杂所用试剂和主要实验操作均正确的是( )
物质(括号内为杂质)
所用试剂
主要实验操作
A
MnO2(KCl)
H2O
溶解、过滤
B
NaCl (MgSO4)
NaOH
溶解、过滤、蒸发
C
SO2(CO)
盐酸
溶解、蒸发结晶
D
NH3(H2O)
浓H2SO4
洗气
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
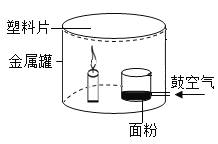
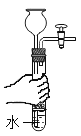
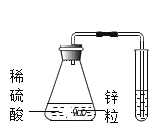
下列实验能达到实验目的是
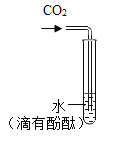
A证明CO2水溶液呈酸性
B验证面粉粉尘能发生爆炸
C检验该装置的气密性
D实验室制取并收集少量氢气
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
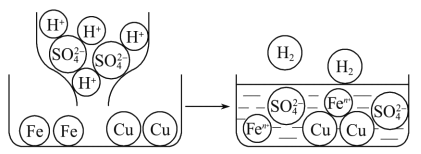
FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu
 cCuCl2+dX。向含溶质32.5 g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图。下列说法不正确的是
cCuCl2+dX。向含溶质32.5 g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图。下列说法不正确的是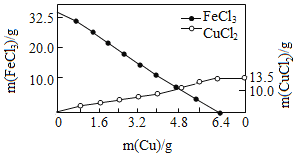
A.X为FeCl2 B.化学计量数c=1
C.方程式中a和b的比为1∶2 D.完全反应后,生成X的质量为25.4 g
难度: 中等查看答案及解析
 粉末”的实验进行探究:
粉末”的实验进行探究: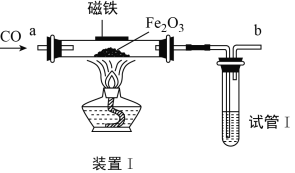
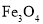 均为黑色固体;铁粉、
均为黑色固体;铁粉、
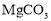 、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:_____、_____(填化学式)。
、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:_____、_____(填化学式)。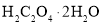 )制备CO:
)制备CO: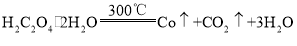
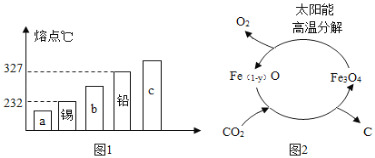
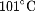 。比较草酸晶体的熔点和分解温度,分析若选用下图装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是__________。
。比较草酸晶体的熔点和分解温度,分析若选用下图装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是__________。