-
苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.脱落酸 B.乙烯 C.生长素 D.甲烷
难度: 简单查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A. Al2O3熔点高,可用作耐高温材料
B. SO2具有氧化性,可用于漂白纸浆
C. SiO2硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
难度: 简单查看答案及解析
-
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
选项
叙述Ⅰ
叙述Ⅱ
A
酸性:HCl>H2S
非金属性:Cl>S
B
铁表面镀锌可以增强其抗腐蚀性
构成原电池且铁作负极
C
Na在Cl2中燃烧的生成物含离子键
NaCl固体可导电
D
向NaI溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈紫红色
I-还原性强于Cl-
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
2019年6月5日,中国主办世界环境日,聚焦“空气污染”主题.有关该主题的以下说法不正确的是( )
A.PM2.5是指大气中直径小于等于2.5微米的颗粒物,也称可入肺颗粒物
B.汽车排放的废气主要有一氧化碳、二氧化硫、氮氧化物和碳氢化合物等
C.防治空气污染除了要减少污染物的排放量,还要从我做起
D.氮氧化物不仅会形成酸雨等危害,还会引起温室效应
难度: 简单查看答案及解析
-
垃圾处理无害化、减量化和资源化逐渐被人们所认识。垃圾的分类收集是实现上述理念的重要措施。某垃圾箱上贴有如图所示的标志,向此垃圾箱中丢弃的垃圾应是( )

A.危险垃圾 B.可回收垃圾 C.有害垃圾 D.其他垃圾
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A.硫离子的结构示意图:
 B.氯化氢的电子式:
B.氯化氢的电子式: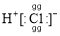
C.
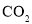 的电子式是
的电子式是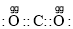 D.
D.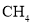 的比例模型:
的比例模型:
难度: 简单查看答案及解析
-
2016年1月《中国科学报》报道,又有113号、115号、117号和118号四种元素被载入元素周期表.其中118号元素的原子符号为
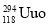 ,该原子的中子数为( )
,该原子的中子数为( )A.294 B.176 C.1l8 D.412
难度: 中等查看答案及解析
-
下列物质中既有离子键又有共价键的化合物是( )
A.
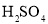 B.
B.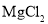 C.
C.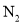 D.
D.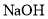
难度: 简单查看答案及解析
-
下列过程中所发生的化学变化属于取代反应的是( )
A.光照射甲烷与氯气的混合气体 B.乙烯通入溴水中
C.在镍做催化剂的条件下,苯与氢气反应 D.乙酸溶液中加入纯碱
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.苯和乙烯均可使酸性
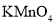 溶液褪色
溶液褪色B.纤维素、淀粉和蛋白质都是高分子化合物
C.煤的干馏和石油的分馏均属物理变化
D.葡萄糖和淀粉均能发生水解反应
难度: 简单查看答案及解析
-
对于工业合成氨反应:N2+3H2
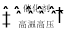 2NH3,下列说法错误的是( )
2NH3,下列说法错误的是( )A.使用合适的催化剂可以加大反应速率 B.升高温度可以增大反应速率
C.增大N2浓度可以使H2完全反应 D.增大N2浓度可以增大反应速率
难度: 简单查看答案及解析
-
海水电池常用在海上浮标等助航设备中,其示意图如图所示。电池反应为2Li+2H2O=2LiOH+H2↑。电池工作时,下列说法错误的是( )
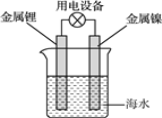
A.金属锂作负极
B.电子从锂电极经导线流向镍电极
C.海水作为电解质溶液
D.可将电能转化为化学能
难度: 简单查看答案及解析
-
下列各组离子在溶液中可以大量共存的是( )
A.
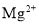 、
、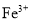 、
、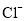 、
、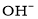 B.
B.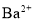 、
、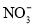 、
、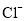 、
、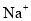
C.
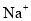 、
、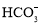 、
、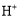 、
、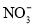 D.
D.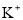 、
、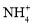 、
、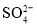 、
、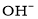
难度: 简单查看答案及解析
-
用
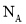 表示阿伏加德罗常数的值,下列叙述正确的是( )
表示阿伏加德罗常数的值,下列叙述正确的是( )A.常温常压下,
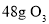 含有的氧原子数为3 NA
含有的氧原子数为3 NAB.标准状况下,
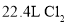 与足量的
与足量的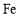 反应转移的电子数为3 NA
反应转移的电子数为3 NAC.NA个一氧化碳分子和
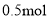 甲烷的质量比为7:4
甲烷的质量比为7:4D.
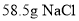 固体溶于1L的水中,所得溶液的物质的量浓度为
固体溶于1L的水中,所得溶液的物质的量浓度为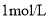
难度: 简单查看答案及解析
-
某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物;②煤和石油都是可再生能源;③
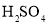 和
和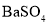 都是电解质;④不锈钢和目前流通的硬币都是合金;⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;⑥鸡蛋清的水溶液和雾都是胶体.上述说法正确的是( )
都是电解质;④不锈钢和目前流通的硬币都是合金;⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;⑥鸡蛋清的水溶液和雾都是胶体.上述说法正确的是( )A.①②④ B.①⑤⑥ C.②③④⑤ D.①③④⑥
难度: 简单查看答案及解析
-
自然界中氮的循环如图所示。下列说法不正确的是( )
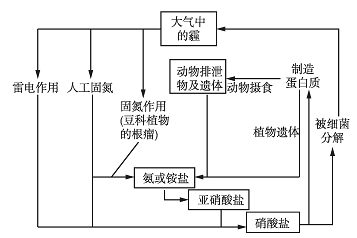
A.工业合成氨属于人工固氮
B.在雷电作用下N2与O2发生化学反应
C.在氮的循环过程中不涉及氧化还原反应
D.含氮无机物与含氮有机物可相互转化
难度: 简单查看答案及解析
-
某温度下,在一固定容积的容器中进行反应:SO3(g)+NO(g)
 NO2(g)+SO2(g),下列情况一定能说明已经达到化学平衡状态的是
NO2(g)+SO2(g),下列情况一定能说明已经达到化学平衡状态的是A. 气体的密度不再随时间而改变
B. 体系总质量不再随时间而改变
C. NO(g)和NO2(g)的生成速率相同
D. SO3(g)和NO(g)的浓度比为1:1
难度: 简单查看答案及解析
-
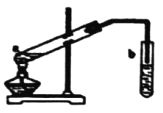
利用下列有关实验装置进行的相应实验,能达到实验目的的是( )
A.
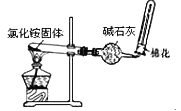 实验室制取纯净干燥的氨气
实验室制取纯净干燥的氨气B.
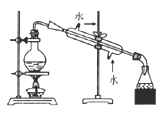 实验室用自来水制取蒸馏水
实验室用自来水制取蒸馏水C.
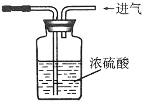 用浓硫酸干燥CO2
用浓硫酸干燥CO2D.
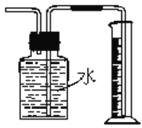 测量铜与浓硝酸反应生成气体的体积
测量铜与浓硝酸反应生成气体的体积难度: 中等查看答案及解析
-
下列反应的离子方程式书写不正确的是( )
A.铁与氯化铁溶液:Fe+Fe3+=Fe2+
B.稀盐酸与氢氧化钠溶液:H++OH-=H2O
C.铜与硝酸银溶液:Cu+2Ag+=Cu2++2Ag
D.碳酸钙与稀盐酸:CaCO3+2H+=Ca2+ +CO2↑+H2O
难度: 中等查看答案及解析
-
下列“实验结论”与“实验操作及现象”相符的一组是( )
选项
实验操作及现象
实验结论
A
向某溶液中加入
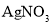 溶液,有白色沉淀生成
溶液,有白色沉淀生成该溶液中一定含有
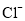
B
向某溶液中加入稀盐酸,有无色气体产生
该溶液中一定含有
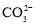
C
向某溶液中加入
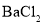 溶液,有白色沉淀生成
溶液,有白色沉淀生成该溶液中一定含有
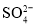
D
向某溶液中加入
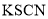 溶液,溶液变为红色
溶液,溶液变为红色该溶液中一定含有
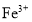
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列关于海水资源综合利用的说法中,正确的是( )
A.只通过物理变化即可提取海水中的溴单质
B.海水蒸发制海盐的过程只发生化学变化
C.从海水中可以得到
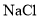 ,可电解
,可电解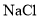 溶液制备
溶液制备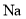
D.海水中提取镁的过程中加入贝壳煅烧制得的石灰,目的是将
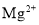 转变成
转变成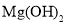
难度: 简单查看答案及解析
-
高炉炼铁中存在反应:
 ,下列说法不正确的是( )
,下列说法不正确的是( )A.该反应属于氧化还原反应
B.在该条件下,将还原剂
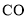 换成
换成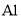 ,发生反应后也能生成
,发生反应后也能生成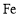
C.每生成
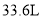 (标况下)的
(标况下)的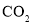 ,转移
,转移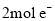
D.
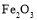 俗称“铁红”,外观为红棕色粉末,在该反应中被还原
俗称“铁红”,外观为红棕色粉末,在该反应中被还原难度: 简单查看答案及解析
-
前20号主族元素W、X、Y、Z的原子序数依次增加。W的最外层电子数是内层电子数的3倍,W、X、Z最外层电子数之和为10;W与Y同族。下列说法不正确的是( )
A. 简单离子半径 X > W B. W的氢化物沸点大于Y的氢化物沸点
C. Z的氧化物中含离子键 D. 最高价氧化物对应水化物的碱性 Z > X
难度: 中等查看答案及解析
-
巴豆酸的结构简式为CH3-CH=CH-COOH。现有①氯化氢;②溴水;③纯碱溶液;④丁醇;⑤酸性高锰酸钾溶液。试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A.②④⑤ B.①③④ C.①②③④ D.①②③④⑤
难度: 中等查看答案及解析
-
55g铁铝混合物与足量的盐酸反应生成标准状况下的氢气44.8L,则混合物中铁和铝的物质的量之比为 ( )
A.1:1 B.1:2 C.2:1 D.2:3
难度: 简单查看答案及解析
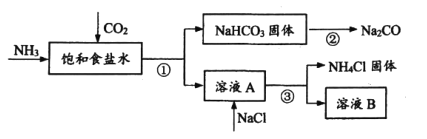
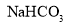 固体的化学方程式是_____________
固体的化学方程式是_____________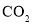 可循环使用
可循环使用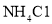 可用作肥料
可用作肥料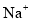 、
、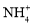 、
、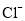
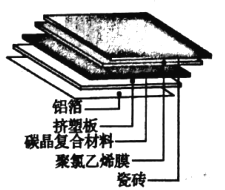
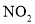 的过程中,会伴有C与
的过程中,会伴有C与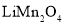 是锂离子电池的一种正极材料,可通过
是锂离子电池的一种正极材料,可通过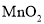 与
与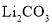 煅烧制备,同时还生成
煅烧制备,同时还生成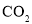 和一种单质,写出该反应的化学方程式:________
和一种单质,写出该反应的化学方程式:________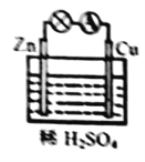
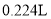 氢气(标准状况)时,导线中通过了____
氢气(标准状况)时,导线中通过了____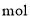 电子
电子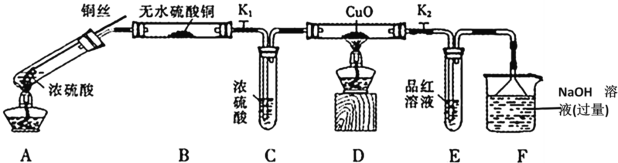
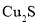 。产生
。产生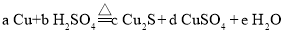 ,则
,则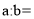 _____
_____