-
水是一种宝贵的自然资源,下列有关水的说法正确的是( )
A. 水的净化过程中用活性炭对水进行杀菌消毒
B. 生活中常用煮沸的方法将硬水转化成软水
C. 硬水中含较多的钙、镁化合物,长期饮用有益人体健康
D. 电解水的实验说明水由氢气和氧气组成
难度: 简单查看答案及解析
-
下列变化属于化学变化的是( )
A. 冰雪融化 B. 大米酿酒 C. 汽油挥发 D. 玻璃破碎
难度: 简单查看答案及解析
-
推理和归纳是研究和学习化学的重要方法下列说法正确的是( )
A.溶液是均一稳定的,所以均一稳定的物质,一定是溶液
B.单质由同种元素组成,所以由同种元素组成的物质一定是单质
C.氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素
D.催化剂可以加快化学反应速率所以任何化学反应当中都需要催化剂
难度: 简单查看答案及解析
-
图为空气成分示意图(按体积计算),其中“c”代表的是( )

A.二氧化碳 B.氮气 C.氧气 D.稀有气体
难度: 简单查看答案及解析
-
下列溶液中溶质判断正确的是( )
A.澄清石灰水:生石灰 B.碘酒:酒精 C.茶水:茶叶 D.生理盐水:氯化钠
难度: 简单查看答案及解析
-
配制6%的氯化钠溶液时导致溶质质量分数偏大可能原因是( )
A.转移称量好的氯化钠固体时有少量洒落在桌面上 B.量取水的体积时仰视量筒读数
C.转移配置好的溶液时有少量液体溅出 D.量取水的体积时俯视量筒读数
难度: 中等查看答案及解析
-
葡萄中含有丰富的叶酸,对防癌、抗癌有积极作用,其化学式为C19H19N7O6.下列有关叶酸的说法中正确的是( )
A.叶酸的相对分子质量为441g B.叶酸中碳、氢、氮、氧四种元素的质量比为19:19:7:6
C.叶酸中氮元素的质量分数大于氧元素的质量分数 D.叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
难度: 简单查看答案及解析
-
等质量的锌、铁与足量的稀硫酸反应,下列产生氢气的质量与反应时间的关系图,合理的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
有关化学基本观念的认识错误的是( )
A.微粒观:在化学变化中分子、原子均要改变形成新的分子和原子
B.能量观:天然气燃烧放出大量的热
C.分类观;过氧化氢和水从组成上看都属于氧化物
D.守恒观:镁带燃烧反应前后,元素种类和原子数目均不变
难度: 简单查看答案及解析
-
下列实验设计不能达到实验目的是( )
选项
A
B
C
D
实验设计
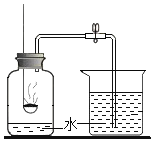
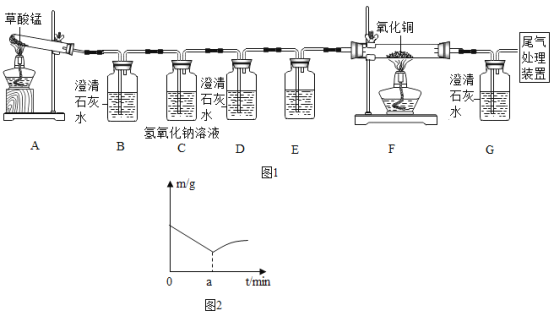
实验目的
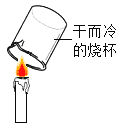
红磷燃烧测定空气中氧气的含量
探究石蜡中含有氧元素
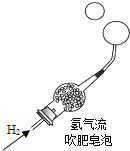
验证氢气的密度比空气小
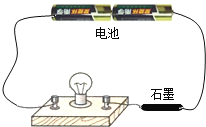
证明石墨具有导电性
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
据报道,中国科学技术大学研究人员利用钴及其氧化物成功研制一种新型催化剂,可将二氧化碳高效“清洁”地转化成液体燃料,反应的微观示意图如图。下列说法正确的是( )
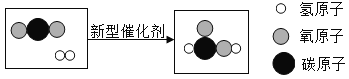
A.反应前后原子总数减少 B.可用于减少温室气体的排放
C.该反应的化学方程式为CO2+3H2
CH3OH+H2O D.反应物和生成物中共有两种氧化物
难度: 简单查看答案及解析
-
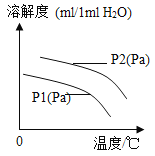
甲乙两种固体的溶解度曲线如图所示,下列说法正确的是( )

A.50℃时,100g水中加入20g乙并降温至20℃,溶液中溶质的质量分数不变
B.20℃时,可配制溶质质量分数为30%的乙溶液
C.20℃时,50g水中加入20g乙可得到饱和溶液70g
D.20℃时,甲的某一溶液中的溶质质量分数一定小于乙的某一溶液的质量分数
难度: 简单查看答案及解析
-
将未知金属M和金属镁的粉末状混合物共ag,加入一定质量的Cu(NO3)2、Fe(NO3)2的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关判断中,正确的是( )
A.若滤渣中含有Cu、Fe,则滤液一定为无色溶液 B.滤渣的质量一定大于ag
C.若向滤渣中加入稀盐酸没有气泡产生,则滤渣中一定只含有Cu D.若滤液中金属离子只含有Mg2+,则金属活动性一定有Mg>M
难度: 中等查看答案及解析
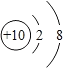 B.
B.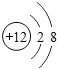 C.
C.