-
下列物质中,可用作复合肥料的是( )
A. KNO3 B. CO(NH2)2 C. K2SO4 D. Ca3(PO4)2
难度: 简单查看答案及解析
-
“抗击新冠肺炎疫情,人人都有群防责任”,下列做法符合科学道理的是
A.家庭消毒时,消毒液越浓越好 B.吸烟、喝酒可以预防“新型冠状病毒”
C.应经常保持室内清洁卫生和通风 D.必须每天吃药,补充人体所需化学物质
难度: 简单查看答案及解析
-
1月以来,各行业已有序复工。下列活动中,主要涉及化学变化的是
A.出示身份证件 B.登记身份信息 C.体温计测体温 D.用消毒剂消毒
难度: 简单查看答案及解析
-
75%的酒精溶液是医疗预防常用的消毒剂。75%的酒精属于
A.化合物 B.单质 C.氧化物 D.混合物
难度: 简单查看答案及解析
-
扬州某社区向武汉的医护人员捐赠10吨沼虾,沼虾为人体提供营养素主要是
A.淀粉 B.油脂 C.蛋白质 D.维生素
难度: 简单查看答案及解析
-
“84消毒液”(有效成分是次氯酸钠NaClO)能杀灭新冠病毒,次氯酸钠中Cl的化合价
A.+1 B.+2 C.+3 D.+4
难度: 简单查看答案及解析
-
氯气制备“84消毒液”时有如下反应:Cl2+2NaOH=NaCl+NaClO+X,则X的化学式
A.H2O2 B.H2O C.O2 D.H2
难度: 简单查看答案及解析
-
次氯酸钠(NaClO)可由NaOH+HClO=NaClO+H2O制得,该反应的基本反应类型为
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
难度: 简单查看答案及解析
-
中医在抗新冠疫情的中发挥了重要作用,下列中草药煎制操作步骤中,属于过滤的是
A.
 冷水浸泡 B.
冷水浸泡 B. 加热煎制
加热煎制C.
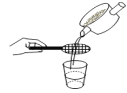 箅渣取液 D.
箅渣取液 D.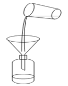 灌装保存
灌装保存难度: 简单查看答案及解析
-
南中医为我市中小学赠送了防疫香囊,香囊含有黄酮素(C15H10O2)。有关叙述正确的是
A.黄酮素属于有机物 B.黄酮素中碳、氢元素的质量比为3:2
C.黄酮素中含有氧分子 D.黄酮素的相对分子质量为222g
难度: 简单查看答案及解析
-
生活中的溶液显碱性的是
A.酸雨 B.果汁 C.肥皂水 D.盐水
难度: 简单查看答案及解析
-
7月1日起扬州正式实行垃圾分类,易拉罐应丢入贴有下列何种标志的垃圾箱里
A.

B. C.
C.
D.
难度: 简单查看答案及解析
-
为了安全,骑电动车时必须戴头盔,头盔的盔体部分采用玻璃钢材质,玻璃钢属于
A.复合材料 B.合成材料 C.金属材料 D.无机非金属材料
难度: 简单查看答案及解析
-
下列实验现象描述正确的是
A.足量SO2能使稀KMnO4溶液褪色 B.木炭在氧气中燃烧,产生二氧化碳
C.打开浓盐酸瓶塞,瓶口产生大量白烟 D.灼烧棉线,有烧焦羽毛气味产生
难度: 简单查看答案及解析
-
甲、乙两种固体物质的溶解度曲线如图所示。下列说法不正确的是
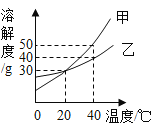
A.40℃时,甲的溶解度大于乙的溶解度
B.可用冷却热饱和溶液的方法从甲溶液中提取甲
C.20℃时,甲、乙两溶液中溶质的质量分数一定相等
D.将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液
难度: 简单查看答案及解析
-
“化学链燃烧”是新的燃烧概念,即燃料不直接与空气接触燃烧,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。该过程具有无火焰、低污染、高效率等特点。氧化镍(NiO)作载氧体的“化学链燃烧”过程如图,相比直接燃烧甲烷,对该技术的评价错误的是
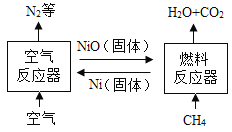
A.反应更充分、能源利用率高
B.较安全,减少爆炸风险
C.消耗等质量甲烷,参加反应氧气较少
D.有利于分离和回收较纯净的二氧化碳
难度: 简单查看答案及解析
-
回收硫酸铜废液中的铜,取12.8kg铁粉与硫酸铜废液混合,充分反应,过滤、洗涤、干燥,得到的固体能被磁铁吸引;再将该固体与过量的稀硫酸充分反应,过滤、洗涤、干燥,得固体12.8kg,不能被磁铁吸引。整个过程中参加反应的CuSO4与H2SO4的质量之比
A.80:7 B.80:49 C.10:7 D.8:7
难度: 中等查看答案及解析