-
用下列实验方案及所选玻璃仪器(非玻璃任选),就能实现相应实验目的的是( )
序号
实验目的
实验方案
所选玻璃仪器
A
除去KNO3中少量NaCl
将混合物制成热的饱和溶液,冷却结晶,过滤
酒精灯、烧杯、玻璃棒
B
证明HClO与CH3COOH的酸性强弱
同温下用pH试纸测定浓度为0.1mol/L'NaClO溶液和0.1mol/LCH3COONa溶液
玻璃棒、玻璃片
C
检验蔗糖水解产物且具有还原性
向蔗糖容易中加入几滴稀硫酸,水浴加热5分钟,再向其中加入新制银氨溶液,水浴加热
试管、烧杯、酒精灯、滴管
D
配制1L1.6%的硫酸铜溶液(其密度为1.0g/mL)
将25gCuSO4·5H2O溶解在975g水中
烧杯、量筒、玻璃棒
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列实验预测现象与实际相符的是
选项
实验
预测现象
A
向粗锌粒(含硫化物)中滴入稀硫酸,产生的气体通入少量KMnO4稀溶液中
KMnO4稀溶液紫色逐渐变浅
B
向砂纸打磨后的铝片上滴加浓硝酸
铝片逐渐溶解,产生红棕色气体
C
向品红溶液中通入足量Cl2,然后加热
溶液红色褪去,加热后恢复红色
D
向Fe2(SO4)3溶液中加入足量铁粉,充分反应后滴入KSCN溶液
溶液黄色逐渐褪去,滴入KSCN溶液后溶液变红
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
现代社会的发展与进步离不开材料,下列有关材料的说法不正确的是( )
A.500米口径球面射电望远镜被誉为“中国天眼”,其“眼眶”是钢铁结成的圈梁,属于新型纯金属材料
B.用于新版人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C.港珠澳大桥路面使用了沥青和混凝土,沥青可以通过石油分馏得到
D.国庆阅兵仪式上的坦克和军车都喷涂着新式聚氨酯迷彩伪装涂料,能适应多种环境背景下的隐蔽需求,聚氨酯属于有机高分子材料
难度: 简单查看答案及解析
-
中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是
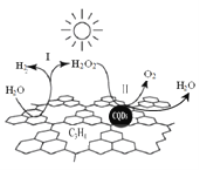
A. C3N4中C的化合价为−4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
难度: 中等查看答案及解析
-
已知
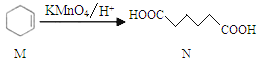 。下列说法错误的是
。下列说法错误的是A. M的分子式为C6H10
B. M中所有碳原子在同一平面上
C. N能发生氧化反应和取代反应
D. N的含有相同官能团的同分异构体有8种(不考虑立体结构)
难度: 中等查看答案及解析
-
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点。如图所示为镁-次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )
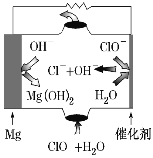
A.该燃料电池中镁为负极,发生氧化反应
B.正极反应为ClO-+H2O+2e-===Cl-+2OH-
C.电池总反应为Mg+ClO-+H2O===Mg(OH)2+Cl-
D.放电过程中OH-移向正极
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值。下列判断正确的是( )
A.1mol C3H8分子中含共用电子对数为10NA
B.1mol Cl2参加反应,转移电子数一定为2NA
C.Na2S和Na2O2固体混合物7.8 克中,含有的阴离子数为0.3 NA
D.电解精炼铜时,阳极质量减少12.8g时,转移电子数为0.4NA
难度: 中等查看答案及解析
-
下列解释事实的离子方程式正确的是( )
A.0.01 mol/LNH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:NH4++ Al3++ 2SO42-+ 2Ba2++ 4OH-=2BaSO4↓+ Al(OH)3↓+ NH3·H2O
B.铁和稀硝酸反应制得浅绿色溶液:Fe + 4H+ + NO3-=Fe3+ + NO↑+ 2H2O
C.向Ca(ClO)2溶液中通入过量CO2制次氯酸:2ClO-+ H2O + CO2==2HClO+CO32-
D.向酸性KMnO4溶液中通入SO2:2MnO4-+ 5SO2 + 4OH-=2Mn2+ + 5SO42-+ 2H2O
难度: 中等查看答案及解析
-
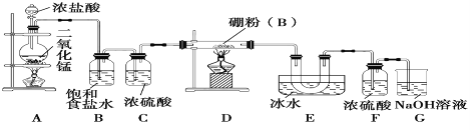
利用如图装置可制取二水亚硫酸铜(I,II)(Cu2SO3·CuSO3·2H2O)。下列说法错误的是
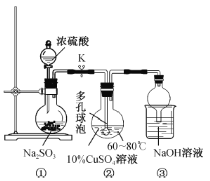
A.滴加浓硫酸前需先打开止水夹K
B.装置①中Na2SO3可换成铜屑
C.装置②加热时宜采用热水浴
D.装置③中的NaOH溶液可防止尾气污染
难度: 中等查看答案及解析
-
下列关于有机化合物的说法正确的是( )
A.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏得到
B.C6H3Cl2Br的同分异构体有7种(不含立体异构)
C.乙醇和乙酸均能与酸性KMnO4溶液发生氧化反应
D.X是苯的同系物,苯环上有两个位于对位的取代基,其结构可表示为
,则X的结构共有(不考虑立体异构)10种
难度: 中等查看答案及解析
-
X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4。化合物WYZ2是一种工业盐,对人体危害很大。下列叙述正确的是
A.简单氢化物的沸点:Y<Z
B.化合物WY3中只存在离子键
C.原子半径:W>Z>Y>X
D.X2Z与W2Z2发生的反应中,X2Z被氧化
难度: 中等查看答案及解析
-
X、Y、Z、W 为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断错误的是
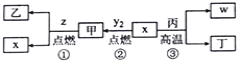
A.反应①、②、③都属于氧化还原反应
B.X、Y、Z、W四种元素中,Y的原子半径最小
C.Na 着火时,可用甲扑灭
D.一定条件下,x与甲反应生成丁
难度: 中等查看答案及解析
-
常温下,用0.1000
NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法不正确的是( )
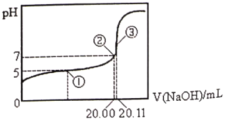
A. 点①②③三处溶液中水的电离程度依次增大
B. 该温度时CH3COOH的电离平衡常数约为
C. 点①③处溶液中均有c(H+)=c(CH3COOH)+c(OH-)
D. 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
难度: 中等查看答案及解析
-
用锌灰(主要成分Zn、ZnO,还含有少量FeO、MnO、CuO及SiO2)制备ZnC12溶液的一种工艺流程如下:
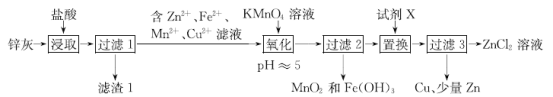
下列说法错误的是
A.“浸取”时不断搅拌可提高锌的浸取率
B.滤渣1的主要成分为SiO2
C.“氧化”时,Mn2+、Fe2+均被氧化
D.“置换”中所加试剂X可能是铁粉
难度: 中等查看答案及解析
-
常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数
(X)=
与pH的关系如图所示:
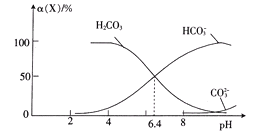
下列说法正确的是
A. 反应HCO3-
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
难度: 困难查看答案及解析
-
常温下,下列各组离子在指定溶液中能大量共存的是
A.NaHCO3溶液:K+、SO42-、Cl-、AlO2-
B.由水电离出的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.
=1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
难度: 中等查看答案及解析