-
除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物 质
杂 质
除杂所用试剂和方法
A
H2
HCl气体
先通过NaOH溶液,再通过浓硫酸
B
NaOH溶液
Ca(OH)2溶液
先加入过量的Na2CO3溶液,再过滤
C
CO2
CO
点燃气体
D
CaO固体
CaCO3固体
加入适量的稀盐酸
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列是某同学在填写实验报告册时描述的实验现象,其中正确的是
A.将氢氧化钠溶液滴入硫酸铜溶液中,产生蓝色沉淀
B.在稀盐酸中滴入石蕊试液,石蕊试液变成蓝色
C.在燃着的CO火焰上罩冷而干燥的烧杯,烧杯内壁出现小水珠
D.硫在氧气中燃烧时,产生白烟,生成有刺激性气味的气体
难度: 简单查看答案及解析
-
坚持人与自然和谐共生是我国新时代发展的基本方略之一。为建设“天蓝、地绿、水净”的美丽合肥,下列做法正确的是( )
A.推广使用太阳能等清洁能源
B.为发展经济过度开发矿产资源
C.在空旷的地方焚烧废旧塑料
D.工业废水直接排放到下水道
难度: 简单查看答案及解析
-
现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3,溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示,下列说法不正确的是( )
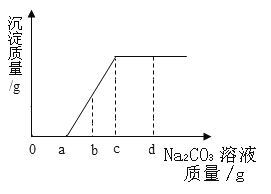
A.反应过程中先冒气泡,后产生白色沉淀
B.滴至bg时,溶液中的含HCl、NaCl两种溶质
C.滴至cg时,溶液恰好完全反应
D.滴至dg时,溶液pH>7
难度: 困难查看答案及解析
-
下列选项中物质的名称、俗名、化学式、类别、用途完全对应的是( )
A.碳酸钠 石碱
碱 制玻璃
B.氧化钙 熟石灰
氧化物 补钙剂
C.硫酸铜 胆矾
酸 制农药
D.氢氧化钠 苛性钠
碱 人造棉
难度: 简单查看答案及解析
-
化学与人类健康密切相关,下列做法正确的是( )
A.用福尔马林(甲醛的水溶液)对鱼肉等食品进行保鲜
B.在卤肉中添加过量的亚硝酸钠,使卤肉色泽鲜美
C.为保护水资源,禁止使用化肥、农药
D.适量的小苏打用于制作面包
难度: 简单查看答案及解析
-
某种新型药物的化学式为C5H4N3O2F,下列关于这种药物的说法中正确的是( )
A.这种药物是混合物
B.这种药物中碳元素和氢元素的质量比为5 : 4
C.这种药物中含有2个氢分子
D.这种药物由碳、氢、氮、氧、氟五种元素组成
难度: 简单查看答案及解析
-
实验室里Na2CO3试剂可能混有Ba(NO3)2、KCl、NaHCO3杂质,今取10.6g样品,溶于水得澄清溶液,另取10.6g样品,加入足量的盐酸,收集到4gCO2,则下列判断正确的是
A.样品中只含有NaHCO3 B.样品中混有KCl,也可能有NaHCO3
C.样品中有NaHCO3,也有Ba(NO3)2 D.样品中混有NaHCO3,也可能有KCl
难度: 困难查看答案及解析
-
有一包白色固体样品,可能由CaCO3、NaOH、MgCl2、Na2SO4和BaCl2中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。

下列判断正确的是( )
A. 原固体样品中一定有CaCO3、NaOH、MgCl2、BaCl2,可能有Na2SO4
B. 滤液中溶质的成分是NaOH、BaCl2
C. 滤渣a的成分是CaCO3
D. 若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品中仍能确定是否存在MgCl2
难度: 困难查看答案及解析