某种镀锡铜线表面锡的褪除及回收的工艺流程如图所示,请回答以下问题:
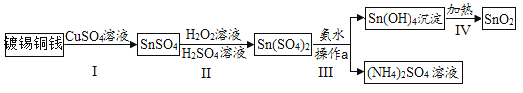
(1)Sn(OH)4中锡(Sn)的化合价为_________________。
(2)步骤Ⅲ中操作a的名称是_____________,该操作中用到的一种玻璃仪器的名称是______________。
(3)写出过程I中发生反应的化学方程式:_____________;过程IV发生的反应的基本反应类型是________。
九年级化学流程题中等难度题
某种镀锡铜线表面锡的褪除及回收的工艺流程如图所示,请回答以下问题:

(1)Sn(OH)4中锡(Sn)的化合价为_________________。
(2)步骤Ⅲ中操作a的名称是_____________,该操作中用到的一种玻璃仪器的名称是______________。
(3)写出过程I中发生反应的化学方程式:_____________;过程IV发生的反应的基本反应类型是________。
九年级化学流程题中等难度题
某种镀锡铜线表面锡的褪除及回收的工艺流程如图所示,请回答以下问题:

(1)Sn(OH)4中锡(Sn)的化合价为_________________。
(2)步骤Ⅲ中操作a的名称是_____________,该操作中用到的一种玻璃仪器的名称是______________。
(3)写出过程I中发生反应的化学方程式:_____________;过程IV发生的反应的基本反应类型是________。
九年级化学流程题中等难度题查看答案及解析
据统计,我国每年报废的手机超过 1 亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有 Sn、Fe、Cu、Au、Ag 等金属。如图是某工厂回收其中部分金属的流程图。( 假设流程图中各反应均恰好完全反应。已知: 2Cu+O2+2H2SO42CuSO4+2H2O)

(1)步骤②中产生的气体是_______ ;步骤②~⑤都涉及到的操作是_______ ,其中用到的金属仪器是 ____ 。滤渣 1 中含有的金属是____ (选填字母)。
A Cu、Sn、Au、Pd B Cu、Au、Ag、Pd
C Sn、Au、Ag、Pd D Cu、Sn、Au、Ag
(2)已知 Sn 的化合价为+2 价,则步骤③反应的化学方程式为________ 。
(3)步骤⑥回收的纯净物 B 是________ (写名称)。
九年级化学流程题简单题查看答案及解析
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有Sn、Fe、Cu、Au、Ag等金属。如图是某工厂回收其中部分金属的流程图。(假设流程图中各反应均恰好完全反应。已知:2Cu+O2+2H2SO42CuSO4+2H2O)

(1)步骤②中产生的气体是_____;步骤②~⑤都涉及到的操作是_____,其中用到的金属仪器是_____。滤渣1中含有的金属是_____(选填字母)。
A Cu、Sn、Au B Cu、Au、Ag C Au、Ag D Cu、Sn、Au、Ag
(2)已知Sn的化合价为+2价,则步骤③反应的化学方程式为_____。步骤⑤的现象为_____。
(3)步骤⑥回收的纯净物B是_____(写名称)。
九年级化学流程题中等难度题查看答案及解析
木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下。
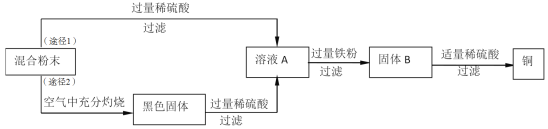
请根据流程图,回答下列问题:
(1)稀硫酸的溶质是H2SO4,其中硫元素的化合价为_________。
(2)固体B所含的物质是________(填物质化学式),溶液A加入过量铁粉的化学方程式是_________(任写一个)。
(3)检验得到的铜是否含铁粉的的操作是__________。
(4)途径2与途径1比较,途径2优点是__________。
九年级化学流程题中等难度题查看答案及解析
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程图如图:

已知:,铜与SnCl4不反应。
(1)在化学反应中含元素化合价升高的反应物作还原剂,降低的作氧化剂,的反应中还原剂是_____。
(2)步骤①中需要进行的操作是_____,实验室中进行该操作时需要用到的仪器有_____。
(3)固体A中一定含有的金属是_____,步骤②发生的反应属于_____(填基本反应类型)。
九年级化学流程题中等难度题查看答案及解析
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2。
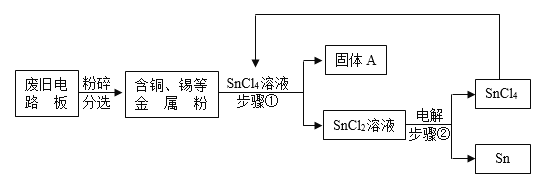
(1)步骤①的操作是_____。
(2)SnCl4中锡元素的化合价是_____。
(3)铜的金属活动性比锡的_____(填“强”或“弱”),固体A中一定含有的金属元素是_____(填元素符号)。
(4)写出步骤②发生反应的化学方程式_____,其基本反应类型是_____。
(5)该流程中可以循环利用的物质是_____。
(6)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是_____(回答一点即可)。
九年级化学流程题中等难度题查看答案及解析
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下:
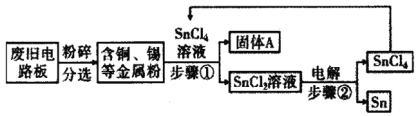
已知:Sn十SnCl2===2SnCl2
(1)SnCl2中锡元素的化合价是___________。
(2)步骤①的操作是_____,固体A中一定含有的金属元素是_____。
(3)写出步骤②发生反应的化学方程式______________。
(4)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是__________(回答一点即可)
九年级化学流程题简单题查看答案及解析
已知某矿石主要成分是MgO,另外还含有少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg (OH) 2的工艺流程简图如下:
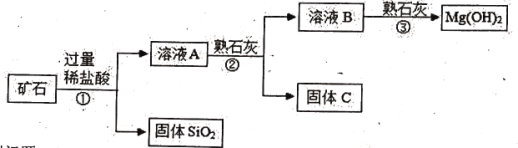
回答下列问题:
(1)请标出二氧化硅中硅元素的化合价______,步骤①和步骤②均用到某种操作,此操作中会用到的玻璃仪器有_____(写一种)。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、 Mg2+和_____(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
| 对应离子 | Fe3+ | Cu2+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的pH范围为_________。
步骤③制得Mg (OH) 2的化学方程式为_____.
九年级化学流程题中等难度题查看答案及解析
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2 。
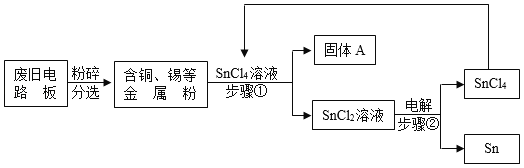
(1)SnCl4中锡元素的化合价是_______________。
(2)铜的金属活动性比锡的________(填“强”或“弱”),固体A中一定含有的金属元素是___________。
(3)写出步骤②发生反应的化学方程式____________,反应的基本类型是______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是___________(回答一点即可)。
九年级化学流程题简单题查看答案及解析
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2 。
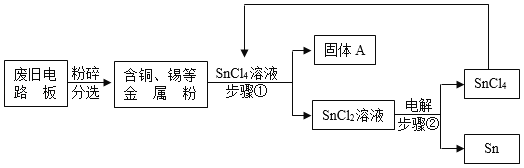
(1)SnCl4中锡元素的化合价是_______________。
(2)铜的金属活动性比锡的________(填“强”或“弱”),固体A中一定含有的金属元素是___________。
(3)写出步骤②发生反应的化学方程式____________,反应的基本类型是______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是___________(回答一点即可)。
九年级化学流程题简单题查看答案及解析