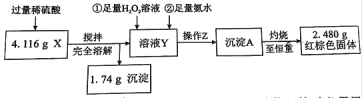
-
我国大力弘扬中华优秀传统文化体现“文化自信”。下列有关说法错误的是( )
A.制备“白玉金边素瓷胎,雕龙描凤巧安排”中的瓷,主要原料为黏土
B.商代后期铸造出了工艺精湛的司母戊鼎,该鼎属于铜合金制品
C.成语“百炼成钢”、“沙里淘金”中均包含了化学变化
D.《本草纲目》中有关于酿酒的记载“凡酸坏之酒,皆可蒸烧”,其描述的过程是蒸馏
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.Na2CO3和NaHCO3可做食用碱或工业用碱
B.海水晒盐的原理是升高温度从而降低食盐在水中的溶解度
C.二氧化硅是制造太阳能电池和计算机芯片的主要材料
D.在清洗卫生间时,从安全角度可将“洁厕灵”(主要成分是稀盐酸)与84消毒液混和使用
难度: 简单查看答案及解析
-
下列物质中属于纯净物的是( )
A.盐酸 B.胆矾 C.漂白精 D.水玻璃
难度: 简单查看答案及解析
-
下列气体呈无色无味的是( )
A.Cl2 B.SO2 C.NO2 D.CO
难度: 简单查看答案及解析
-
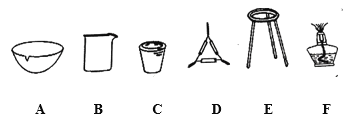
进行下列实验,括号内的实验用品都必须用到的是( )
A.配置一定物质的量浓度的溶液(容量瓶、烧杯、锥形瓶)
B.实验室制取蒸馏水(烧瓶、温度计、冷凝管)
C.钠的焰色反应(酒精灯、稀盐酸)
D.粗盐提纯(漏斗、玻璃棒、坩埚)
难度: 中等查看答案及解析
-
在盛装氯酸钾固体和浓硫酸的试剂瓶上,分别印有的警示标志是( )
①
②
③
④




A.②① B.②④ C.③④ D.③①
难度: 简单查看答案及解析
-
下列实验中,所采取的分离、提纯方法与对应原理都正确的是( )
选项
目的
分离方法
原理
A
分离煤油和水
分液
煤油的密度小于水
B
分离NH4Cl和Na2CO3
加热
热稳定性不同
C
分离KNO3和 NaCl
结晶
KNO3的溶解度大于 NaCl
D
分离C2H5OH和Br2的混合物
CCl4萃取
Br2在CCl4中溶解度极大
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列关于钠及其化合物说法正确的是( )
A.将小块钠投入滴有石蕊试液的水中,反应后溶液变红
B.钠的含氧化合物都是碱性氧化物
C.金属钠久置空气中最终转变为 NaHCO3
D.过氧化钠既具有氧化性也具有还原性
难度: 简单查看答案及解析
-
将两份等质量的铝片,分别投入等物质的量浓度等体积的稀硫酸和氢氧化钠溶液中充分反应,消耗的铝的质量比为( )
A.1:1 B.1:6 C.2:3 D.无法确定
难度: 中等查看答案及解析
-
标准状况下,一个装满CO2的容器的质量为67 g,若装满H2时总质量为60 .7 g,则此容器的容积为( )
A.2.24 L B.3.36 L C.11.2L D.4.48L
难度: 中等查看答案及解析
-
某溶液中只含有Na+、Al3+、Cl—、X四种离子,已知这四种离子的物质的量的浓度比为3:2:1:4 ,则X离子可能是( )
A.SO42— B.CO32— C.Mg2+ D.NO3—
难度: 简单查看答案及解析
-
人们常用图示的方法表示不同物质之间的关系,如溶液与胶体属于并列关系。非金属氧化物和酸性氧化物的关系可用图甲表示,图乙表示氢化物、氧化物和过氧化物三者之间的关系,则C表示( )
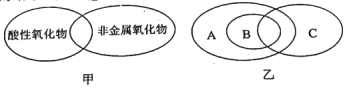
A.氢化物 B.氧化物 C.过氧化物 D.三者中的任意一类
难度: 简单查看答案及解析
-
所示装置能达到目的的是( )
A.
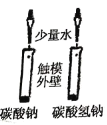 比较NaHCO3和Na2CO3的溶解度
比较NaHCO3和Na2CO3的溶解度B.
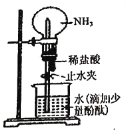 证明氨气易溶于水
证明氨气易溶于水C.
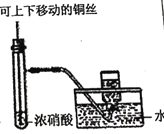 制备并收集少量NO2气体
制备并收集少量NO2气体D.
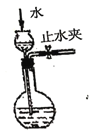 检验装置气密性
检验装置气密性难度: 中等查看答案及解析
-
根据以下三个实验:①铁钉放入硫酸铜溶液中 ②铜丝放入氯化铁溶液中 ③铜丝放入稀硝酸中,下列判断正确的是( )
A.实验①③中硫酸铜、稀硝酸都只做氧化剂
B.实验①②中发生的都是置换反应
C.实验③中可收集到NO、H2的混合气体
D.上述实验证明氧化性:稀硝酸>Cu2+>Fe2+
难度: 简单查看答案及解析
-
与0.2 L 1 mol/L FeCl3溶液中的氯离子的数目相同是( )
A.0.2 L 1 mol/L KCl溶液 B.0.6 mol HCl气体
C.0.2 L 3 mol/L KClO3溶液 D.0.6mol NaCl晶体
难度: 简单查看答案及解析
-
下列叙述中正确的是( )
A.离子反应一定使溶液中所有离子的浓度都发生变化
B.铁和醋酸溶液反应的离子方程式为Fe+2H+=Fe2++H2↑
C.硫酸铝钾在水中电离的方程式为KAl(SO4)2=K++Al3++2SO42-
D.酸碱中和反应都能用离子方程式H++OH-=H2O表示
难度: 简单查看答案及解析
-
下列物质不能由化合反应直接生成的是( )
A.NaOH B.Cu2(OH)2CO3 C.H2SiO3 D.FeCl2
难度: 中等查看答案及解析
-
设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.3.9 g Na2O2所含的离子数为0.15 NA
B.标准状况下,每有22.4 L Cl2溶于水,所得溶液中H+的数目为NA
C.20 g 氖气中所含分子的数目为0.5 NA
D.0.2 mol CO2与足量的 Na2O2充分反应,转移的电子总数为0.4NA
难度: 中等查看答案及解析
-
向含有下列离子的稀溶液中分别通人大量氯气后,溶液中离子个数不变的是( )
A.Fe2+ B.CO32- C.Cl- D.Na+
难度: 简单查看答案及解析
-
实验室欲用18 mol/L的浓硫酸配制90 mL 1 mol/L的稀硫酸,下列说法正确的是( )
A.用量筒量取5.0 mL的浓硫酸
B.浓H2SO4在烧杯中稀释后,立即转移至容量瓶中
C.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
D.定容时,若仰视刻度线,所配溶液浓度会偏低
难度: 中等查看答案及解析