-
有些化学反应反应速率很慢且副反应较多,测定这些反应的焓变可运用
A.阿伏加德罗定律 B.勒夏特列原理 C.盖斯定律 D.质量守恒定律
难度: 中等查看答案及解析
-
下列做法不利于环境保护的是( )
A.开发太阳能、水能、风能、地热能等新能源
B.减少资源消耗,注重资源的重复使用、资源的循环再生
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
难度: 简单查看答案及解析
-
关于吸热反应的说法,正确的是
A.凡需加热的反应一定是吸热反应 B.只有分解反应才是吸热反应
C.使用催化剂的反应是吸热反应 D.酸碱中和反应的逆反应是吸热反应
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
B.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
C.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
难度: 中等查看答案及解析
-
纯水在20℃和80℃时的pH
A.前者大 B.后者大 C.相等 D.无法确定
难度: 简单查看答案及解析
-
下图为可逆反应A(g)+2B(g)
nC(g)△H>0生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是 ( )
A.p2>p1,n<3
B.p2>p1,n>3
C.p1>p2,n<3
D.p1>p2,n>3
难度: 中等查看答案及解析
-
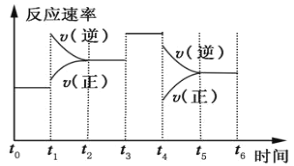
对已达化学平衡的下列反应 2X(g)+Y(g)
2Z(g),增大容积,减小压强时,对反应产生的影响是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向正反应方向移动
D.正、逆反应速率都减小,平衡向逆反应方向移动
难度: 中等查看答案及解析
-
在一定温度下的定容密闭容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)
C(g)+D(g)已达平衡的是
A.混合气体的密度 B.B物质的相对分子质量
C.混合气体的压强 D.气体的总物质的量
难度: 中等查看答案及解析
-
下列关于反应热的说法正确的是
A.已知C(石墨,s)=C(金刚石,s) △H>0,说明金刚石比石墨稳定
B.将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
2NH3(g) △H=-38.6kJ/mol
C.已知甲烷的燃烧热为890.3kJ/mol,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H = -890.3kJ/mol
D.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.4kJ/mol,则含0.5 mol NaOH的稀溶液与稀醋酸完全中和,放出热量小于28.7kJ
难度: 中等查看答案及解析
-
在3H2+N2
2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6 mol/L,在此时间内,用H2表示的反应速率为0.45 mol/(L·s),反应所经过的时间是( )
A.0.44s B.1s C.2s D.1.33s
难度: 简单查看答案及解析
-
下列物质的水溶液能导电,但属于非电解质的是( )
A.Cl2 B.CH3COOH C.SO2 D.NH4HCO3
难度: 简单查看答案及解析
-
将0.1 mol·L-1醋酸溶液加水稀释,下列说法正确的是( )
A.溶液中c(OH-)和c(H+)都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
难度: 中等查看答案及解析
-
常温下某溶液中由水电离产生的c(H+)=1×10-10 mol·L-1,则下列叙述正确的是( )
A.一定是碱溶液 B.一定是酸溶液
C.pH值一定为10 D.pH值可能为10
难度: 中等查看答案及解析
-
温度下,相同体积相同pH的盐酸和醋酸分别加水稀释,pH随溶液体积变化的曲线如图所示。下列判断正确的是( )
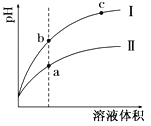
A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点Kw的数值比c点Kw的数值大
D.b点酸的总浓度大于a点酸的总浓度
难度: 中等查看答案及解析
-
已知反应:A(s)+3B(g)
2C(g)ΔH<0,在体积为10L的密闭容器中发生反应的过程如图所示:
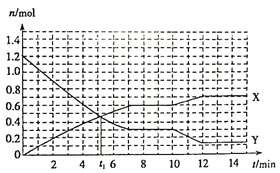
下列说法正确的是( )
A.前4 min,用A表示反应速率为υ(A)=0.005mol/(L·min)
B.X曲线表示B的物质的量随时间变化的关系
C.第t1 min时说明反应达到了平衡
D.第10 min时,可能采取了降温
难度: 简单查看答案及解析