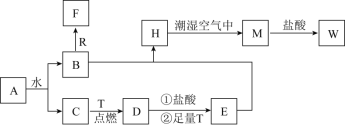
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 2.3g钠与水反应产生气体的分子数为0.1NA
B. 28gN2和CO组成的混合气体中含有的原子数为2NA
C. 0.1 mol•L﹣1Na2SO4溶液含有0.1NA个SO42﹣
D. 22.4L氯气中含有的电子总数一定为34NA
难度: 困难查看答案及解析
-
下列叙述正确的是
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合生成Na2CO3,Na2O2与CO2发生置换生成O2
③Na2O是淡黄色物质,Na2O2是白色物质
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2和Na2O焰色反应均为黄色
A. 都正确 B. ②③④⑤ C. ②③⑤ D. ④⑤
难度: 简单查看答案及解析
-
有关焰色反应的说法正确的是( )
A. 焰色反应是金属单质表现的性质
B. 焰色反应是因为发生了化学变化而产生
C. 焰色反应看到黄色火焰并不能确定该物质一定不含钾元素
D. 可用稀硫酸代替稀盐酸洗涤焰色反应中用到的铂丝
难度: 中等查看答案及解析
-
朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里......月光是隔了树照进来的,高处丛生的灌木,落下参差的斑驳的黑影......”月光穿过薄雾所形成的种种美景的本质原因是( )
A.空气中的小水滴颗粒大小约为10-9m~10-7m
B.光是一种胶体
C.雾是一种胶体
D.发生丁达尔效应
难度: 中等查看答案及解析
-
对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )
A.
 B.
B.
C.
 D.
D.
难度: 简单查看答案及解析
-
如图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是
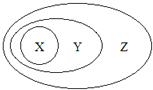
X
Y
Z
A
纯碱
盐
纯净物
B
胶体
分散系
混合物
C
Al2O3
两性氧化物
氧化物
D
单质参与反应
置换反应
氧化还原反应
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
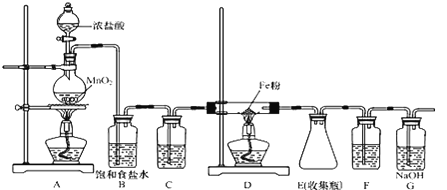
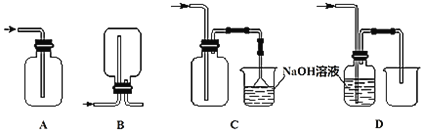
关于下列各装置图的叙述中,正确的是
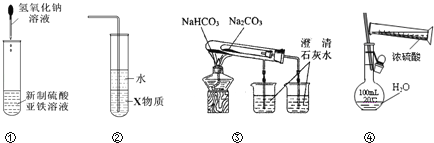
A.利用装置①可制备氢氧化亚铁并长时间观察其颜色
B.装置②中X若为四氯化碳,可用于吸收HCl气体,并防止倒吸
C.装置③验证Na2CO3和NaHCO3两种固体的热稳定性
D.通过④的方法配制一定浓度的稀硫酸溶液
难度: 中等查看答案及解析
-
下列各组离子一定能大量共存的是
A.在无色溶液中:NH4+、Fe2+、SO42-、CO32-
B.在含大量
的溶液中:Na+、CO32-、Cl-、OH-
C.在强碱性溶液中:Na+、K+、SO42-、HCO3-
D.在强酸性溶液中:K+、Fe2+、Cl-、SO42-
难度: 简单查看答案及解析
-
将金属铜、铁置于氯化铁溶液中充分反应,下列对反应情况设想的评价正确的是( )
选项
反应情况设想
评价
A
当铁、铜均不剩余时,溶液中一定有Fe2+、Cu2+,一定无Fe3+
正确,Fe3+和Fe、Cu均可反应
B
当铁、铜均有剩余时,溶液中一定有Fe2+、Cu2+,无Fe3+
正确,Fe和Cu与Fe3+都反应,故有Fe2+和Cu2+,无Fe3+
C
当铜有剩余,铁无剩余时,溶液中一定只有Fe2+,无Cu2+
正确,Cu有剩余,故无Cu2+
D
当铁有剩余,铜无剩余时,溶液中一定有Fe2+、Cu2+
不正确,不可能有Fe剩余而无Cu剩余,因为Fe比Cu优先与Fe3+反应
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
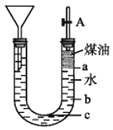
在 2L 由 NaCl、MgCl2、BaCl2 组成的混合液中,部分离子浓度大小如图所示,则此 溶液中 Ba2+的物质的量是
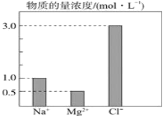
A.3.0mol B.2.0mol C.1.0mol D.0.5 mol
难度: 中等查看答案及解析
-
已知I-、Fe2+、SO2和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为H2O2<Fe2+<I-<SO2。则下列反应不能发生的是
A.2Fe3++SO2+2H2O
2Fe2++SO42-+4H+ B.H2O2+H2SO4
SO2↑+O2↑+2H2O
C.I2+SO2+2H2O
H2SO4+2HI D.2Fe3++2I-
2Fe2++I2
难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是
A.往澄清的石灰水中通入过量CO2:Ca2++ 2OH-+ CO2=CaCO3↓+ H2O
B.用小苏打(NaHCO3)治疗胃酸过多:HCO3-+ H+= H2O+ CO2↑
C.往碳酸钡中滴加稀盐酸:CO32-+2 H+= H2O + CO2↑
D.氢氧化钡溶液与稀H2SO4反应:Ba2++ SO42-+ H++ OH-= H2O+ BaSO4↓
难度: 简单查看答案及解析
-
钢铁“发蓝”是指在钢铁的表面形成一层四氧化三铁的技术过程。其中第一步反应为:3Fe+ NaNO2+ 5 NaOH= 3Na2FeO2+ H2O+ NH3↑。关于该反应说法正确的是
A.反应中N元素被氧化
B.NaFeO2既是氧化产物也是还原产物
C.整个反应过程中每有
参加反应就转移
电子
D.氧化剂与还原剂的物质的量之比为3:1
难度: 简单查看答案及解析
-
提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法为( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
难度: 中等查看答案及解析
-
通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列化学实验现象与结论对应完全正确的是
化学实验现象
解释与结论
A
钠与水反应时浮在水面上
钠与水生成的气体托举钠浮在水面上
B
铁与氯气反应剧烈燃烧产生红棕色的烟
产物为红棕色小颗粒,燃烧不一定需要氧气
C
氯水呈黄绿色
氯气与水反应生成了黄绿色物质
D
氢气在氯气中燃烧时瓶口有白雾
氯气逸出结合空气中的水蒸气而呈白雾状
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
一定量
通入某浓度的NaOH溶液中,反应后得到溶液A,向A溶液中逐滴滴入某浓度稀盐酸,加入V(HCl)与生成n(CO2)的关系如图所示。下列有关叙述正确的是
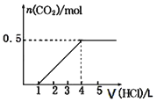
A.通入的
气体为
L
B.A溶液中既含有NaOH,又含有Na2CO3
C.A溶液中n(NaHCO3) =2 n(Na2CO3)
D.盐酸浓度为2/3
难度: 中等查看答案及解析
 D.
D.