-
“保护环境”是我国的基本国策。下列做法不应该提倡的是( )
A. 采取低碳、节俭的生活方式 B. 按照规定对生活废弃物进行分类放置
C. 深入农村和社区宣传环保知识 D. 经常使用一次性筷子、纸杯、塑料袋等
难度: 简单查看答案及解析
-
关于实验安全下列说法正确的是
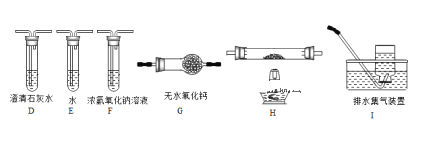
A.用排水法收集氧气时,先熄灭酒精灯,再把导气管从水槽中取出
B.在贴有此标志
 的地方,禁止吸烟
的地方,禁止吸烟C.浓硫酸不小心沾在皮肤,先用大量水冲洗,再涂上3﹪~5﹪的烧碱溶液
D.氢气点燃不会发生爆炸,所以在点燃前不需要验纯
难度: 中等查看答案及解析
-
下列实验操作中不正确的是
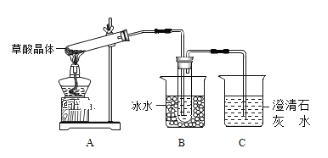
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
B.蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干
C.从碘水中萃取碘时,可以在碘水中加入CCl4为萃取剂,充分振荡萃取,静置后再分液
D.溶解操作时,玻璃棒作用是搅拌以加速溶解;过滤操作时,用玻璃棒在漏斗中轻轻搅动以加快过滤速度
难度: 中等查看答案及解析
-
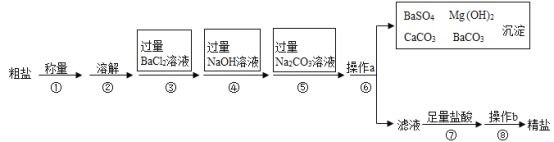
除去下列物质中的杂质(括号内为杂质),所选的试剂及操作方法均正确的一组是
选项
待提纯的物质
选用的试剂
操作的方法
A.
FeSO4(CuSO4)
水和锌粉
溶解、过滤
B.
Cu(CuO)
稀硫酸
溶解、过滤、洗涤、干燥
C.
CuSO4(H2SO4)
氢氧化钠溶液
过滤
D.
NaOH(Na2CO3)
稀盐酸
溶解、蒸发
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列说法中正确的是
A.氢原子的摩尔质量为1g B.2molO2的摩尔质量为64g·mol-1
C.3.01×1022CO2分子的质量为2.2g D.标准状况下,11.2LCCl4的质量为7.7g
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下,11.2L盐酸的原子总数为NA
B.常温常压下,14gN2含有的分子数为0.5NA
C.标准状况下,6.72L氖气中含有的分子数为0.3NA
D.常温常压下,9gH2O中含有的原子总数为1.5NA
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,1 NA 个CO2分子占有的体积为22.4L
B.常温常压下,14gN2含有原子数为0.5NA
C.常温常压下,14gCO的质子数为7NA
D.74.5 g KCl固体中含有KCl分子数为NA
难度: 中等查看答案及解析
-
下列有关仪器的使用正确的是
A.手持试管给试管内的物质加热
B.用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁
C.用天平称量药品时用手直接拿砝码
D.用燃着的酒精灯去点燃另一盏酒精灯
难度: 中等查看答案及解析
-
有关物质的量浓度配制说法正确的是
A.定容时,直接加水至刻度线,当凹液面与刻度线相切时,停止加水
B.向容量瓶中转移液体前容量瓶未烘干,所配得的浓度偏低
C.配制一定物质的量浓度的氢氧化钠溶液,移液时未冷却,所配得的浓度偏低
D.配制一定物质的量浓度的硫酸溶液,量取浓硫酸时仰视读数,所配得的浓度偏高
难度: 中等查看答案及解析
-
标准状况下,将VL A气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为
A.
B.
C.
D.
难度: 困难查看答案及解析
-
用98%的浓H2SO4(密度为1.84g/cm3)配制0.5mol/L的稀H2SO4 250 mL,按下列要求进行操作,其中操作顺序正确的是
① 用10mL量筒量取6.79mL浓硫酸 ② 用10mL量筒量取6.8mL浓硫酸 ③ 在烧杯中稀释浓H2SO4 ④反复颠倒摇匀 ⑤ 用胶头滴管加蒸馏水至刻度线 ⑥将冷却的稀硫酸溶液转入250mL容量瓶中
A.①③⑥⑤④ B.②③⑥⑤④ C.②③⑤⑥④ D.①③⑤⑥④
难度: 中等查看答案及解析
-
化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是
A.利用废弃的秸秆生产生物质燃料乙醇 B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物 D.利用蒸馏法从海水中分离出淡水
难度: 中等查看答案及解析
-
CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A.光合作用 B.自然降雨 C.化石燃料的燃烧 D.碳酸盐的沉积
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数,下列说法正确的是
A.1 mol氦气中有2NA个氦原子 B.32g氧气中含NA个氧原子
C.2 L 0.3 mol·L-1 Na2SO4溶液中含1.2 NA个Na+ D.18 gH2O中所含的电子数为8NA
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A.64 g SO2含有氧原子数为1NA
B.物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C.标准状况下,22.4 L H2O的分子数为1NA
D.标准状况下,17gOH-所含电子数和22.4LNH3所含质子数均为10NA
难度: 中等查看答案及解析
-
标准状况下,将5.6LCO2和CO混合气体,通入足量澄清石灰水中,经过滤洗涤干燥后得到10.0g固体,则混合气体中CO所占质量分数为
A.48.8% B.51.2% C.60.0% D.40.0%
难度: 困难查看答案及解析