-
当光束通过下列分散系:①有尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔效应的是( )
A.①② B.②③ C.①④ D.②④
难度: 简单查看答案及解析
-
下列说法中正确的是( )
①只要能源充足而且价格低廉,废弃物中的原子都可以成为有用物质的原料
②化学家能合成大量自然界中并不存在的新物质、新材料
③学习化学不限于书本和实验室,成功的关键在于如何激发自己对于自然现象的兴趣
④实验是学习化学、体验化学和探究化学过程的重要途径
A.③④ B.①③④ C.②③④ D.①②③④
难度: 简单查看答案及解析
-
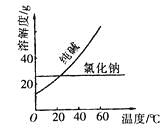
下列试剂中,标签上应标注
 和
和 的是( )
的是( )A.HNO3 B.Na2CO3 C.NaOH D.HCl
难度: 中等查看答案及解析
-
下列中草药煎制步骤中,属于过滤操作的是( )
A.冷水浸泡
B.加热煎制
C.箅渣取液
D.灌装保存
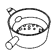
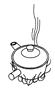


A. A B. B C. C D. D
难度: 简单查看答案及解析
-
在溶液中能大量共存,加入OH-有沉淀析出,加入H+有气体放出的是( )
A.H+、Cu2+、Cl-、CO32- B.Fe3+、K+、SO42-、NO3-
C.Ba2+、Al3+、MnO4-、SO42- D.Na+、Ca2+、Cl-、HCO3-
难度: 中等查看答案及解析
-
实验室需要用1.0 mol/LNaOH溶液480 mL进行相关的实验,下列说法正确的是( )
A.用托盘天平称取19.2 g NaOH固体配制溶液
B.用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余的液体
C.若其他操作均正确,定容时俯视刻度线将导致结果偏高
D.容量瓶中开始有少量的水可置于烘箱中烘干
难度: 中等查看答案及解析
-
进行化学实验必须注意安全,下列说法不正确的是( )
A.把盛有液体的蒸发皿直接放在铁架台的铁圈上加热
B.取用金属钠时,将切下来的碎屑放回原试剂瓶
C.CCl4萃取碘水中的I2,先从分液漏斗下口放出有机层,后从上口倒出水层
D.加热试管内物质时,试管底部与酒精灯灯芯接触
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列说法中正确的是( )
A.0.1mol/L Na2SO4溶于水中,所得溶液中Na+个数为0.2NA
B.78g Na2O2中含有离子总数为3NA
C.标准状况下,NA个水分子所占的体积为22.4L
D.Na2O2与CO2反应生成2.24L氧气转移电子数为0.2NA
难度: 简单查看答案及解析
-
从平时学生实验中我们发现,同学们在进行实验时,出现许多不正确的操作方式,希望同学们在今后的实验中,克服不规范的操作。请找出下列图示中正确的实验操作( )
A.除去CO中的CO2
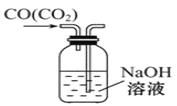 B.萃取时振荡混合液
B.萃取时振荡混合液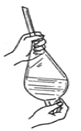 C.稀释浓硫酸
C.稀释浓硫酸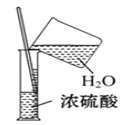 D.向试管中滴加液体
D.向试管中滴加液体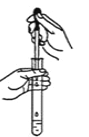
难度: 中等查看答案及解析
-
生产、生活中下列过程不涉及氧化还原反应的是 ( )
A.多吃水果(富含维生素C)美容养颜 B.铝的表面生成致密的氧化薄膜
C.久置于空气中,浓硫酸的体积增大 D.食品袋内装有还原铁粉的小袋防食品变质
难度: 简单查看答案及解析
-
下列有关0.1mol/LNaOH溶液的叙述正确的是( )
A.1L该溶液中含有NaOH40g
B.100mL该溶液中含有OH-0.01mol
C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01mol/L
D.在1L水中溶解4gNaOH即可配制得0.1mol/LNaOH溶液
难度: 中等查看答案及解析
-
某研究性学习小组参照课文中的实验装置图做高温下铁与水蒸气反应的实验装置如图所示。在玻璃管中放入铁粉与石棉绒的混合物,加热,并通入水蒸气。用试管收集产生的干燥气体,并靠近火焰点火,观察现象。下列说法错误的是( )

A.圆底烧瓶中盛装的是水,该装置受热后提供水蒸气
B.在圆底烧瓶内加入碎瓷片加快化学反应速率
C.实验时应先点燃酒精灯,后点燃酒精喷灯
D.石棉绒作铁粉的载体,防止铁粉被吹入导管而引起堵塞
难度: 中等查看答案及解析
-
黑火药是我国古代四大发明之一,黑火药燃料发生反应的化学方程式为S+2KNO3+3C
K2S+N2↑+3CO2↑.有关该反应的说法不正确的是( )
A.S、KNO3均作氧化剂 B.反应生成1molCO2转移了4mole﹣
C.参加反应的氧化剂与还原剂的物质的量之比为1:2 D.C表现出还原性
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.鉴别碳酸钠和碳酸钾可以通过焰色反应实验,焰色反应属于化学变化
B.钠投入到饱和石灰水中有金属钙被还原出来
C.铝的化学性质本不活泼,难被腐蚀
D.铝制容器不宜长时间存放酸性、碱性或咸的食物
难度: 中等查看答案及解析
-
下列反应的离子方程正确的是( )
A.硫酸铜溶液中加入氢氧化钡溶液Ba2+ + SO42-=BaSO4↓
B.过氧化钠与水反应2O22-+2H2O=4OH- + O2↑
C.铝盐溶液与氨水反应Al3+ + 3OH-=Al(OH)3↓
D.铝片与氢氧化钠溶液反应2Al + 2OH- + 2H2O=2AlO2- + 3H2↑
难度: 简单查看答案及解析
-
已知:①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O,②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O,③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4。下列结论正确的是( )
A.①②③均是氧化还原反应
B.氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2
C.反应②中氧化剂与还原剂的物质的量之比为6:1
D.反应③中0.1mol还原剂共得到电子数为6.02×1022
难度: 中等查看答案及解析