-
向体积和物质的量浓度都相等的盐酸和氢氧化钠溶液中投入足量的铝粉,放出的氢气在同温同压下的体积之比为
A. 1︰1 B. 1︰3 C. 3︰1 D. 1︰2
难度: 简单查看答案及解析
-
《本草衍义》是北宋医家寇宗爽所撰,对后世有很大影响,其中对精制砒霜过程有如下叙述:取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之,文中涉及的操作方法是
A.升华 B.蒸馏 C.蒸发 D.萃取
难度: 简单查看答案及解析
-
电解法炼铝时,冰晶石的作用是
A.助熔剂 B.催化剂 C.还原剂 D.氧化剂
难度: 简单查看答案及解析
-
下列有关物质分类或归类正确的一组是
①液氨、液氯、干冰、碘化银均为化合物②漂白粉、水玻璃、氨水、铝热剂均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质④碘酒、牛奶、豆浆、雾均为胶体
⑤NaAlO2、Na2O2、Na2CO3、Na2SiO3均为钠盐
A.①和② B.②和③ C.③和④ D.②③⑤
难度: 简单查看答案及解析
-
下列有关实验操作说法正确的是
A.用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余液体
B.实验室提取碘水中的碘可以采取加酒精进行萃取的方法
C.配制FeSO4溶液时要用加热煮沸并冷却的蒸馏水溶解绿矾,再加入一定量铁屑和稀硫酸
D.做焰色反应时需要用稀硫酸或稀盐酸洗涤铂丝
难度: 简单查看答案及解析
-
下列反应中,通过置换反应得到金属单质的是
A.钠块投入氯化铜溶液中 B.一氧化碳通过炽热的氧化铜
C.焦炭与石英混合高温加热 D.火法炼铜
难度: 简单查看答案及解析
-
设N A 代表阿伏加德罗常数的值,下列说法正确的是
A.1 mol Na在空气中完全燃烧,转移的电子数为2 N A
B.常温下,2.7 g铝与足量NaOH溶液反应,消耗0.1 N A个OH-
C.0.1 mol Fe 与足量水蒸气反应,生成H2的分子数为0.1 N A
D.11.2 L Cl2含有的原子数为N A
难度: 简单查看答案及解析
-
现有MgCl2、AlCl3、CuCl2、FeCl3、KCl五种溶液,只用一种试剂就能把它们鉴别出来,这种试剂是
A. 氨水 B. AgNO3溶液 C. NaCl溶液 D. NaOH溶液
难度: 中等查看答案及解析
-
下列实验室保存试剂的方法正确的是
A.氢氟酸存放在配有橡胶塞的玻璃瓶中
B.碳酸钠溶液或氢氧化钠溶液存放在配有磨口玻璃塞的试剂瓶中
C.氯化铁溶液存放在铜制容器中
D.氯水应保存在棕色配玻璃塞的细口瓶中
难度: 简单查看答案及解析
-
下列关于元素化合物的说法不正确的是
A.Ca(ClO)2溶液通入少量CO2,溶液变浑浊
B.向氯水加入AgNO3溶液,产生白色沉淀,证明氯水中含有Cl-
C.碳酸氢钠能与碱反应,因此可以用作食品的膨松剂
D.将铝箔在酒精灯火焰上加热,铝箔熔化但不滴落,证明氧化铝的熔点高于铝
难度: 简单查看答案及解析
-
下列各组离子能大量共存的是
A.Cu2+、Mg2+、SO42-、OH- B.Na+、H+、SO42-、ClO-
C.MnO4-、Al3+、Fe2+、SO42- D.Na+、NO3-、K+、SO42-
难度: 中等查看答案及解析
-
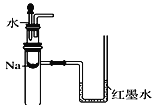
下列实验装置不能达到实验目的的是( )
A.验证Na和水反应是否为放热反应
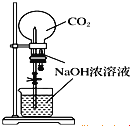
B.用CO2做喷泉实验
C.观察纯碱的焰色反应
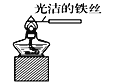
D.比较NaCO3、NaHCO3的稳定性
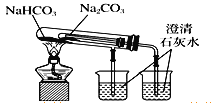
难度: 中等查看答案及解析
-
下列叙述正确的是
A.卤水点豆腐和静电除尘都应用了胶体聚沉的性质
B.工业上常利用铝热反应冶炼难熔的金属,如钒、铬、锰等
C.合金的熔点一般比组成成分的金属熔点都高
D.水泥、玻璃、陶瓷等硅酸盐工业产品的共同原料为石灰石
难度: 简单查看答案及解析
-
下列物质既能与盐酸反应,又能与烧碱溶液反应的是
①NaHSO4 ②Al ③Al(OH)3 ④ Al2O3 ⑤NaHCO3 ⑥ SiO2 ⑦(NH4)2CO3 ⑧CaCO3
A.②③④⑤⑦ B.②③④⑤⑥
C.②③④⑦⑧ D.全部都可以
难度: 简单查看答案及解析
-
实验室用足量的二氧化锰和40mL 10mol/L浓盐酸充分反应制氯气,下列说法正确的是
A.该实验中共消耗0.1 mol MnO2,生成标准状况下2.24L氯气
B.氯气有毒、有刺激性气味,常用澄清石灰水吸收多余的氯气
C.氯气可以用向下排空气法或排水法收集
D.在该反应中二氧化锰作氧化剂,浓盐酸作还原剂
难度: 中等查看答案及解析
-
下列各组物质,因反应条件(温度或者反应物用量)改变,不会引起产物改变的是
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.AlCl3和NaOH
难度: 简单查看答案及解析
-
下列各组物质中,X是主要成份,Y是少量杂质,Z是除杂所加的试剂,正确的一组是
A
B
C
D
X
Na2CO3溶液
HCl气体
Fe
CO2气体
Y
NaHCO3
Cl2
Al
HCl
Z
NaOH溶液
饱和食盐水
NaOH溶液
饱和Na2CO3溶液
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
关于反应过程中的先后顺序,下列说法正确的是
A.已知:2Fe3++2I-=2Fe2++I2,则向FeI2溶液中通入少量Cl2时,Fe2+首先被氧化
B.向Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成
C.向浓度均为0.1mol/L的Na2CO3和NaOH混合溶液中通入CO2气体,NaOH首先反应
D.向0.1mol/L FeCl3溶液中,同时加入铁和铜,铜首先参加反应
难度: 中等查看答案及解析
-
下列实验“操作和现象”与“结论”对应关系正确的是
选项
实验操作及现象
实验结沦
A
向酸性KMnO4溶液中滴加双氧水,紫色消失
H2O2具有氧化性
B
氯气通入紫色石蕊试液中,溶液先变红后褪色
氯水有酸性,氯气有漂白性
C
将NaOH溶液滴加到饱和FeC13溶液中呈红褐色
制Fe(OH)3胶体
D
向Fe2(SO4)3溶液中加入铜粉,固体溶解,溶液变蓝
Fe3+氧化性强于Cu2+
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
溶解34.6g碳酸铜和碱式碳酸铜的混合物,消耗1mol/L盐酸600mL。灼烧等质量的上述混合物,得到氧化铜的质量是
A.30g B.24g C.20g D.12g
难度: 中等查看答案及解析
-
在Fe2(SO4)3和CuSO4的混合液中逐渐加入铁粉,溶液中Fe2+的物质的量浓度和加入铁粉的物质的量之间关系如图所示。则该溶液中Fe2(SO4)3与CuSO4的物质的量浓度之比为

A.3∶1 B.1∶2 C.2∶1 D.1∶1
难度: 中等查看答案及解析
-
二氧化硅又称硅石,是制备硅及含硅化合物的重要原料。部分转化过程如图所示,下列说法正确的是
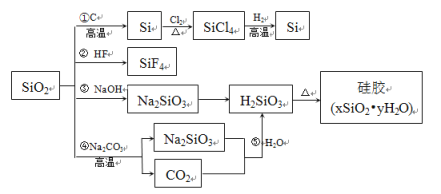
A.SiO2既能发生②反应,又能发生③反应,说明SiO2属于两性氧化物
B.④反应是水泥工业的化学反应原理之一,⑤反应可证明H2CO3酸性强于H2SiO3
C.①反应的生成物除Si外还有CO2,硅胶可用作催化剂的载体
D.除了粗硅的制备和提纯过程中涉及的反应外,图中所示其他反应都是非氧化还原反应
难度: 中等查看答案及解析