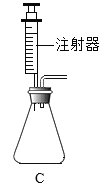
-
下列物质的性质与应用对应关系正确的是
A. 小苏打能与酸反应,可用作治疗胃酸过多的药剂
B. 氮气熔沸点低,可用作保护气
C. 碳酸氢铵受热易分解,可用作氮肥
D. 铝片有金属光泽,可用作导电材料
难度: 中等查看答案及解析
-
下列实验现象描述正确的是
A. 打开浓盐酸、浓硫酸的试剂瓶,瓶口都看到白雾
B. 铁丝在纯氧中燃烧,火星四射,生成黑色固体四氧化三铁
C. 实验室电解水,正负极产生的气体体积比约为2:1
D. 灼烧鸡蛋清,产生烧焦羽毛的特殊气味
难度: 中等查看答案及解析
-
下列说法正确的是
A. 天然气可以作燃料 B. 过滤可以将硬水软化
C. 水由氢气和氧气组成 D. 大量施用化肥、农药不会污染环境
难度: 中等查看答案及解析
-
“绿水青山就是金山银山”,下列措施或行为不利于留住“绿水青山”的是:( )
A.工业废水处理达标后再排放 B.农业上合理使用化肥和农药
C.生活污水实现集中处理和排放 D.固体垃圾直接倒入江河
难度: 简单查看答案及解析
-
下列有关说法错误的是
A.水的三态变化说明分子间具有间隙 B.原子不显电性是因为原子中质子数与中子数相等
C.五个二氧化硫分子可表示为5SO2 D.Al3+可表示一个铝离子带三个单位的正电荷
难度: 简单查看答案及解析
-
新冠肺炎这一公共卫生事件让人们更注重卫生习惯。例如:生活中常有揭开盖子(塞子)的动作,如茶杯盖子、锅盖、酒瓶、饮料瓶的盖子等,这些盖子取下后像试剂瓶盖一样,应该怎样放在桌面上才符合良好的卫生习惯( )
A.侧放 B.正放 C.随意放 D.倒放
难度: 简单查看答案及解析
-
下列实验基本操作正确的是( )
A.取用固体药品
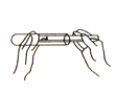
B.加热液体
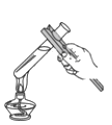
C.振荡试管
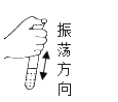
D.连接仪器
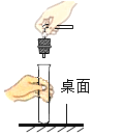
难度: 简单查看答案及解析
-
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
代表一个碳原子,
代表一个氢原子,
代表一个氧原子。下列说法不正确的是( )

A.一个乙酸分子由两个碳原子、四个氢原子和两个氧原子构成
B.乙酸中氧元素与氢元素的质量比为8:1
C.乙酸中碳元素的质量分数为41%
D.乙酸燃烧的产物可能是二氧化碳和水
难度: 简单查看答案及解析
-
推理是一种重要的化学思维方法,但推理必须科学、严谨。下列推理不正确的是( )
A.若测得某雨水的pH<7,则该雨水不一定是酸雨
B.复分解反应中反应物和生成物都是化合物,反应物和生成物都是化合物的反应不一定是复分解反应
C.二氧化碳能使燃着的木条熄灭,能使燃着的木条熄灭的气体不一定是二氧化碳
D.活泼金属与酸反应有气体产生,则与酸反应产生气体的物质一定是活泼金属
难度: 简单查看答案及解析
-
下图是某化学反应的微观示意图。下列说法中正确的是 ( )
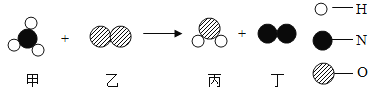
A.丙物质含有3个原子 B.物质乙、丙都属于氧化物
C.该反应前后,原子的种类不变 D.该反应属于化合反应
难度: 简单查看答案及解析
-
甲、乙两种物质的溶解度曲线如图。下列说法正确的是( )

A.常温下,物质乙易溶于水 B.甲的溶解度大于乙的溶解度
C.t1℃时,两种溶液中溶质的质量分数一定相等 D.当乙中混有少量的甲时,可以采用降温结晶的方法提纯乙
难度: 简单查看答案及解析
-
某无色溶液中主要含四种离子,已知其中三种为
、
、
,则另一种离子可能是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列实验操作中不能达到实验目的是( )
选项
物质
目的
主要实验操作
A
CO2和N2
鉴别
分别通入澄清石灰水,观察现象
B
NaOH固体中含有Na2CO3
检验
取样,配成溶液加入少量盐酸,观察现象
C
KCl和MnO2的混合物
分离
溶解、过滤,蒸发结晶,固体洗涤并烘干
D
CaCl2溶液混有HCl杂质
除杂
先加入过量的碳酸钙固体反应后过滤
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列归纳总结不完全正确的一组是( )
A.物质构成
B.化学与生活
①氧气是由分子构成的
②水银是由原子构成的
③食盐是由离子构成的
①
与
不能大量共存,“钡餐”服BaSO4
②缺铁会贫血
③缺维生素A会得夜盲症
C.物质分类
D.油污处理
①合金属于混合物
②纯碱属于氧化物
③干冰属于有机物
①汽油除油污是溶解原理
②洗涤剂除油污是乳化原理
③炉具清洁剂用于除油污
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在今年初中化学实验操作考查中,甲同学用高锰酸钾来制取氧气,加热一段时间后,称得试管里剩余固体的质量为6g,该同学继续加热剩余固体至不再有气体产生时,冷却后向试管中加入足量的水溶解,过滤,洗涤,烘干得滤渣为1.74g。则在6g剩余固体中钾元素的质量分数为( )
A.25% B.26% C.40% D.52%
难度: 简单查看答案及解析