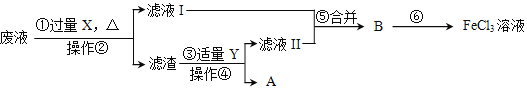
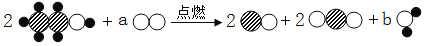-
下列有关化学史的说法中错误的是( )
A.门捷列夫发表元素周期表
B.卢瑟福提出原子的核式结构模型
C.拉瓦锡发现氧气约占空气的1/5体积
D.诺贝尔提出质量守恒定律
难度: 简单查看答案及解析
-
面粉中富含的营养素是( )
A. 维生素 B. 油脂 C. 蛋白质 D. 糖类
难度: 简单查看答案及解析
-
“绿水青山就是金山银山”,下列做法与该主题不相符的是
A.开发清洁能源 B.大量使用农药 C.垃圾分类回收 D.倡导公交出行
难度: 简单查看答案及解析
-
能保持氢气化学性质的微粒是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
生活中下列物质,能使无色酚酞试液变红的是
A.食盐水 B.白醋 C.蒸馏水 D.肥皂水
难度: 简单查看答案及解析
-
下列化学实验操作正确的是
A.将浓硫酸缓慢加入水中,边加边用玻璃棒搅拌 B.用10mL的量筒量取9.75mL的液体
C.加热后的试管立即用冷水冲洗 D.用嘴吹灭酒精灯
难度: 简单查看答案及解析
-
“我是碳家族的大女儿,让大地充满生机、让地球因我而温暖;我调皮可爱,钻进石灰灰水,搅得人家不安宁;我藏在汽水里,小朋友喝了直打隔。”这里叙述中的“我”是指
A.二氧化碳 B.氧气 C.氮气 D.一氧化碳
难度: 简单查看答案及解析
-
下列物质的用途是利用其物理性质的是
A. 金刚石用于切割玻璃 B. 小苏打用于治疗胃酸过多
C. 一氧化碳用于冶炼金属 D. 食品包装中充氮气用于防腐
难度: 简单查看答案及解析
-
水是生命之源。下列“水”属于纯净物的是( )
A. 海水 B. 蒸馏水 C. 矿泉水 D. 雨水
难度: 简单查看答案及解析
-
下列措施中,不能防止金属制品锈蚀的是( )
A. 在表面刷漆 B. 在表面涂油 C. 在表面镀铬 D. 用湿布擦拭
难度: 简单查看答案及解析
-
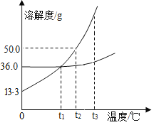
下列说法中,正确的是
A.在同一温度下,同一物质的饱和溶液一定比不饱和溶液所含溶质多
B.同一温度下,任何饱和溶液一定比不饱和溶液溶质质量分数大
C.硝酸钾的饱和溶液一定比它的不饱和溶液溶质质量分数大
D.在同一温度下,氯化钠的饱和溶液一定比它的不饱和溶液溶质质量分数大
难度: 简单查看答案及解析
-
在指定条件下,下列物质间的转化不能一步实现的是
A.S
SO3 B.CO2
O2 C.Fe3O4
Fe D.Ca(OH)2
NaOH
难度: 简单查看答案及解析
-
下列探究燃烧条件的实验中,只能得出“燃烧需要温度达到可燃物的着火点”的是( )
A.
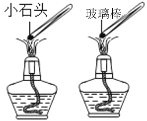 B.
B.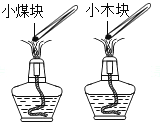
C.
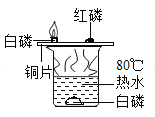 D.
D.
难度: 简单查看答案及解析
-
《新型冠状病毒感染的肺炎诊疗方案(试行第三版)》中提到可试用利托那韦进行抗病毒治疗,利托那书的化学式为C37H48N6O5S2,下列说法中正确的是
A.利托那韦是由5种元素组成的混合物 B.每个利托那韦分子中含37个碳元素
C.利托那韦的相对分子质量为720 D.利托那韦中氢元素的质量分数最高
难度: 简单查看答案及解析
-
除去下列物质中的少量杂质(括号内为杂质)的方法错误的是
A.O2(H2O)一用生石灰 B.CaCO3粉末(Na2CO3)一加水过滤、洗涤,干燥
C.CO2(CO)一点燃 D.KCl溶液(K2CO3)一加适量盐酸、蒸发
难度: 简单查看答案及解析
-
下列四种离子在水中能大量共存,且形成无色溶液的是
A.Cu2+ SO42- Na+ Cl- B.H+ Na+ K+ NO3- C.H+ Ca2+ NO3- CO32- D.Mg2+ Cl- OH- Na+
难度: 简单查看答案及解析
-
逻辑推理是学习化学常用的思维方法,下列推理正确的是
A. 原子是不带电的粒子,所以不带点的粒子一定是原子
B. 溶液时均一稳定的,所以均一稳定的混合物一定是溶液
C. 单质只含一种元素,所以含一种元素的物质一定是单质
D. 碱中含有氢元素和氧元素,所以含有氢元素和氧元素的物质一定是碱
难度: 中等查看答案及解析
-
实验室欲将80g溶质质量分数为25%的糖溶液浓度增大至50%,简单易行的方法是
A.恒温蒸发40g水 B.恒温蒸发25g水 C.再溶解48g糖 D.再溶解20g蔗糖
难度: 简单查看答案及解析
-
中和反应是一类重要的化学反应。用pH和温度传感器研究稀盐酸与氢氧化钠溶液反应的过程,测量反应过程中相关物理量的变化情况,得到下面两张图。下列说法错误的是
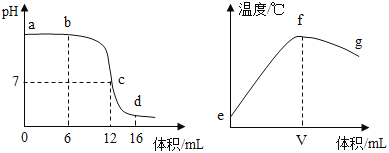
A.b点所示溶液中的溶质是NaCl和NaOH
B.c→d所示溶液中NaCl的质量不再增加
C.e→f变化趋势可说明该反应是放热反应
D.从变化趋势看,b点和f点存在对应关系
难度: 中等查看答案及解析
-
电解法是工业炼铜的主要方法,化学方程式为2CuSO4+2H2O
2Cu↓+O2↑+2H2SO4,取一定质量的硫酸铜溶液,在实验室中模拟工业条件进行电解,当硫酸铜恰好完全反应时,得到488.0g溶液和9.6g铜(注:本题不考虑气体在溶液中的溶解)。向电解后得到的488.0g溶液中加入一定量的某物质,充分反应后,所得溶液的质量,溶质量分数均与原硫酸铜溶液相同,则这种物质可能是下列物质中的
①Cu ②CuO ③CuCO3 ④Cu(OH)2
A.①② B.②③ C.②④ D.③④
难度: 中等查看答案及解析