-
下列关于物质用途的描述不正确的是
A. 氧气可用作燃料 B. 二氧化碳可用作气体肥料
C. 干冰可用于人工降雨 D. 铜丝可用作导线
难度: 中等查看答案及解析
-
今年诺贝尔化学奖授予了在开发锂离子电池方面作出贡献的科学家。钴酸锂(LiCoO2)是锂电池中的常见材料,其中锂(Li)的化合价为+1,求钴(Co)元素的化合价
A.﹣3 B.+ 1 C.﹢2 D.﹢3
难度: 简单查看答案及解析
-
下列实验方法能达到实验目的的是
选项
实验目的
实验方法
A
检验一瓶O2是否收集满
将带火星的木条伸入瓶中
B
鉴别H2 和CH4
分别点燃,在火焰上方罩一干冷烧杯
C
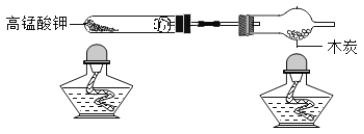
证明燃烧的条件之一是可燃物与氧气接触
将白磷放入80℃热水中,不燃烧,通入氧气后白磷燃烧
D
比较Fe、Cu、Ag的金属活动性
将Fe和Cu分别放入AgNO3溶液中
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
玻璃棒不可用来
A.蘸取溶液测定其酸碱度 B.过滤时引流液体注入漏斗
C.搅拌漏斗中的浑浊液,加快过滤速度 D.搅拌烧杯中的溶液,加速溶解
难度: 简单查看答案及解析
-
下列现象,属于化学变化的是()
A.电灯发光 B.自行车车胎爆裂 C.饭菜变馊 D.玻璃破碎
难度: 简单查看答案及解析
-
下列化学方程式4NH3+3O2
2X+6H2O中X的化学式是
A.N2 B.NO C.NO2 D.N2O
难度: 简单查看答案及解析
-
下列操作不正确的是( )
A.
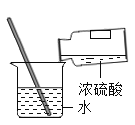 稀释 B.
稀释 B.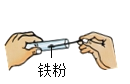 取药 C.
取药 C. 称量 D.
称量 D.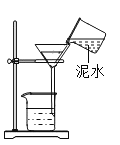 过滤
过滤难度: 简单查看答案及解析
-
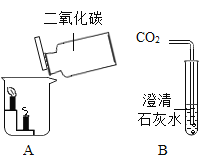
鉴别空气、氧气和二氧化碳3瓶气体最合理的方法是( )
A.闻气味 B.将集气瓶倒扣在水中
C.观察颜色 D.将燃着的木条伸入集气瓶中
难度: 中等查看答案及解析
-
推理是学习化学常用的思维方法,下列推理正确的是( )
A. 在化学变化中原子不能再分,所以在化学变化中离子也不能再分
B. 洗涤剂除油污的原理是乳化,所以氢氧化钠除油污的原理也是乳化
C. CO2使饱和石灰水变浑浊是化学变化,所以升温使饱和石灰水变浑浊也是化学变化
D. 化合物是由不同种元素组成的物质,所以由同种元素组成的物质一定不是化合物
难度: 中等查看答案及解析
-
如图是a、b两种固体物质的溶解度曲线,下列说法中不正确的是( )
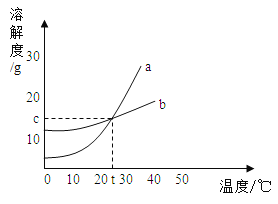
A.a的溶解度大于b的溶解度
B.在t℃时,a、b饱和溶液中溶质的质量分数相同
C.当a中含有少量b时,可以用降温结晶法提纯a
D.a,b都属于易溶物质
难度: 中等查看答案及解析
-
氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下。下列说法不正确的是( )
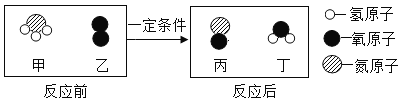
A. 甲中氮、氢原子个数比为1:3 B. 乙的相对分子质量为32
C. 两种生成物均为化合物 D. 生成的丙与丁的分子个数比为1:2
难度: 简单查看答案及解析
-
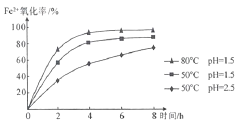
为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
图象
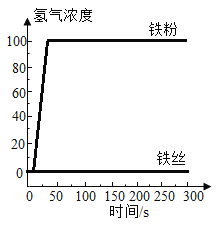 图1
图1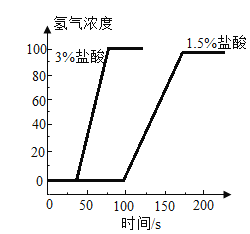 图2
图2 图3
图3实验
等质量的铁丝、铁粉分别与相同浓度的盐酸反应
等质量的铁粉分别与不同浓度的盐酸(3%和15%)反应
不同温度下,等质量的铁粉与相同浓度的足量稀盐酸反应
A.由图1可知:盐酸不能与铁丝反应
B.由图1可得结论:铁粉反应更快
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
难度: 困难查看答案及解析