-
下列物质露置在空气中一段时间后,因为发生化学变化而质量增加的是( )
A.浓硫酸 B.浓盐酸 C.氢氧化钠 D.石灰石
难度: 中等查看答案及解析
-
下列人体所必需的元素中,缺乏会导致骨质疏松、佝偻病的是
A. 铁 B. 碘 C. 锌 D. 钙
难度: 简单查看答案及解析
-
下列肥料属于氮肥的是
A.CO(NH2)2 B.Ca(H2PO4)2 C.KCl D.K2CO3
难度: 简单查看答案及解析
-
生活中的下列物质,属于溶液的是
A.豆浆 B.牛奶 C.蔗糖水 D.蒸馏水
难度: 简单查看答案及解析
-
氢氧化钙的俗名是
A. 消石灰 B. 苛性钠 C. 石灰石 D. 生石灰
难度: 简单查看答案及解析
-
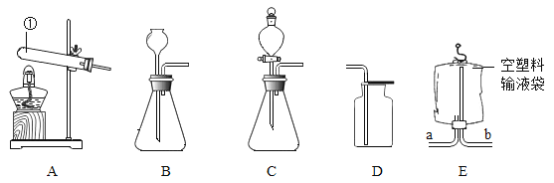
下图所示的实验操作中,正确的是
A.
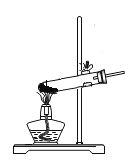 加热高锰酸钾制取氧气 B.
加热高锰酸钾制取氧气 B.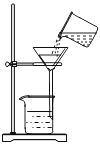 过滤
过滤C.
配制溶液 D.
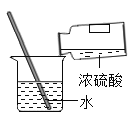 稀释浓硫酸
稀释浓硫酸难度: 简单查看答案及解析
-
硫代硫酸钠,又名大苏打,化学式为Na2S2O3,其中S元素的化合价是
A.+2 B.+4 C.+6 D.-2
难度: 简单查看答案及解析
-
下列有关溶液的说法正确的是
A.溶液都是无色的、透明的 B.水是最常用的溶剂
C.形成溶液的溶质都是固体 D.同种溶质的饱和溶液一定比不饱和溶液的浓度大
难度: 简单查看答案及解析
-
灰水粽是广西特产之一,灰水的主要成分是碳酸钾。碳酸钾属于
A.盐 B.碱 C.单质 D.氧化物
难度: 简单查看答案及解析
-
分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
难度: 简单查看答案及解析
-
如图进行金属片互相刻画实验,下列说法正确的是
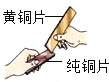
A.该实验过程中,铜片发生了化学变化
B.该实验过程中,铜原子之间的间隔变大
C.该实验说明:铜是由铜分子组成的
D.该实验说明:黄铜片的硬度比纯铜片大
难度: 简单查看答案及解析
-
氢氧化钠和氢氧化钙都是常见的碱。下列关于它们的说法中,正确的是
A.都能用作建筑材料 B.都能用作某些气体的干燥剂
C.它们的溶液都能与碳酸钾溶液反应 D.它们的溶液都能使无色酚酞溶液变红
难度: 简单查看答案及解析
-
下列关于稀盐酸化学性质的描述中,不属于酸的共同性质的是( )
A.能与氧化铝反应生成盐和水
B.能使石蕊试液变红色
C.能与氢氧化钠反应生成水
D.能与AgNO3溶液反应生成白色沉淀
难度: 简单查看答案及解析
-
在“粗盐中难溶性杂质去除”实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
难度: 中等查看答案及解析
-
下列化学方程式符合题意且书写正确的是
A.正常雨水偏弱酸性原因:SO3+H2O= H2SO4
B.实验室用酒精作燃料:C2H5OH+3O2
2CO2+3H2O
C.用小苏打治疗胃酸过多症:NaHCO3+HCl= NaCl+CO2+H2O
D.工业上用熟石灰制烧碱:Ca(OH)2+2NaNO3= Ca(NO3)2+2NaOH
难度: 简单查看答案及解析
-
已知反应:Mn + FeCl2 = MnCl2 + Fe,下列说法错误的是
A.可以用锰制的容器盛装硫酸铜溶液 B.锰的金属活动性比铁的强
C.锰可以与稀盐酸反应放出气体 D.锰可以与硝酸银溶液发生置换反应
难度: 中等查看答案及解析
-
只用一种试剂就可一次性鉴别稀硫酸、烧碱溶液、食盐溶液的是
A.纯碱溶液 B.酚酞试液 C.石蕊试液 D.稀盐酸
难度: 中等查看答案及解析
-
如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
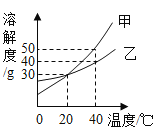
A.20 ℃时,甲、乙两种固体物质的溶解度都是30
B.40 ℃时,甲物质饱和溶液的溶质质量分数为50%
C.将130 g 20 ℃时甲的饱和溶液升温到40 ℃,最多还能溶解甲物质20 g
D.40 ℃时,将50 g乙物质溶于100 g水中,恰好能得到150 g乙的饱和溶液
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的的是
选项
实验目的
实验操作
A
除去铁粉中少量的铜粉
加入足量稀硫酸
B
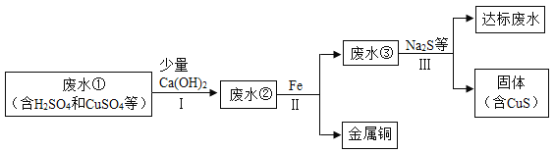
除去CuSO4溶液中的少量FeSO4
加入足量的铜粉
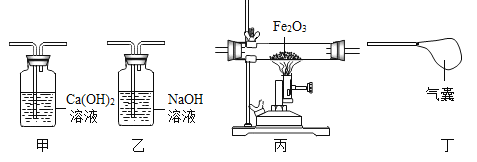
C
鉴别澄清石灰水和NaOH溶液
加入稀盐酸
D
鉴别硬水和软水
加入肥皂水
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列图像不能正确反映对应实验过程中相关量的变化的是
A.
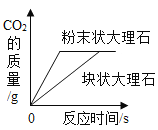 将等质量、形态不同的大理石分别与足量质量分数相同的稀盐酸反应
将等质量、形态不同的大理石分别与足量质量分数相同的稀盐酸反应B.
一定压强下,氧气的溶解度受温度影响的变化曲线
C.
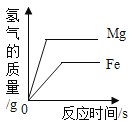 等质量的镁粉和铁粉与足量同浓度的稀盐酸反应
等质量的镁粉和铁粉与足量同浓度的稀盐酸反应D.
向盐酸中加入水稀释
难度: 困难查看答案及解析