-
恩格斯指出“劳动创造了人本身”。下列人们的劳动中,不涉及化学变化的是( )。
A.粮食酿酒 B.海水晒盐 C.伐薪烧炭 D.湿法冶金
难度: 简单查看答案及解析
-
每年4月22日是世界地球日,旨在唤起人类爱护地球、保护家园的意识,促进资源开发与环境保护的协调发展,进而改善地球的整体环境。下列有关说法错误的是( )。
A.未经处理的工业废水、农业废水及生活污水随意排放,会污染水体
B.为减少或消除煤炭燃烧产生的二氧化硫,向煤炭中加入石灰石作固硫剂
C.为保持住宅小区整洁,将其中散落的塑料袋、树叶等杂物集中焚烧
D.为提高农作物产量并减少对环境的污染,应该合理使用农药和化肥
难度: 简单查看答案及解析
-
每年5月第三周是中国的全民营养周。“全民营养周”旨在传播核心营养知识,提高健康素养,建立营养新生活,让营养意识和健康行为代代相传,实现“营养梦、健康梦、中国梦”。下列有关说法不正确的是( )。

A.亚硝酸钠常用作食品发色剂和防腐剂,可在食品中大量使用
B.我们应当妥善保存食物,不吃霉变或超过保质期的食物
C.健康饮食金字塔可以指导民众合理膳食营养,保持身体健康
D.人体中钙、铁、碘元素缺乏或过量均会引发疾病,应合理摄取
难度: 简单查看答案及解析
-
现有一包可溶性固体粉末,若要检验该物质的酸碱性,下列有关操作错误的是( )。
A.取少量固体样品
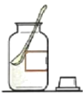 B.加适量水溶解
B.加适量水溶解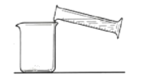
C.搅拌加速溶解
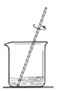 D.取样测酸碱性
D.取样测酸碱性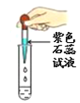
难度: 简单查看答案及解析
-
铝—石墨烯电池是浙江大学高分子科学与工程学系近期研制出的一种新型电池,它具有耐高温、抗严寒、柔性好等令人惊讶的特性,能在1.1秒内完成充电。根据如图信息,判断下列有关说法中不正确的是( )。

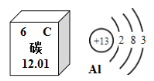
A.碳元素属于非金属元素
B.碳原子的相对原子质量为12.01
C.铝原子的质子数为13
D.铝原子在化学变化中易得电子变成阳离子
难度: 简单查看答案及解析
-
下列做法中,不符合安全要求的是( )。
A.居室里煤炉取暖,保持通风预防CO中毒
B.厨房里油锅着火,锅盖盖灭或放入青菜等食材
C.加油站严禁吸烟,避免一切明火及静电火花
D.实验室稀释浓硫酸,将水直接倒入浓硫酸中
难度: 简单查看答案及解析
-
下列有关物质变化规律、研究方法的说法中,不正确的是( )。
A.水的天然循环是通过其三态变化实现的
B.物质发生化学变化时,通常伴随着能量的变化
C.通过测定两种不同浓度的盐酸的pH,可以比较它们的酸性强弱
D.向纯碱溶液中滴加无色酚酞试液,溶液变成红色,说明纯碱属于碱
难度: 中等查看答案及解析
-
生活离不开化学,化学服务于生活。下列相关解释和判断中,不正确的( )。
A.生活中可用肥皂水鉴别硬水和软水,常用加热煮沸的方法将硬水软化
B.将0.9g NaCl溶于100g水中,配制成溶质质量分数为0.9% 的生理盐水
C.侯德榜创立侯氏制碱法,优化了纯碱制取工艺,同时得到铵态氮肥氯化铵
D.口罩中的熔喷布,是由聚丙烯((CH2CHCH3)n)超细纤维制成,属于有机高分子材料
难度: 中等查看答案及解析
-
通过对宏观现象的观察、思考、推理,构建起对微观粒子的认知,是化学学科的重要特点之一。下列有关说法中,不正确的是( )。
A.春天里柳絮漫天飞扬,因为分子在不断地运动
B.过氧化氢分解产生水是化学变化,因为分子种类发生了改变
C.盐酸和硫酸具有相似的化学性质,因为它们溶于水时都能解离出氢离子
D.固态碘和气态碘都能使淀粉变蓝色,因为分子相同化学性质相同
难度: 简单查看答案及解析
-
酸雨能酸化土壤、污染水体、腐蚀建筑及文物古迹、加速金属制品的锈蚀,已成为全球性灾害。酸雨形成的原因主要有两种:①3NO2 + H2O = 2HNO3 + X ② 2SO2 + O2 + 2H2O = 2H2SO4 。下列有关说法中,不正确的是( )。
A.反应①中X的化学式为NO
B.反应②既是化合反应,也是氧化反应
C.反应①、②中共涉及6种氧化物
D.SO2和氮氧化物是导致酸雨的“元凶”
难度: 中等查看答案及解析
-
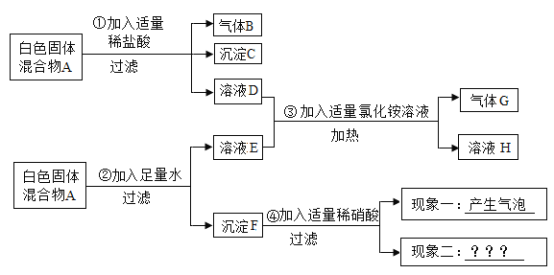
取某单一成分的溶液X三等份,分别加入到足量的硝酸铵溶液、碳酸钠溶液和硫酸镁溶液中,充分振荡,产生的现象如下表所示,则下列有关说法不正确的是 ( )。
加入物质
硝酸铵溶液
碳酸钠溶液
硫酸镁溶液
实验现象
产生刺激性气味的无色气体
生成白色沉淀
生成白色沉淀
A.该溶液X一定呈碱性 B.与硝酸铵反应生成的气体通入无色酚酞试液,酚酞溶液变红色
C.该溶液X中可能含有Ca2+ D.与硫酸镁反应生成的沉淀加入稀硝酸无任何变化
难度: 中等查看答案及解析