-
宏观辨识与微观探析是化学学科的核心素养之一。用分子、原子的观点解释下列现象,其中不合理的是( )
A. 水结成冰﹣﹣分子停止运动
B. 电解水生成氢气和氧气﹣﹣分子本身发生变化
C. 气体可以压缩储存在钢瓶中﹣﹣分子间有间隔
D. 1滴水中大约有1.67×1021个水分子﹣﹣分子很小
难度: 简单查看答案及解析
-
2020 年 3 月 22 日是第二十八届“世界水日”。今年“世界水日”的主题是“Water and climate Change”(水与气候变化)。下列做法有利于保护环境的是
A.为了粮食增产,大量使用农药化肥 B.大量使用塑料制品,减少森林开发
C.回收植物秸秆,加工生产生物柴油 D.为了保护环境,大量开采化石燃料
难度: 简单查看答案及解析
-
下列古代生产工艺中属于物理变化的是
A.纺纱织布 B.烧制瓷器 C.钢铁冶炼 D.粮食酿酒
难度: 简单查看答案及解析
-
调味剂是重要的食品添加剂。将下列调味剂加入水中,不能形成溶液的是
A.味精 B.胡椒粉 C.蔗糖 D.食盐
难度: 简单查看答案及解析
-
下列化学用语书写正确的是
A.银元素:Hg B.两个氢分子:2H
C.亚硫酸钠中硫元素的化合价:
D.一个铝离子:Al3+
难度: 简单查看答案及解析
-
下列实验操作中,正确的是
A.
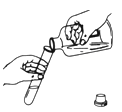 倾倒液体 B.
倾倒液体 B.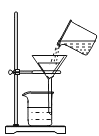 过滤
过滤C.
 称量氢氧化钠 D.
称量氢氧化钠 D.量取水的体积
难度: 简单查看答案及解析
-
下列有关实验现象的描述,正确的是
A.硫在空气中燃烧发出蓝紫色火焰
B.细铁丝在空气中燃烧,火星四射
C.酚酞溶液滴加到碳酸钠溶液中,溶液变红
D.打开浓盐酸的试剂瓶盖时,瓶口有白烟产生
难度: 简单查看答案及解析
-
下列关于家庭小实验的说法正确的是
A.用食品级的小苏打和柠檬酸等可自制汽水
B.用淬火后的钢针制钓鱼钩
C.用加热的方法修补电木等热固性塑料
D.用 10%的盐酸溶液可制叶脉书签
难度: 简单查看答案及解析
-
苹果酸(C4H6O5)是一种白色晶体,有较强的吸湿性,易溶于水、乙醇,有特殊愉快的酸味,主要用于食品和医药行业。下列关于苹果酸的说法中正确的是
A.苹果酸中有 4 个碳原子、6 个氢原子、5 个氧原子
B.苹果酸中氧元素的质量分数最大
C.苹果酸中 C、H、O 三种元素质量比为:4∶6∶5
D.苹果酸的相对分子质量为 134g
难度: 简单查看答案及解析
-
善于归纳知识,有利于培养素质。下列知识整理的内容完全正确的一组是
A.化学与生活
B.化学中常见的“三”
①除锈迹—用醋酸
②去餐具油污—用洗洁精乳化
③硬水软化—用肥皂水
①工业上的三大化石燃料—煤、石油、天然气
②三大合成材料—合金、合成纤维、合成橡胶
③三种还原性物质—碳、氢气、一氧化碳
C.化学与健康
D.化学概念中的不一定
①人体缺乏维生素C—引起夜盲症
②人体摄入过量食盐—引起高血压
③人体缺铁—引起贫血
①酸性溶液不一定是酸溶液
②生成盐和水的反应不一定是中和反应
③由同种元素组成的物质不一定是单质
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
a、b、c 三种固体物质的溶解度曲线如图所示,下列叙述正确的是

A.a 物质的溶解度大于 b 物质的溶解度
B.a、c 两种物质的饱和溶液降温均能析出晶体
C.t2℃时,等质量 a 和c 溶于水形成饱和溶液,则所需水的质量为:a﹤c
D.将t2℃的a、b、c 三种物质的饱和溶液降温到t1℃,所得溶液溶质质量分数的关系为 b>a=c
难度: 简单查看答案及解析
-
某同学梳理了以下知识:①盐中都含有金属元素;②物质发生化学变化时一定放热;③分子可分,原子不可分;④能使紫色石蕊试液变红色的一定是酸溶液;⑤炼钢、气焊常用 CO;⑥用湿润的 pH 试纸测定醋酸溶液的 pH,会使得 pH 偏大。其中正确的个数是
A.1 个 B.2 个 C.3 个 D.4 个
难度: 简单查看答案及解析
-
分离、提纯、除杂、鉴别是基本的实验技能,下列实验设计能达到实验目的的是
选项
实验目的
实验设计
A
除去 CO2 中混有的少量 CO
通过足量 NaOH 溶液后,干燥,收集气体
B
分离铜粉和铁粉的混合物
加入足量稀硫酸充分反应后,过滤、洗涤、干燥
C
提纯混有少量 Ca(OH)2 的 KOH 溶液
加入过量 K2CO3 溶液,振荡、静置、过滤
D
鉴别 CaCO3、NaOH、NaCl 固体
分别加入等量的水,观察并感知温度变化
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在给定条件下,下列物质间的转化不能一步实现的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
乙醇在常温常压下是一种易燃、易挥发的无色透明液体。现将 4.6gC2H5OH 与一定量的氧气置于密闭容器中,通过电火花点火,乙醇完全反应,容器内具体数值见下表。根据表格提供的数据, 下列说法错误的是
C2H5OH
O2
CO2
M
H2O
反应前质量(g)
4.6
a
0
0
0
反应后质量(g)
0
0
4.4
b
c
A.c 的数值为 5.4
B.M 中一定有碳元素
C.当 a≧9.6 时,产物中将不会有 M
D.当 a 的值在合理范围内发生变化时,b、c 的值也随之变化
难度: 简单查看答案及解析