-
同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是( )
A.2A(l)+B(l)=2C(g) ΔH1
B.2A(g)+B(g)=2C(g) ΔH2
C.2A(g)+B(g)=2C(l) ΔH3
D.2A(l)+B(l)=2C(l) ΔH4
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.石油经过分馏及裂化等工序得到的物质均为纯净物
B.乙酸乙酯、油脂、葡萄糖、蛋白质均可以发生水解反应
C.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
D.苯不能使酸性高锰酸钾溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
难度: 简单查看答案及解析
-
为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入的一种试剂是( )
A.NaOH B.Na2CO3 C.氨水 D.MgO
难度: 中等查看答案及解析
-
下列烷烃的系统命名正确的是( )
A.2-乙基丁烷 B.3,3-二甲基丁烷
C.2-甲基-4-乙基庚烷 D.3-乙基-2,3-二甲基戊烷
难度: 中等查看答案及解析
-
下列有关H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ·mol-1的离子反应说法正确的是( )
A.代表所有的酸碱中和反应
B.反应物一定是强酸与强碱
C.强酸与强碱的中和反应都可以这样表示
D.代表稀的强酸与稀的强碱反应生成1mol液态水时,放出热量57.3kJ
难度: 困难查看答案及解析
-
化学反应经常伴随着颜色变化,下列关于颜色的叙述正确的是( )
①鸡蛋白溶液遇浓硝酸——黄色 ②淀粉溶液遇碘离子——蓝色
③溴化银见光分解——白色 ④热的氧化铜遇乙醇——红色
⑤新制氯水久置后——无色 ⑥过氧化钠在空气中久置——淡黄色
⑦Fe3+离子遇苯酚——紫色 ⑧石蕊试液中通二氧化硫气体——无色.
A.①②③⑧ B.②③④⑥ C.①④⑤⑦ D.②④⑤⑦
难度: 中等查看答案及解析
-
在一定温度下,将等物质的量的CO和水蒸气通入恒容密闭容器中,发生如下反应:CO(g)+H2O(g)
CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是( )
A. 正反应速率等于零 B. 正反应速率大于逆反应速率
C. 正反应速率等于逆反应速率 D. 正反应速率小于逆反应速率
难度: 简单查看答案及解析
-
干冰灭火器常用于扑救档案资料室发生的火灾,下列关于干冰灭火的说法不正确的是( )
A.干冰升华时吸热,降低可燃物的着火点 B.CO2覆盖在可燃物表面,隔绝空气
C.CO2不能支持燃烧 D.干冰升华后不污染档案资料
难度: 简单查看答案及解析
-
一定条件下,对于可逆反应N2(g)+3H2(g)
2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A.C1:C2=1:3
B.平衡时,H2和NH3的生成速率之比为2:3
C.N2、H2的转化率之比为1:3
D.C1的取值范围为0.04 mol·L-1<C1<0.14 mol·L-1
难度: 中等查看答案及解析
-
在一密闭的容器中,将一定量的NH3加热使其发生分解反应:2NH3(g)
N2(g)+3H2(g),当达到平衡时,测得25%的NH3分解,此时容器内的压强是原来的( )
A. 1.125倍 B. 1.25倍
C. 1.375倍 D. 1.5倍
难度: 中等查看答案及解析
-
某同学设计了一种电解法制取Fe(OH)2的实验装置(如图)。通电后,溶液中产生白色沉淀,且较长时间不变色。下列说法中正确的是( )
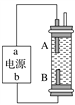
A.电源中a为负极,b为正极
B.电解池中的电解液不可以是NaCl溶液
C.B电极发生的反应:2H++2e-=H2↑
D.A、B两端都必须使用铁作电极
难度: 中等查看答案及解析
-
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
A.NH4HCO3和盐酸的反应是放热反应
B.NH4HCO3和盐酸的反应是吸热反应
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl==NH4Cl+CO2↑+H2O ΔH=+Q kJ/mol
难度: 中等查看答案及解析
-
下列式子中,属于水解反应的是( )
A.H2O+H2O
H3O++OH- B.
+H2O
+OH-
C.NH3+H2O
NH3·H2O D.
+OH-
H2O+
难度: 简单查看答案及解析
-
化工生产中常用MnS作为沉淀剂除去工业废水中Cu2+:Cu2+(aq)+MnS(s)
CuS(s)+Mn2+(aq),下列说法错误的是( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=
难度: 简单查看答案及解析
-
右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是
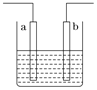
A.a、b不可能是同种材料的电极
B.该装置可能是电解池,电解质溶液为稀盐酸
C.该装置可能是原电池,电解质溶液为稀盐酸
D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A.在熔融和溶解时均不导电的化合物,叫做非电解质
B.电解质、非电解质都是对化合物而言,单质不在此范畴
C.强电解质溶液的导电能力不一定比弱电解质溶液强
D.在水中导电的物质一定是电解质
难度: 简单查看答案及解析
-
已知酸性大小:羧酸>碳酸>酚。下列含溴化合物中的溴原子,在适当的条件下都能被羟基(—OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是
A.
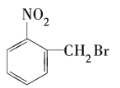 B.
B. C.
C.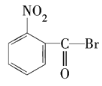 D.
D.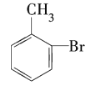
难度: 中等查看答案及解析
-
中和热测定实验中,下列操作一定会降低实验准确性的是( )
A.用滴定管取所用药品
B.NaOH溶液在倒入小烧杯时,有少量溅出
C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
难度: 简单查看答案及解析
-
下列说法正确的是
A.HR溶液的导电性较弱,HR属于弱酸
B.某化合物溶于水导电,则该化合物为电解质
C.根据电解质在其水溶液中能否完全电离,将电解质分为强电解质和弱电解质
D.食盐是电解质,食盐的水溶液也是电解质
难度: 简单查看答案及解析
-
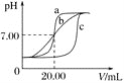
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )
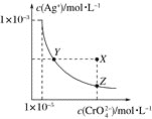
A.t℃时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t℃时,将0.01 mol·L-1AgNO3溶液滴入20 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
难度: 困难查看答案及解析
-
某炔烃经催化加氢后,得到2-甲基丁烷,该炔烃是:
A.2-甲基-1-丁炔 B.2-甲基-3-丁炔 C.3-甲基-1-丁炔 D.3-甲基-2-丁炔
难度: 中等查看答案及解析
-
下列有关滴定操作的顺序正确的是( )
①检查滴定管是否漏水 ②用蒸馏水洗涤玻璃仪器
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤取一定体积的待测液于锥形瓶中 ⑥滴定操作
A.①③②④⑤⑥ B.①②③④⑤⑥ C.②③①④⑤⑥ D.④⑤①②③⑥
难度: 简单查看答案及解析
-
下列有机分子中,所有的原子不可能处于同一平面的是( )
A.CH2=CH-CN
B.CH2=CH-CH=CH2
C.
D.
难度: 中等查看答案及解析
-
能源可划分为一级能源和二级能源,直接来自自然界的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源。氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(l)
2H2(g)+O2(g),该反应需要吸收大量的热,下列叙述正确的是( )
A.水煤气是二级能源 B.水力是二级能源
C.天然气是二级能源 D.电能是一级能源
难度: 简单查看答案及解析