-
“一带一路”建设是东西方经济、文化、政治交流的重要纽带。下列相关事项中,主要涉及物理变化的是( )
A.种桑养蚕,印染丝绸 B.制胎施釉,烧制瓷器
C.医疗援助,消毒防疫 D.铁路铺设,压实底碴
难度: 简单查看答案及解析
-
绿色化学又称“清洁化学”、“环境友好化学”,其核心是利用化学原理从源头上减少和消除工业生产对环境的污染。反应原料应符合“5R”原则,其最理想的化工生产方式就是 反应物的原子全部转化为期望的最终产物,实现原料原子的“零排放”。下列相关叙述中,不正确的是( )
A. 地沟油经处理转化为航空煤油,能变废为宝
B. 废旧金属回收循环利用,可节约能源和资源
C. 拒绝使用一切塑料制品,避免产生白色污染
D. 侯德榜创立联合制碱法,优化了纯碱生产工艺
难度: 简单查看答案及解析
-
化学与生产、生活密切相关。下列有关说法中错误的是( )
A.用干冰冷藏食品优点多
B.铵态氮肥不可与碱性物质混用
C.用工业酒精勾兑饮用酒
D.焙制面包时可加入适量小苏打
难度: 简单查看答案及解析
-
在下列实验操作中,没有科学、规范地运用人体五官的是( )。
A.
 鼻闻盐酸气味 B.
鼻闻盐酸气味 B. 耳听氢气验纯的声音
耳听氢气验纯的声音C.
眼观量筒刻度 D.
 嘴吹灭酒精灯
嘴吹灭酒精灯难度: 简单查看答案及解析
-
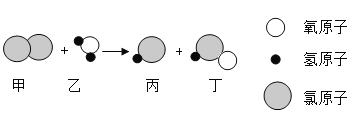
根据如图信息进行判断,下列有关说法中错误的是( )。

A.甲微粒可表示为 Cl-
B.乙微粒的相对原子质量是 35.5g
C.甲、乙两种微粒均属于氯元素
D.甲、乙两种微粒具有不同的化学性质
难度: 简单查看答案及解析
-
如图所示为探究分子性质的小实验。一段时间后,观察到试管内滴在滤纸条上相同间距的酚酞液滴从左到右依次变红,而棉花没有明显现象。
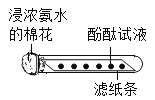
下列有关该实验的说法中,不正确的是
A.浓氨水具有挥发性 B.酚酞具有挥发性 C.氨分子在不断运动 D.浓氨水显碱性
难度: 中等查看答案及解析
-
逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A.催化剂可以加快化学反应速率,也可以增加生成物的质量
B.置换反应一定有单质生成,有单质生成的反应一定是置换反应
C.盐通常是由金属离子和酸根离子构成的,NH4NO3中没有金属离子,但它也属于盐
D.将氯化氢和二氧化碳分别通入紫色石蕊试液中,溶液都变为红色,所以它们都属于酸
难度: 简单查看答案及解析
-
对照实验是运用比较的方法来揭示事物的性质或变化规律的一种实验方法。下列对照实验设计中,明显欠缺变量控制而缺乏科学严谨性的是( )。
A.
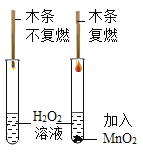 比较催化剂对化学反应速率的影响
比较催化剂对化学反应速率的影响B.
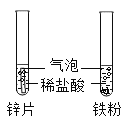 比较反应物接触面积对反应速率的影响
比较反应物接触面积对反应速率的影响C.
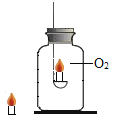 比较反应物浓度对反应速率的影响
比较反应物浓度对反应速率的影响D.
 比较反应条件对反应产物种类的影响
比较反应条件对反应产物种类的影响难度: 困难查看答案及解析
-
人类的日常生活和工农业生产离不开水。下列有关说法中,不正确的是( )。
A.天然水经过自然沉降、过滤、吸附,即可得到纯水
B.将氢氧化钠固体溶于水,所得溶液的温度会明显升高
C.利用洗涤剂的乳化作用,可轻松去除衣物或餐具上的油污
D.若配制 200g 49%的硫酸溶液,可向 100g 水中慢慢加入 100g 98%的浓硫酸
难度: 中等查看答案及解析
-
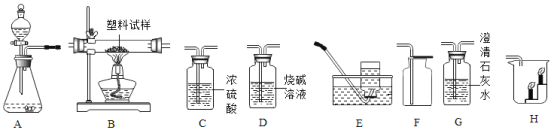
下列有关盐酸性质探究实验的叙述中,错误的是( )。
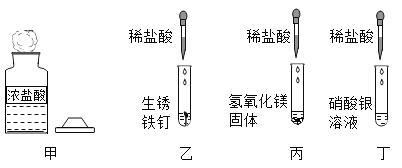
A.甲中试剂瓶口出现白雾,说明浓盐酸具有挥发性
B.乙中铁锈溶解且溶液变黄色,说明盐酸可用于除铁锈
C.丙中白色固体溶解消失,说明两者发生了中和反应
D.丁中出现白色沉淀,由此可证明盐酸中存在 H+
难度: 中等查看答案及解析
-
下列实验方案中,你认为不能达到实验目的的是( )。
选项
实 验 目 的
实 验 方 案
A.
分离获取空气中的主要组成成分
先将空气液化,再升温逐一气化
B.
检验头发中是否含有蛋白质
取样灼烧,闻气味
C.
鉴别黄金和黄铜(铜锌合金)
分别加入稀盐酸,观察现象
D.
除去 NaCl 固体中混有的少量 Na2SO4 杂质
加入过量 BaCl2 溶液,过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析