-
下列仪器中,不能作为反应容器的是
A. 试管 B. 烧杯 C. 量筒 D. 锥形瓶
难度: 简单查看答案及解析
-
铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
难度: 简单查看答案及解析
-
某农技站货架上待售的化肥有CO(NH2)2、KCl、KNO3,其中缺少的肥料品种是
A. 氮肥 B. 磷肥 C. 钾肥 D. 复合肥
难度: 简单查看答案及解析
-
下列过程中,一定发生了化学变化的是
A.水的沸腾 B.胆矾的研碎
C.比较合金和纯金属的硬度 D.石笋和钟乳石的形成
难度: 简单查看答案及解析
-
下列材料中,属于复合材料的是
A.玻璃钢 B.铝合金 C.聚乙烯塑料 D.天然橡胶
难度: 简单查看答案及解析
-
下列物质能为人体生命活动提供能量的是
A.氯化钠 B.葡萄糖 C.氮气 D.二氧化碳
难度: 简单查看答案及解析
-
下列常见物质的pH大于7的是
A.白醋 B.橘汁 C.厕所清洁剂 D.炉具清洁剂
难度: 简单查看答案及解析
-
在元素周期表中碳元素和铝元素的某些信息如图所示,下列说法正确的是、

A.碳和铝都是金属元素
B.碳的原子序数为6
C.铝是地壳中含量最多的元素
D.铝的相对原子质量为26.98g
难度: 简单查看答案及解析
-
红葡萄酒中含有某种花色苷(化学式为C16H16O6),下列说法正确的是
A.1个该花色苷分子由48个原子构成
B.该花色苷中氧元素的质量分数最小
C.该花色苷中碳、氢两种元素的质量比为12︰1
D.组成该花色苷的元素在人体中都属于微量元素
难度: 中等查看答案及解析
-
下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是
A.
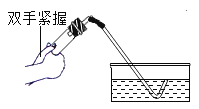 检查装置气密性 B.
检查装置气密性 B.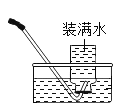 加热立即收集
加热立即收集C.
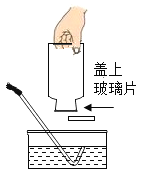 收满后移出集气瓶 D.
收满后移出集气瓶 D.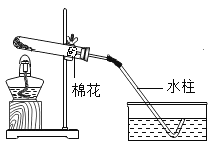 结束时停止加热
结束时停止加热难度: 中等查看答案及解析
-
下列有关二氧化碳的制取与性质的说法中,不正确的是
A.实验室里可用大理石(或石灰石)与稀盐酸反应来制取二氧化碳
B.二氧化碳能使澄清石灰水变浑浊,该反应可以用来检验二氧化碳
C.过量二氧化碳可能使人窒息死亡,因为二氧化碳是极易与血红蛋白结合的有毒气体
D.碳与二氧化碳在高温的条件下反应生成一氧化碳,该反应中二氧化碳表现出氧化性
难度: 中等查看答案及解析
-
下列叙述正确的是
A.钢的性能优良,所以钢是纯铁
B.C、CO、H2都能通过置换反应还原Fe2O3
C.可以通过灼烧的方法区分羊毛织物和纯棉织物
D.金刚石、石墨和C60都是由碳原子构成的单质
难度: 简单查看答案及解析
-
下列各组离子在水中能大量共存的是
A.H+、Na+、NO3-、CO32- B.Na+、Cu2+、OH-、SO42-
C.K+、Ag+、Cl-、NO3- D.H+、NH4+、Cl-、SO42-
难度: 中等查看答案及解析
-
除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是
A.CO2(HCl)—— 依次通过足量的NaOH溶液和浓硫酸
B.H2(HCl)—— 依次通过足量的NaHCO3溶液和浓硫酸
C.KCl溶液(CaCl2)—— 加入足量的Na2CO3溶液,过滤
D.木炭粉(CuO)—— 加入足量的稀硫酸,过滤,洗涤,干燥
难度: 中等查看答案及解析
-
29g某纯净物在氧气中完全燃烧,生成88g二氧化碳和45g水,已知该纯净物的相对分子质量为58,则其化学式为
A.C2H5 B.C4H10 C.C2H2O2 D.C3H6O
难度: 中等查看答案及解析