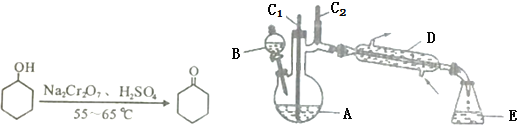
-
化学与环境保护密切相关,下列叙述正确的是
A. 家庭装修所产生的甲醛、苯等有害物质可用水溶解吸收
B. 处理废水时加入明矾作为消毒剂对水进行杀菌消毒
C. 含汞废旧电池需回收处理是因为重金属离子污染土壤和水体
D. 某酸雨样品放置过程中pH减小是因为溶解了更多的CO2
难度: 中等查看答案及解析
-
化合物
(b)、
(d)、CH≡C-CH=CH2(p)的分子式均为C4H4。下列说法正确的是
A. b的同分异构体只有d和p两种
B. 只有b的所有原子处于同一平面
C. b、d、p均可与酸性高锰酸钾溶液反应
D. d的一氯代物和二氯代物均只有一种
难度: 困难查看答案及解析
-
X、Y、Z、W、Q是原子序数逐渐增大的短周期主族元素,其中Z、W为金属元素,Q是同一周期中非金属性最强的元素,且过量的XY2能与由Y、Z、W三种元素组成的一种化合物的水溶液反应得到一种白色沉淀,该白色沉淀能溶于过量的NaOH溶液,但不溶于氨水。下列说法正确的是
A.原子半径:Q>Z>W
B.熔融WQ3固体时需要破坏离子键
C.Z、W、Q三种元素的最高价氧化物对应的水化物两两之间能相互反应
D.非金属性:Y<Q
难度: 中等查看答案及解析
-
下列各组中微粒能大量共存,且当加入试剂后反应的离子方程式书写正确的是( )
选项
微粒组
加入的试剂
发生反应的离子方程式
A
Fe3+、I−、Cl−
NaOH溶液
Fe3++3OH−═Fe(OH)3↓
B
K+、NH3⋅H2O、CO32−
通入少量CO2
2OH−+CO2═CO32−+H2O
C
H+,Fe2+、SO42−
Ba(NO3)2溶液
SO42−+Ba2+═BaSO4↓
D
Na+、Al3+、Cl−
少量澄清石灰水
Al3++3OH−═Al(OH)3↓
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
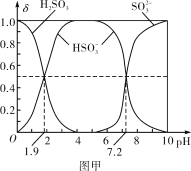
常温下,下列有关叙述正确的是( )
A. 向0.1mol/LNa2CO3溶液中通入适量
气体后:
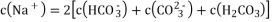
B. pH=6的NaHSO3溶液中:
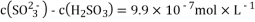
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:
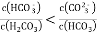
D. 0.1mol/LNa2C2O4溶液与0.1mol/LHCl溶液等体积混合(H2 C2O4为二元弱酸):
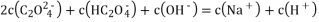
难度: 中等查看答案及解析
-
下列实验可以达到目的是( )
选项
实验目的
实验过程
A
探究浓硫酸的脱水性
向表面皿中加入少量胆矾,再加入约3mL浓硫酸,搅拌,观察实验现象
B
制取干燥的氨气
向生石灰中滴入浓氨水,将产生的气体通过装有P2O5的干燥管
C
制备氢氧化铁胶体
向饱和氯化铁溶液中滴加氨水
D
除去MgCl2溶液中少量FeCl3
向溶液中加入足量MgO粉末,充分搅拌后过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
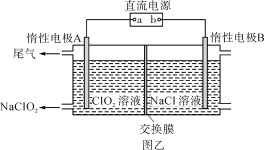
我国科学家发明了一种安全可充电的柔性水系钠离子电池,可用生理盐水或细胞培养基为电解质,电池放电的总反应式为:Na0.44MnO2+NaTi2(PO4)3=Na0.44-xMnO2+Na1+xTi2(PO4)3,其工作原理如下图。
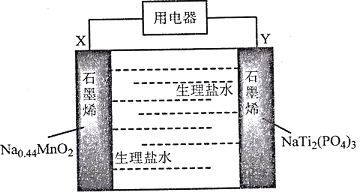
下列说法错误的是
A. 放电时,Cl-向X极移动
B. 该电池充电时Y极应该与电源的正极相连
C. 充电时,阴极反应为:NaTi2(PO4)3+xNa++xe-=Na1+ xTi2( PO4)3
D. 该电池可能作为可植入人体的电子医疗设备的电源
难度: 中等查看答案及解析
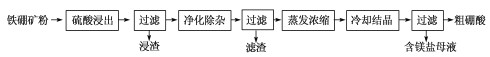
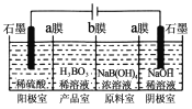
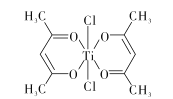

 。参照上述合成路线,设计一条由苯和乙酸为起始原料制备
。参照上述合成路线,设计一条由苯和乙酸为起始原料制备