-
下列有关甲烷及其氯代物说法正确的是
A.甲烷及其氯代物中都只存在极性键 B.甲烷及其氯代物都是正四面体结构
C.甲烷性质稳定,但可以被酸性高锰酸钾溶液氧化 D.甲烷与氯气发生取代反应时,共生成四种物质
难度: 简单查看答案及解析
-
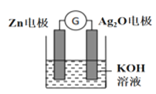
下列有关电池的说法不正确的是
A.手机上用的锂离子电池属于二次电池 B.锌锰干电池中,锌电极是负极
C.甲醇燃料电池可把化学能转化为电能 D.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
难度: 简单查看答案及解析
-
加成反应是有机化学中的一类重要的化学反应,下列属于加成反应的是( )
A.甲烷与氯气混合后在光照条件下反应
B.乙烯与溴的四氯化碳溶液反应
C.乙烯使酸性高锰酸钾溶液褪色
D.在苯中滴入溴水,溴水褪色
难度: 中等查看答案及解析
-
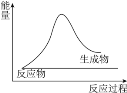
下列图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中不正确的是
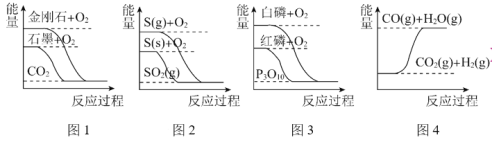
A.图1石墨转变为金刚石是吸热反应 B.图2等质量的S(g)完全燃烧放出的热量大于S(s)
C.图3白磷比红磷稳定 D.图4CO(g)+H2O(g)=CO2(g)+H2(g)为放热反应
难度: 简单查看答案及解析
-
比较乙烷和乙醇的结构,下列说法错误的是
A.两个碳原子以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
难度: 中等查看答案及解析
-
已知2SO2(g)+O2(g)
2SO3(g)为放热反应,则下列说法正确的是
A.单位时间内生成2molSO2,同时生成1molO2,说明反应达到平衡状态
B.上述热化学反应方程式说明反应物的总键能小于生成物的总键能
C.升高温度,正反应速率增大,逆反应速率减小
D.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后生成2molSO3(g)
难度: 中等查看答案及解析
-
下列对乙烯分子的叙述中错误的是
A.乙烯的电子式为
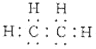 B.乙烯分子里碳碳双键中有一个键不稳定
B.乙烯分子里碳碳双键中有一个键不稳定C.乙烯分子中碳氢键之间的夹角约为120° D.乙烯分子中既含有极性键又含有非极性键
难度: 简单查看答案及解析
-
在2L容积不变的容器中,发生N2+3H2⇌2NH3的反应.现通入4molH2和4molN2,10s内用H2表示的反应速率为0.12mol/(L•s),则10s后容器中N2的物质的量是
A.3.6mol B.3.2mol C.2.8mol D.1.6mol
难度: 简单查看答案及解析
-
少量铁片与100mL0.01mol/L的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H2的产量,可以使用如下方法中的:
①加H2O ②加KNO3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加入少量CH3COONa固体 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol/L盐酸
A.③⑦⑧ B.③⑤ C.①⑥⑦ D.③④⑥⑦⑧
难度: 中等查看答案及解析
-
一定温度下,在某恒容的密闭容器中,建立化学平衡:C(s)+H2O(g)
CO(g)+H2(g)。下列叙述中能说明该反应已达到化学平衡状态的是
A.体系的压强不再发生变化 B.v(CO)=v(H2O)
C.生成nmolCO的同时生成nmolH2 D.1molH-H键断裂的同时形成2molH-O键
难度: 简单查看答案及解析
-
一定温度下的恒容容器中,下列哪些物理量不再发生变化时,不能表明反应A(g)+2B(g)
C(g)+D(g)已达到化学平衡状态
A.混合气体的密度
B.混合气体的物质的量
C.B的物质的量浓度
D.混合气体的平均相对分子质量
难度: 简单查看答案及解析
-
某种碱性氢氧燃料电池的正极反应式为:O2+4e-+2H2O = 4OH-。下列有关该电池的叙述正确的是( )
A. 工作时,电解质溶液中的OH-向正极移动
B. 负极上发生的反应为H2-2e-=2H+
C. 工作一段时间后,电解液中KOH的物质的量浓度减小
D. 若电池在工作过程中有0.4 mol电子转移,则正极消耗2.24LO2
难度: 中等查看答案及解析
-
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。关于该电池的叙述正确的是( )

A. b极发生氧化反应
B. a极为该电池的正极
C. 放电时,电流从a极经过负载流向b极
D. a极的反应式:N2H4+4OH﹣﹣4e﹣=N2↑+4H2O
难度: 中等查看答案及解析
-
在实验室中,下列除杂的方法中正确的是
A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴
B.乙烷中混有乙烯,通入H2在一定条件下反应,使乙烯转化为乙烷
C.乙烯中混有CO2和SO2,将其通入酸性KMnO4溶液中洗气
D.硝基苯中混有浓硫酸和浓硝酸,将其倒入NaOH溶液中,静置、分液
难度: 中等查看答案及解析
-
实验室用下图所示装置进行液体石蜡分解及其产物性质实验。下列操作或叙述错误的是
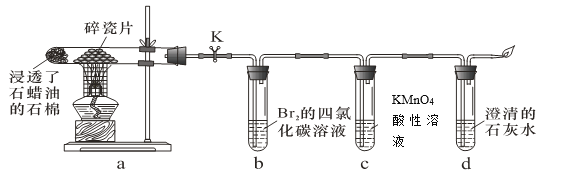
A.装置b、c中发生反应的基本类型不同 B.d中溶液变浑浊证明石蜡分解产生了CO2
C.实验中可以看到b、c中溶液褪色 D.停止加热后立即关闭K可以防止液体倒吸
难度: 中等查看答案及解析
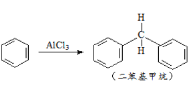 +2HCl,下列说法不正确的是
+2HCl,下列说法不正确的是 在氧气中充分燃烧,需要消耗氧气___________mol,它在光照的条件下与氯气反应,能生成_____种不同的一氯取代物。
在氧气中充分燃烧,需要消耗氧气___________mol,它在光照的条件下与氯气反应,能生成_____种不同的一氯取代物。 B.CH3CH2CH2CH2CH3C.
B.CH3CH2CH2CH2CH3C. ,其中A与B互称为__________________;B与C互称为___________________.
,其中A与B互称为__________________;B与C互称为___________________.