-
下列物质都曾用作制造口罩或面巾的材料,其中主要成分属于合成高分子化合物的是( )
A.丝 B.棉 C.聚丙烯 D.活性炭
难度: 简单查看答案及解析
-
下列各组物质的分类正确的是( )
选项
纯净物
酸
碱
盐
氧化物
A
漂白粉
H2SO4
NaOH
NaHCO3
CO
B
纯碱
HNO3
Ca(OH)2
Cu2(OH)2CO3
KClO3
C
重晶石
NaHSO4
NH3·H2O
Na2O2
Al2O3
D
蔗糖
HClO
Ba(OH)2
CuSO4
Fe2O3
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
用
表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,
所含的分子数目为
B.
环氧乙烷(
)分子中含有共价键的数目为
C.
与水反应生成
时,转移的电子数为
D.
溶液中
的数目为
难度: 简单查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使酚酞变红色的溶液:
、
、
、
B.
溶液:
、
、
、
C.
的溶液:
、
、
、
D.由水电离出的
的溶液:
、
、
、
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的的是( )
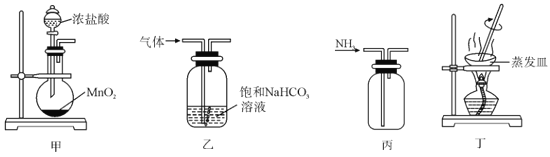
A.用装置甲制取
B.用装置乙除去
中的少量
C.用装置丙收集
D.用装置丁从
溶液中获得无水
难度: 简单查看答案及解析
-
下列关于常见有机物的说法正确的是( )
A.用酸性
溶液除去甲烷中的乙烯
B.石油分馏时,得到的产品均为纯净物
C.乙醇、水均能与钠反应,且现象相同
D.在加热条件下,葡萄糖能与含氢氧化钠的氢氧化铜悬浊液发生反应
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.铁制器具表面涂油,可防止其锈蚀
B.
使氯水褪色,证明
具有漂白性
C.在空气中蒸干
溶液可获得
固体
D.浓盐酸敞口放置浓度会降低,说明其具有吸水性
难度: 中等查看答案及解析
-
下列化学反应的离子方程式表示正确的是( )
A.向
溶液中通入足量的
B.向澄清石灰水中加入少量的
C.向
溶液中加入
溶液至
沉淀完全:
D.向
沉淀中滴加氢碘酸(HI的水溶液):
难度: 中等查看答案及解析
-
相比锂离子电池,钠离子电池具有原材料丰富、成本低、无过放负载电特性等优点。一种可充电钠离子电池的工作原理如图所示(两电极材料均不溶于水,P为
价),下列说法正确的是( )
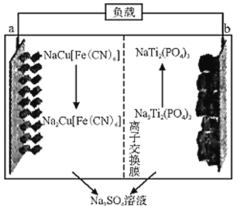
A.放电过程中Ti元素的化合价由
降低到
B.充放电过程中电解质溶液中
基本保持不变
C.充电过程中
通过离子交换膜从右室移向左室
D.充电时阴极反应为
难度: 中等查看答案及解析
-
已知断裂
化学键吸收的能量如下表所示:
化学键
C=C
C-C
C-H
H-H
键能(
)
615
348
413
436
则反应
的
为( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期且相邻,Y是地壳中含量最多的元素,Z是短周期中原子半径最大的主族元素,W的单质常温下是一种淡黄色固体。下列叙述正确的是( )
A.元素的非金属性:
B.Z的单质在空气中燃烧生成阴、阳离子个数比为
的氧化物
C.Y的简单气态氢化物的稳定性强于W的
D.工业上一般采用电解对应盐的水溶液制Z单质
难度: 中等查看答案及解析
-
下列有关实验的现象和结论都正确,且二者具有因果关系的是( )
选项
操作
现象
结论
A
向久置的Na2O2粉末中滴加过量盐酸
有无色无味气体生成
Na2O2没有变质
B
向NaAlO2溶液中通入足量CO2
有白色沉淀生成
Al(OH)3不溶于弱酸
C
室温下,将Cu置于浓硫酸中
无现象
在浓硫酸中Cu表面形成致密氧化膜阻止进一步反应
D
向溶液X中先滴加稀硝酸,再滴加BaCl2溶液
有白色沉淀生成
溶液X中含有Ag+或
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
工业上可由苯和丙烯合成异丙苯:
+CH3CH=CH2
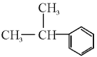 ,下列说法错误的是( )
,下列说法错误的是( )A.异丙苯分子中所有碳原子可能在同一平面内
B.异丙苯分子的一溴代物共有5种
C.可以用溴水鉴别异丙苯和丙烯
D.丙烯能发生加成反应、氧化反应
难度: 简单查看答案及解析
-
常温下,向
溶液中滴加
溶液,混合溶液
与所加
溶液体积的关系如图所示。下列说法正确的是( )

A.a点溶液:
B.b点溶液:
C.c点溶液:
D.d点溶液中由水电离产生的
难度: 中等查看答案及解析