-
现代社会,人们越来越关注饮食中的营养成分。虾皮、海带和豆腐等食物含有丰富的钙,这里的钙应理解为( )
A.单质 B.分子 C.元素 D.同位素
难度: 简单查看答案及解析
-
鉴别溶液和胶体可以采用的方法是
A. 蒸发 B. 从外观观察
C. 稀释 D. 利用丁达尔现象实验
难度: 简单查看答案及解析
-
氧化铁为红棕色粉末,用于油漆、油墨、橡胶等工业中的着色,是无机颜料,在涂料工业中用作防锈颜料,氧化铁属于( )
A.酸 B.碱 C.盐 D.氧化物
难度: 简单查看答案及解析
-
下列关于二氧化氮的说法错误的是( )
A.无色无味 B.有毒 C.密度比空气大 D.氧化物
难度: 简单查看答案及解析
-
臭氧(分子中含有三个氧原子)主要存在于距地球表面20公里的同温层下部的臭氧层中,它吸收对人体有害的短波紫外线。下列元素与氧元素处于同一主族的是 ( )
A.He B.S C.Si D.P
难度: 简单查看答案及解析
-
下列各组物质互为同分异构体的是( )
A.金刚石和石墨 B.CH3CH2CH2CH2CH3和C(CH3)4
C.16O和18O D.乙醇和乙酸
难度: 简单查看答案及解析
-
某溶液中存在大量的Cl-、SO
、H+。该溶液中还可能大量存在的离子是 ( )
A.Na+ B.Ba2+ C.OH- D.Ag+
难度: 简单查看答案及解析
-
下列物质不含有离子键的是( )
A.NaOH B.NaCl C.NH4Cl D.H2O
难度: 简单查看答案及解析
-
下列药品中,不需要密封保存的是 ( )
A.烧碱 B.澄清石灰水 C.浓硫酸 D.氯化钠
难度: 简单查看答案及解析
-
2012年12月7日日本明治奶粉检测出放射性核素铯
Cs而被召回,下列有关铯原子(
Cs)的说法错误的是( )
A.原子序数为55 B.电子数是55 C.中子数是137 D.质量数是137
难度: 简单查看答案及解析
-
下列措施是为了减慢化学反应速率的是
A.合成氨工业中使用催化剂
B.用铁粉代替铁钉与稀硫酸反应制取氢气
C.食品放在冰箱中贮藏
D.在试管中进行铝和盐酸反应时,稍微加热
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32— =CO2↑+ H2O
B.用氢氧化钠检验氯化铵溶液中铵根离子:NH4+ + OH-
NH3 ↑+ H2O
C.在硫酸铜溶液中加入过量氢氧化钡溶液 Ba2++SO42—=BaSO4↓
D.氯气与NaOH溶液反应:Cl2 + OH-= Cl- + ClO- + H2O
难度: 中等查看答案及解析
-
关于化学反应的说法错误的是( )

A. 如图所示的反应为放热反应
B. 化学反应中有物质变化也有能量变化
C. 需要加热的化学反应不一定是吸热反应
D. 化学键断裂吸收能量,化学键形成放出能量
难度: 简单查看答案及解析
-
某物质在氧气中完全燃烧,产物只有二氧化碳和水,则该物质不可能是( )
A.甲烷 B.乙醇 C.蛋白质 D.纤维素
难度: 简单查看答案及解析
-
取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是 ( )
A.丙烷与氯气在光照的作用下生成氯丙烷的反应
B.乙烯与水生成乙醇的反应
C.乙烯与溴的四氯化溶液生成溴乙烷的反应
D.乙烯自身生成聚乙烯的反应
难度: 简单查看答案及解析
-
下列有关实验原理或操作正确的是 ( )
A.闻气体气味
 B.稀释浓硫酸
B.稀释浓硫酸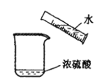
C.转移溶液
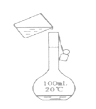 D.点燃酒精灯
D.点燃酒精灯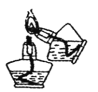
难度: 简单查看答案及解析
-
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。在下列反应中只体现过氧化氢的还原性的反应是 ( )
A.2H2O2=2H2O+O2↑
B.H2O2+SO2=H2SO4
C.H2O2+HI=I2+2H2O
D.5 H2O2+2KMnO4+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A.硫酸铝的电离方程式:Al2(SO4)3=Al3++SO
B.氨气的电子式:
C.乙醇的结构简式:C2H6O D.14C的原子结构示意图:
难度: 简单查看答案及解析
-
用nA表示阿伏加德罗常数的值。下列说法正确的是 ( )
A.22.4L氢气中含有的氢分子数目是NA
B.1mol钠作还原剂可提供的电子数是NA
C.物质的量浓度为1 mol/LBaCl2含有Cl-数目是2 NA
D.1mol OH-所含有的电子数是9 NA
难度: 中等查看答案及解析
-
在下列自然资源的开发利用中,不涉及化学变化的是( )
A.从石油中通过分馏得到汽油、煤油和柴油
B.从煤中得到焦炉煤气、煤焦油和焦炭
C.以煤、石油和天然气为原料生产合成材料
D.从海水中提取溴
难度: 简单查看答案及解析
-
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A.a为负极,是铁片,烧杯中的溶液为硫酸
B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C.a为正极,是碳棒,烧杯中的溶液可为硫酸
D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
难度: 简单查看答案及解析
-
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,下列叙述正确的是( )
A.原子半径:丙<丁<乙 B.单质的还原性:丁>丙>甲
C.甲、乙、丙的氧化物均为共价化合物 D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
硝酸工业尾气中氮的氧化物NO、NO2被氢氧化钠溶液吸收的主要反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O,现有aL(标准状况)NO和NO2混合气体被足量氢氧化钠溶液吸收,没有气体残余,下列说法不正确的是 ( )
A.实际参加反应的氢氧化钠的物质的量是a/22.4 mol
B.混合气体气体中NO2体积一定大于(等于)NO体积
C.溶液中NaNO3物质的量一定小于(等于)NaNO2物质的量
D.若生成的NaNO2与NaNO3的物质的量之比为3:1,则混合气体中NO与NO2的体积比为3:1
难度: 中等查看答案及解析