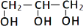-
分子式为C4H9Cl的有机物,其同分异构体的数目有( )
A. 1种 B. 2种 C. 3种 D. 4种
难度: 简单查看答案及解析
-
一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO2-+H2O。下列说法不正确的是( )
A.该电池的优点是电极材料和电解质用完后可以更换
B.该电池发生氧化反应的是金属铝
C.电极的正极反应式为3ClO-+3H2O+6e-=3Cl-+6OH-
D.当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023
难度: 中等查看答案及解析
-
少量铁片与l00mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O
②加KNO3固体
③滴入几滴浓盐酸
④加入少量铁粉
⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
⑧改用10mL 0.1mol/L盐酸.
A.②⑥⑦ B.③⑤⑧ C.③⑦⑧ D.③④⑥⑦⑧
难度: 中等查看答案及解析
-
下列各项中表达正确的是( )
A.CO2分子的电子式:
B.氯离子的结构示意图:
C.苯的结构简式:C6H6
D.水分子的球棍模型:
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数,下列有关说法正确的是( )
A.0.5mol羟基中所含电子数为5NA
B.标况下,11.2LCHCl3中,共用电子对的数目为2NA
C.2.8g的乙烯和丙烯(C3H6)中含有的碳原子数为0.2NA
D.1mol苯乙烯(
)分子中含有碳碳双键的个数为4NA
难度: 中等查看答案及解析
-
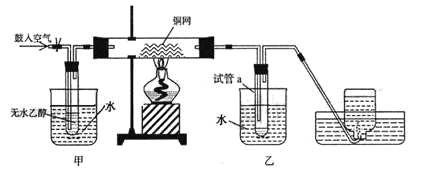
用下列实验装置进行相应实验,能达到实验目的是( )
A.验证钠与水反应是否为放热反应
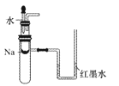
B.探究不同催化剂对反应速率的影响
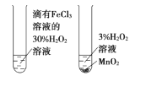
C.组装原电池
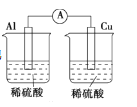
D.分离苯和硝基苯的混合液
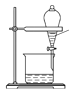
难度: 简单查看答案及解析
-
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
A.Z与Y形成的化合物可作为耐高温材料
B.WY2能与碱反应,但不能与任何酸反应
C.原子半径按X、Y、Z、R、W的顺序依次增大
D.熔沸点:X2R>X2Y
难度: 中等查看答案及解析
-
下列各组顺序的排列正确的是
A. 碱性强弱:KOH>NaOH>Mg(OH)2 B. 热稳定性:PH3>H2S>HCl
C. 单质氧化性:I2>Br2>Cl2 D. 酸性强弱:HIO4>HBrO4>HClO4
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.糖类化合物都具有相同的官能团
B.糖类、油脂、蛋白质都是高分子化合物
C.油脂的皂化反应生成高级脂肪酸和甘油
D.质量相同的苯、甲苯、乙烯、甲烷分别在足量氧气中完全燃烧时,消耗氧气物质的量最多的是甲烷
难度: 简单查看答案及解析
-
已知苯与一卤代烷在催化剂作用下可生成苯的同系物:
+CH3X→
+HX,在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
A.CH2=CH2和HCl B.CH3CH3和I2
C.CH2=CH2和Cl2 D.CH3CH3和HCl
难度: 中等查看答案及解析
-
过氧化氢(H2O2)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。H2O2能与SO2反应生成H2SO4,H2O2的分子结构如图所示。下列说法错误的是( )
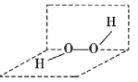
A.H2O2的结构式为H—O—O—H
B.H2O2为含有极性键和非极性键的共价化合物
C.H2O2与SO2在水溶液中反应的离子方程式为SO2+ H2O2=2H++ SO42-
D.H2O2与SO2反应过程中有共价键断裂,同时有共价键和离子键形成
难度: 中等查看答案及解析
-
如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述中,正确的说法有几项( )
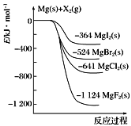
①Mg(s)所具有的能量高于MgX2(s)所具有的能量
②MgCl2电解制Mg(s)和Cl2(g)是吸热过程
③热稳定性:MgI2>MgBr2>MgCl2>MgF2
④断裂Mg(s)和X2(g)的化学键放出的能量比形成MgX2(s)的化学键吸收的能量多
A.1项 B.2项 C.3项 D.4项
难度: 简单查看答案及解析
-
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
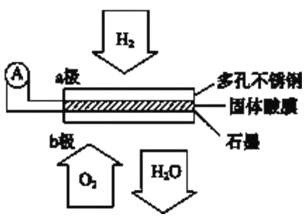
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e--=4OH--
C.每转移0.1mol电子,消耗1.12L的H2
D.H+由a极通过固体酸电解质传递到b极
难度: 简单查看答案及解析
-
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
序号
不纯物
除杂试剂
分离方法
A
CH4(C2H4)
酸性KMnO4溶液
洗气
B
苯(Br2)
NaOH溶液
过滤
C
C2H5OH(乙酸)
新制生石灰
蒸馏
D
乙酸乙酯(乙酸)
饱和Na2CO3溶液
蒸馏
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
对于密闭容器中的反应2SO3(g)⇋O2(g)+2SO2(g),在一定条件下n(SO3)和n(O2)随时间变化的关系如图所示。下列叙述正确的是( )
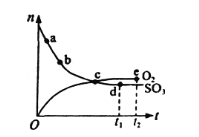
A.点c处反应达到平衡
B.点b的正反应速率比点a的大
C.点e逆反应速率为0
D.一定温度下,2SO3(g) ⇋O2(g)+2SO2(g)在恒容密闭容器中进行,充入He,压强增大,化学反应速率不变
难度: 中等查看答案及解析
-
下列关于有机物因果关系的叙述中,完全正确的一组是( )
选项
原因
结论
A
乙烯与苯都能使溴水褪色
苯分子和乙烯分子含有相同的碳碳双键
B
乙酸分子中含有羧基
可与NaHCO3溶液反应生成CO2
C
将蔗糖溶液与稀硫酸混合水浴加热,取反应后的溶液少量,加入几滴新制的Cu(OH)2悬浊液加热
出现红色沉淀
D
蔗糖和乙烯在一定条件下都能与水反应
二者属于同一反应类型
A.A B.B C.C D.D
难度: 简单查看答案及解析