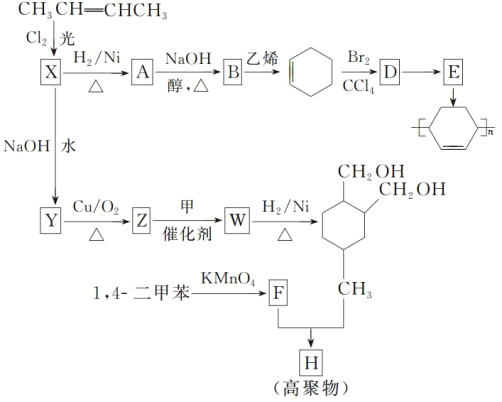
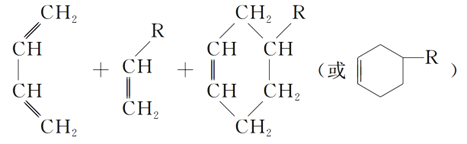
-
有机化学知识在生活中应用广泛,下列说法不正确的是( )
A.甘油加水作护肤剂
B.医用酒精的浓度为75%
C.福尔马林是甲醛的水溶液,具有杀菌防腐能力,因此可以用其保鲜鱼肉等食品
D.苯酚有毒但可以制成药皂,具有杀菌消毒的功效
难度: 简单查看答案及解析
-
下列措施不符合节能减排的是( )
A.大力发展火力发电,解决电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
难度: 中等查看答案及解析
-
下列过程中ΔH 小于零的是( )
A.Ba(OH)2 与 NH4Cl 固体混合 B.氯化铵分解得氨气
C.碳酸钙分解得二氧化碳 D.实验室制备氢气
难度: 中等查看答案及解析
-
下列关于化学反应速率的说法正确的是 ( )
A. 升高温度可降低化学反应的活化能,使化学反应速率提高
B. 在温度、体积都相同的两容器中,分别充入相同物质的量的Br2和Cl2,让它们与等量的氢气发生反应,反应速率相同
C. 0.1 mol·L-1盐酸和0.1 mol·L-1硝酸与相同形状和大小的大理石反应的速率相同
D. 有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加活化分子的百分数,从而使反应速率加快
难度: 中等查看答案及解析
-
下列实验事实不能证明醋酸是弱电解质的是( )
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1 mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.在相同条件下,醋酸溶液的导电性比盐酸的弱
难度: 中等查看答案及解析
-
反应H2(g) + I2(g)
2HI(g)的逆反应速率随时间变化的曲线如下图所示,t1时刻反应达到平衡,维持其他条件不变,t1时刻只改变一种条件,该条件可能是
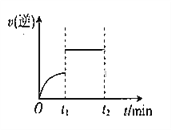
①增大H2浓度 ②缩小容器体积 ③恒容时充入Ar气 ④使用催化剂
A. ①② B. ③④ C. ②④ D. ①④
难度: 困难查看答案及解析
-
下列说法正确的是( )
A.用加热的方法可以除去 KCl 溶液中的 Fe3+
B.洗涤油污常用热的碳酸钠溶液
C.配制 FeSO4溶液时,将 FeSO4 固体溶于稀盐酸中,然后稀释至所需浓度
D.将 AlCl3 溶液和 Na2SO3 溶液分别加热蒸干、灼烧后,所得固体为 Al2O3 和 Na2SO3
难度: 中等查看答案及解析
-
在常温下,pH=2 的氯化铁溶液,pH=2 的硫酸溶液,pH=12 的氨水溶液,pH=12 的碳酸钠溶液,水的电离程度分别为 a、b、c、d,则这四种溶液中,水的电离程度大小比较正确的是( )
A.a=d>b=c B.a=d>c>b C.b=c>a=d D.b=c>a>d
难度: 中等查看答案及解析
-
工业废气H2S经资源化利用后可回收能量并得到单.质硫。反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ·mol-1。H2S燃料电池的工作原理如图所示。下列有关说法不正确的是( )

A. 电极a为电池的负极
B. 电极b上的电极反应式为:O2+4H++4e-=2H2O
C. 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区
D. 若电路中通过2mol电子,则电池内部释放632kJ热能
难度: 中等查看答案及解析
-
在某温度下,将 2 mol A 和 3 mol B 充入一密闭容器中,发生反应:aA(g)+B(g)
C(g)+D(g),5 min 后达平衡,已知各物质的平衡浓度的关系为 ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的 10 倍,A 的转化率没有发生变化, 则B 的转化率为( )
A.60% B.40% C.24% D.4%
难度: 中等查看答案及解析
-
在容积一定的密闭容器中,置入一定量的 NO(g)和足量C(s),发生反应 C(s)+2NO(g)
CO2(g)+N2(g),平衡状态时 NO(g)的物质的量浓度 c(NO)与温度 T 的关系如图所示。则下列说法中正确的是( )
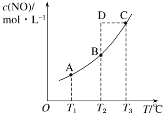
A.该反应的 ΔH>0 B.若该反应在 T1、T2 时的平衡常数分别为 K1、K2,则 K1<K2
C.在 T3 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 C D.在 T2 时,若反应体系处于状态D,则此时一定有 v 正<v 逆
难度: 中等查看答案及解析
-
下列各组混合物中,可以用分液漏斗分离的是
A.溴苯和水 B.苯和乙醇 C.酒精和水 D.溴苯和苯
难度: 简单查看答案及解析
-
25℃时,将1.0Lcmol/LCH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH 或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是
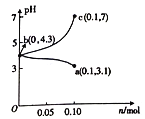
A. 该温度下,醋酸的电离平衡常数Ka=
B. a点对应的混合溶液中c(CH3COOH)>c(Na+)>c(OH-)
C. 水的电离程度:c>b>a
D. 当混合溶液呈中性时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
难度: 困难查看答案及解析
-
下列说法正确的是( )
A. PH=1的醋酸加水稀释到原体积的100倍,稀释后PH=3
B. 室温 pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性
C. 室温pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D. 某温度下,水的离子积常数为1×10-12,该温度下PH=7的溶液呈中性
难度: 中等查看答案及解析
-
已知298 K时,合成氨反应N2(g)+3H2(g)
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)
A.一定小于92.0 kJ B.一定大于92.0 kJ
C.一定等于92.0 kJ D.无法确定
难度: 中等查看答案及解析
-
NH4Cl溶于重水(D2O)后,产生的一水合氨和水合氢离子均正确的是
A.NH2D·H2O和D3O+ B.NH3·D2O和HD2O+
C.NH3·HDO和D3O+ D.NH2D·HDO和H2DO+
难度: 简单查看答案及解析
-
在25℃某稀溶液中,由水电离产生的c(H+)=10-13mol·L-1。下列有关该溶液的叙述正确的是( )
A.该溶液一定呈酸性 B.该溶液一定呈碱性
C.该溶液的pH一定为1 D.该溶液的pH可能为13
难度: 中等查看答案及解析
-
为了鉴定溴乙烷中溴元素的存在,试分析下列各步实验,其中操作顺序合理的是
①加入AgNO3溶液 ②加入NaOH溶液 ③加热
④用HNO3酸化溶液 ⑤加入NaOH溶液醇溶液
A.①②③⑤ B.②③④① C.④③⑤① D.④②⑤③
难度: 中等查看答案及解析
-
下列离子方程式正确的是 ( )
A.尼泊金酸与碳酸氢钠反应:
+2HCO
+2CO2
+2H2O
B.醋酸溶液与新制氢氧化铜反应:2 H++Cu(OH)2→Cu2++2H2O
C.苯酚钠溶液中通入少量二氧化碳: C6H5O-+CO2 +H2O → C6H5OH+HCO
D.甲醛溶液与足量的银氨溶液共热HCHO+2[Ag(NH3)2]++2OH-
CO
+2NH
+ 2Ag↓+ 2NH3+ H2O
难度: 中等查看答案及解析
-
常见有机反应类型有:①取代反应、②加成反应、③消去反应、④酯化反应、⑤加聚反应、⑥氧化反应、⑦还原反应,其中能在有机物中引入羟基的反应类型是
A. ①②③ B. ①②⑦ C. ⑤⑥⑦ D. ③④⑥
难度: 困难查看答案及解析