-
将少量氯水加入盛有KBr溶液的试管中,再加入适量的汽油,然后振荡,静置,产生的现象是( )
A. 溶液呈橙色 B. 溶液呈无色
C. 上层液体呈橙色,下层液体几乎无色 D. 上层液体呈紫红色,下层液体几乎无色
难度: 简单查看答案及解析
-
下列变化中只有通过还原反应才能实现的是( )
A. Fe3+→Fe2+ B.Mn2+→MnO4- C.Cl-→Cl2 D.N2O3→HNO2
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.1molN2的质量是14g B.H2SO4的摩尔质量是98g
C.H2O的摩尔质量是18 g /mol D.1mol HCl的质量是36.5g/mol
难度: 简单查看答案及解析
-
下列物质中既能导电,又属于强电解质的一组物质是( )
A.石墨、醋酸溶液、食盐晶体
B.熔融状态的KOH、熔融状态的NaCl
C.稀H2SO4、NaOH溶液、纯HNO3
D.液氨、石灰水、水银
难度: 简单查看答案及解析
-
下列离子反应方程式中,正确的是( )
A.铁与稀硫酸反应 Fe+2H+=Fe3++H2↑
B.二氧化碳与水反应 CO2+H2O=2H++CO32-
C.碳酸钡与盐酸反应 CO32—+2H+=H2O+CO2↑+Ba2+
D.氢氧化钠溶液与硫酸铜溶液反应 2OH—+Cu2+=Cu(OH)2↓
难度: 简单查看答案及解析
-
24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A.+2 B.+3 C.+4 D.+5
难度: 中等查看答案及解析
-
两份铝片,一份与足量盐酸反应,另一份与足量烧碱溶液反应,同温、同压下,放出相同体积的气体,则两份铝片的质量之比为( )
A.1:1 B.2:3 C.3:2 D.1:6
难度: 简单查看答案及解析
-
当钠、钾等金属不慎着火时,可以用来灭火的是:( )
A.水 B.煤油 C.沙子 D.泡沫灭火剂
难度: 简单查看答案及解析
-
在自然界中,既有以化合态存在,又有以游离态存在的元素是( )
A.碳 B.钠 C.镁 D.铝
难度: 简单查看答案及解析
-
下列各组离子,能大量共存于同一溶液中的是 ( )。
A.CO32-. H + . Na + . NO3- B.H + . Ag+ . Cl-. SO42-
C.K+ . Na + . OH- .NO 3- D.Ba2+ .Ca 2+ .SO42- . OH-
难度: 简单查看答案及解析
-
血液属于胶体,透析是除去肾衰竭病人血液中的毒性物质、从而拯救病人生命的重要方法。透析的原理是
A.蒸发 B.电泳 C.过滤 D.渗析
难度: 简单查看答案及解析
-
配制100 mL 1.0 mol/LNa2CO3溶液,下列操作正确的是
A.称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B.称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C.转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D.定容后,塞好瓶塞,反复倒转、摇匀
难度: 中等查看答案及解析
-
对于反应MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,下列说法正确的是
A.MnO2是还原剂 B.MnCl2是氧化产物
C.Cl2是氧化产物 D.H2O是还原产物
难度: 简单查看答案及解析
-
现有三组实验:①除去混在植物油中的水;②对碘水中的碘进行浓缩;③对30%的酒精溶液中的酒精进行提纯。以上实验采用的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
在溶液导电性实验中,往氢氧化钡溶液中滴加硫酸至过量,灯泡的明亮度变化是:明→暗→明,下列说法正确的是( )
A.溶液的导电性与溶液中离子的浓度有关
B.溶液的导电性与溶液中离子数目的多少有关
C.灯泡最暗时溶液中无任何电解质
D.往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同
难度: 简单查看答案及解析
-
下列有关Na2CO3和NaHCO3性质的比较中,正确的是 ( )
A.等浓度的溶液中滴入稀盐酸,放出气体的快慢Na2CO3<NaHCO3 B.热稳定性Na2CO3<NaHCO3
C.常温时水溶性Na2CO3<NaHCO3 D.相对分子质量Na2CO3<NaHCO3
难度: 中等查看答案及解析
-
要证明某溶液中含Fe2+而不含有Fe3+,进行如下实验操作时最佳顺序为( )
①加入足量氯水 ②观察到无现象 ③加入少量KSCN溶液
A.①③② B.③①② C.③②① D.①②③
难度: 简单查看答案及解析
-
只用一种试剂区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、FeCl3五种溶液,这种试剂是( )
A.Ba(OH)2 B.H2SO4 C.NaOH D.AgNO3
难度: 简单查看答案及解析
-
将5.6LCO2气体缓慢通过一定量的Na2O2固体后,得到3.36L气体(气体体积均在标准状况下测定),所得气体的质量为( )
A.3.8g B.4.8g C.5.4g D.6.6g
难度: 中等查看答案及解析
-
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol/LNaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,则原合金中镁与铝的物质的量之比为( )
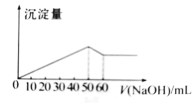
A.1:1 B.1:2 C.2:3 D.3:2
难度: 简单查看答案及解析